Clear Sky Science · pt
Atlas de núcleos únicos da amígdala central revela dinâmica da cromatina e da transcrição gênica no transtorno por uso de álcool
Por que esta pesquisa importa na vida cotidiana
O transtorno por uso de álcool (TUA) afeta milhões de pessoas e suas famílias, mas ainda sabemos surpreendentemente pouco sobre o que o consumo pesado e prolongado faz ao cérebro humano no nível de células individuais. Este estudo focaliza uma região pequena, porém crítica — a amígdala central, um centro para medo, estresse e motivação — para mapear como o álcool remodela as células cerebrais e seus sistemas de controle genético. Ao combinar a técnica avançada de sequenciamento “de célula única” com estudos genéticos sobre risco de dependência, os autores começam a explicar por que algumas pessoas são mais vulneráveis ao TUA e como o álcool deixa cicatrizes moleculares duradouras no cérebro.
Observando de perto um pequeno núcleo cerebral
A amígdala central é uma estação de saída chave na rede emocional e do estresse do cérebro e está fortemente associada ao alívio da ansiedade, ao desejo e ao uso compulsivo de álcool. Neste trabalho, os pesquisadores analisaram cerca de 175.000 núcleos celulares individuais coletados post-mortem da amígdala central de 50 pessoas — 22 com histórico de transtorno por uso de álcool e 28 sem TUA. Usando uma tecnologia que lê tanto a atividade gênica (RNA) quanto a acessibilidade da cromatina (quão “aberto” ou “fechado” o DNA está) na mesma célula, eles construíram um atlas detalhado de todos os principais tipos celulares nessa região, incluindo vários tipos de neurônios e células de suporte como astrócitos e micróglias. Eles descobriram que os neurônios inibitórios — que atenuam ou modelam a atividade cerebral — são especialmente abundantes na amígdala central e parecem particularmente afetados em pessoas com TUA. 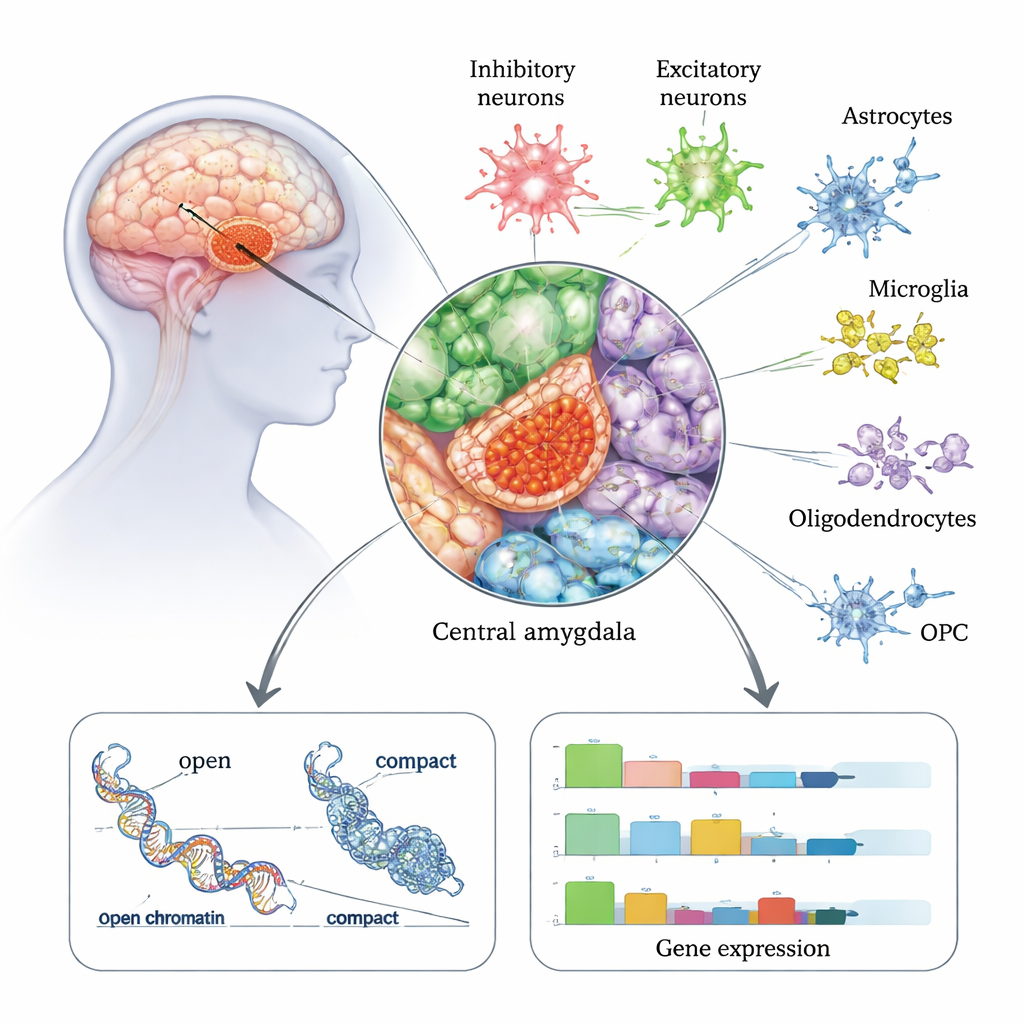
Quais células e genes mudam no transtorno por uso de álcool?
A equipe comparou sistematicamente a atividade gênica em pessoas com e sem TUA, tipo celular por tipo celular. Eles identificaram mais de 1.800 genes cuja atividade foi alterada em populações celulares específicas, com as maiores mudanças ocorrendo nos neurônios inibitórios, seguidos por neurônios excitatórios e astrócitos. Um subtipo de neurônio inibitório marcado pelo peptídeo proencefalina (PENK) mostrou alterações especialmente fortes. Muitos dos genes afetados estão envolvidos na comunicação entre células cerebrais, particularmente no equilíbrio entre o sinal excitatório glutamato e o sinal inibitório GABA. Por exemplo, o gene GABRA2, que contribui para a formação de um tipo importante de receptor GABA, apresentou aumento em certos neurônios inibitórios, enquanto GRM8, um receptor de glutamato, e NCAM1, uma molécula de adesão celular importante para sinapses, mudaram em direções opostas entre subtipos neuronais. Esses padrões sugerem que o ajuste fino da excitação e da inibição na amígdala central está perturbado no TUA.
Os interruptores de controle do cérebro: cromatina e elementos regulatórios
Os genes não atuam isoladamente; eles são controlados por trechos de DNA que funcionam como interruptores e dimmers. Ao examinar a cromatina — a forma como o DNA é embalado — os pesquisadores identificaram mais de meio milhão de elementos regulatórios candidatos e os vincularam a genes próximos de maneira específica por tipo celular. Quase metade desses elementos foi única para um único tipo celular, destacando o quão especializados são os diferentes tipos de células cerebrais. Muitos elementos regulatórios que mudaram no TUA estavam conectados a genes envolvidos no manejo de cálcio e na sinalização por glutamato, como CALN1, um gene de ligação ao cálcio fortemente ativo em neurônios. Em neurônios inibitórios, CALN1 mostrou tanto aumento de expressão quanto aglomerados densos de laços regulatórios, o que implica que a exposição ao álcool remodela a arquitetura local do DNA que controla esse gene. 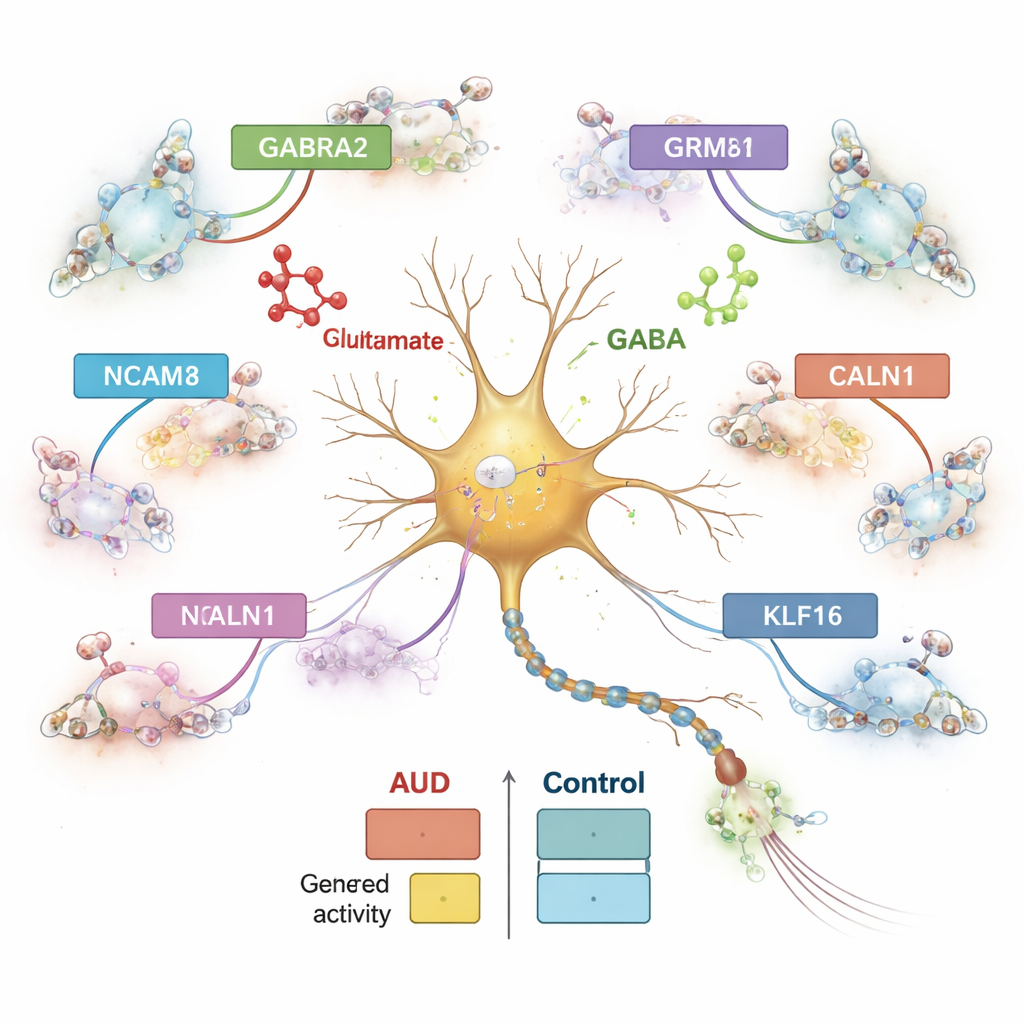
De genes de risco a mudanças reais no cérebro
Estudos genéticos identificaram muitas variantes de DNA que aumentam o risco de desenvolver problemas com álcool, mas onde e como elas atuam no cérebro era incerto. Ao sobrepor seus mapas de célula única com grandes estudos de associação genômica ampla (GWAS) de uso problemático de álcool, os autores descobriram que os genes de risco são desproporcionalmente ativos e desregulados em neurônios da amígdala central, especialmente nos inibitórios. Eles apontaram mais de 200 variantes de risco provavelmente causais localizadas dentro de elementos regulatórios abertos em tipos celulares específicos. Algumas caíram em ou perto de genes já associados à dependência, como CACNA1C e DRD2, que ajudam a controlar a excitabilidade neuronal e a sinalização por dopamina. Outras, incluindo SEMA6D e NF1, emergiram como novos candidatos. A equipe também identificou uma família de fatores de transcrição chamados fatores Kruppel-like (notavelmente KLF16) que parecem coordenar mudanças de amplo alcance em genes relacionados ao cálcio e ao glutamato, e confirmou partes dessa rede regulatória em um modelo de camundongo de exposição aguda ao álcool.
O que isso significa para entender e tratar o TUA
Em termos simples, este estudo mostra que o transtorno por uso de álcool não é apenas um problema cerebral difuso, mas uma perturbação altamente organizada concentrada em tipos celulares e vias moleculares específicas dentro de um núcleo emocional crítico. Neurônios inibitórios da amígdala central, junto com astrócitos e outras células de suporte, exibem mudanças coordenadas na atividade gênica e nos “interruptores” de DNA que controlam esses genes — especialmente em sistemas que regulam sinais de glutamato, GABA e cálcio. Ao conectar essas mudanças celulares a variantes genéticas de risco, o trabalho oferece um mapa que liga a vulnerabilidade herdada a eventos moleculares concretos no cérebro. Com o tempo, tais mapas específicos por célula podem orientar o desenvolvimento de tratamentos mais precisos que restaurem o equilíbrio entre excitação e inibição, em vez de agir de forma ampla sobre todo o cérebro.
Citação: Lee, C.Y., Hwang, A., McRiley, D. et al. Central amygdala single-nucleus atlas reveals chromatin and gene transcription dynamics in human alcohol use disorder. Nat Commun 17, 1634 (2026). https://doi.org/10.1038/s41467-026-68351-1
Palavras-chave: transtorno por uso de álcool, amígdala central, genômica de célula única, neurônios inibitórios, regulação gênica