Clear Sky Science · pt
Da formação do complexo TDP-43/RNA à agregação patogênica de TDP-43 via abordagem estrutural e celular
Por que esta proteína cerebral importa
Doenças neurodegenerativas como a esclerose lateral amiotrófica (ELA) e a demência frontotemporal frequentemente apresentam aglomerados de proteínas mal dobradas dentro dos neurônios. Um dos culpados mais comuns é uma proteína chamada TDP-43, que normalmente ajuda a processar o RNA — a cópia funcional de nossos genes. Este estudo investiga uma questão crucial: o que o TDP-43 faz em células saudáveis e o que dá errado para que um protetor do RNA se transforme em uma proteína tóxica que forma agregados?
Como o TDP-43 funciona em neurônios saudáveis
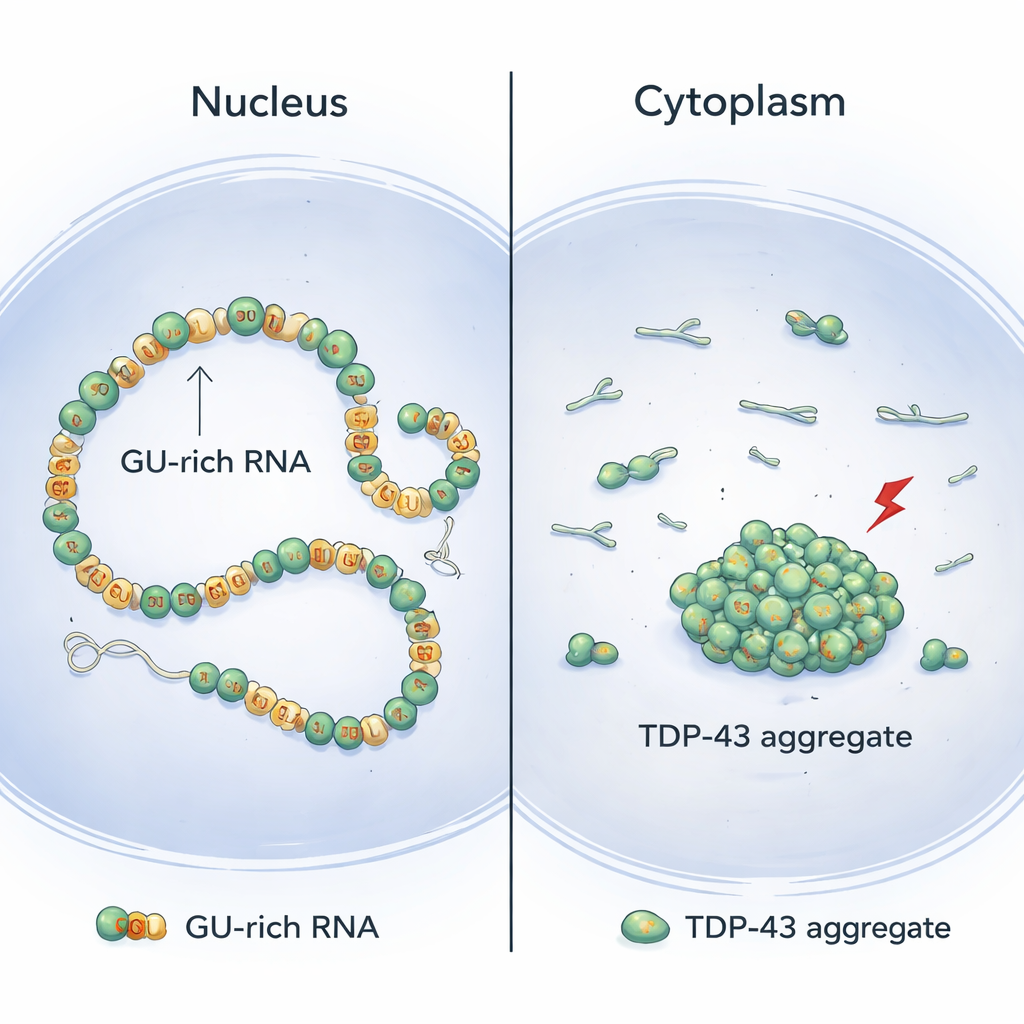
O TDP-43 geralmente reside no núcleo da célula, onde se liga a longos trechos de RNA ricos em repetições de blocos “GU”. Usando uma combinação de biologia estrutural e experimentos celulares, os autores mostram que moléculas de TDP-43 se alinham de forma cooperativa ao longo dessas regiões ricas em GU, formando cadeias suaves e contínuas sobre o RNA. Quando organizadas assim, a extremidade anterior da proteína — seu domínio N-terminal — fica fisicamente separada entre moléculas vizinhas. Como resultado, esses segmentos N-terminais permanecem disponíveis para alcançar e conectar seções distantes ricas em GU do mesmo RNA, formando laços e compactando longos íntrons (os trechos não codificantes dentro dos genes) sem aglomerar.
Uma disputa interna incorporada na proteína
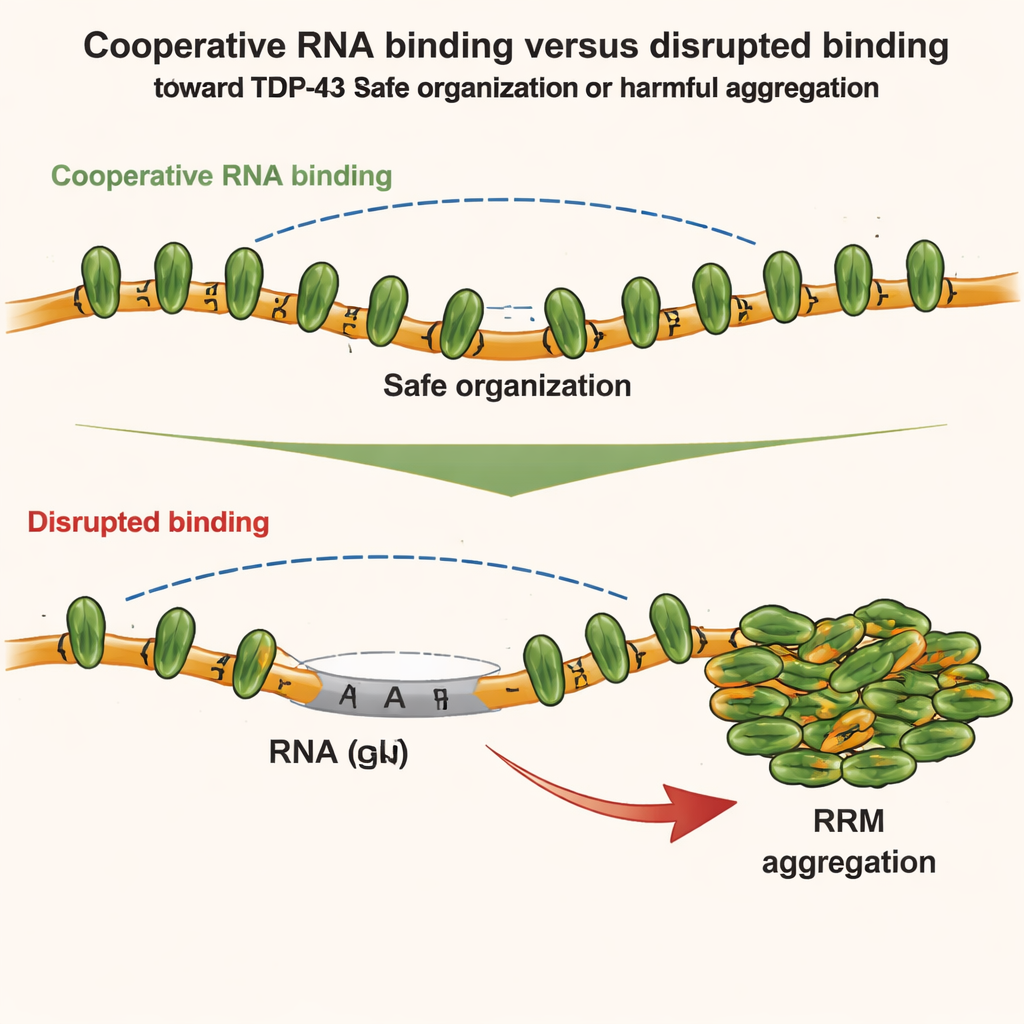
A equipe então explorou como diferentes partes do TDP-43 competem ou cooperam entre si. Eles se concentraram em duas regiões: o domínio N-terminal, que pode aderir a outros domínios N-terminais, e os módulos centrais de ligação ao RNA, que promovem a ligação cooperativa ao longo do RNA rico em GU. Usando técnicas sensíveis, como espectroscopia de RMN, calorimetria e espalhamento de raios X a pequeno ângulo, descobriram que quando o TDP-43 se liga ao RNA de forma cooperativa, a geometria da cadeia enfraquece na prática os contatos diretos N-terminal–N-terminal entre moléculas adjacentes. Em outras palavras, a forte ligação cooperativa ao RNA mantém as interações N-terminais locais sob controle. Mas quando essa cooperatividade é quebrada — por exemplo, ao inserir trechos não-GU no RNA ou ao mutar o TDP-43 — as regiões N-terminais de proteínas vizinhas aproximam-se e podem agora se ligar umas às outras.
Da compactação útil ao aglomerado prejudicial
Essas percepções estruturais foram testadas em células vivas. Os autores usaram sistemas celulares engenheirados para rastrear como diferentes mutantes de TDP-43 se misturam ou se separam dentro de compartimentos artificiais ricos em RNA. Eles descobriram que tanto a ligação cooperativa ao RNA quanto as interações N-terminais ajudam a organizar o TDP-43 em montagens de ordem superior, mas de maneiras distintas. A ligação cooperativa estende as proteínas ao longo do RNA rico em GU, enquanto os contatos N-terminais conectam agrupamentos distantes. Sob estresse oxidativo leve, entretanto, o quadro muda. Um agente químico estressor (arsênito) provoca modificações químicas específicas — acetilação — nos motivos centrais de ligação ao RNA, tornando-os propensos a se aglutinarem. Se a ligação cooperativa ao RNA estiver intacta, o TDP-43 permanece majoritariamente solúvel. Se a cooperatividade for enfraquecida, os elos N-terminais entre moléculas de TDP-43 próximas atuam como uma estrutura que aproxima os núcleos acetilados, favorecendo a agregação irreversível.
Por que o TDP-43 forma mais aglomerados no citoplasma
O modelo emergente deste trabalho ajuda a explicar por que os agregados de TDP-43 são frequentemente encontrados no citoplasma de neurônios doentes em vez do núcleo. No núcleo, longos íntrons com muitas repetições GU são comuns, favorecendo uma ligação contínua e cooperativa que mantém baixos os contatos N-terminais arriscados entre vizinhos e permite, em vez disso, o laço seguro em longa distância. No citoplasma, em contraste, os RNAs maduros têm muito menos trechos ricos em GU. Isso torna a ligação do TDP-43 mais descontínua e menos cooperativa, aumentando as chances de que domínios N-terminais vizinhos interajam e preparem o terreno para agregação quando ocorrerem alterações químicas induzidas por estresse. Em apoio a essa visão, fornecer artificialmente íntrons extras ricos em GU no núcleo reduziu a agregação de TDP-43 sob estresse.
O que isso significa para terapias futuras
Em poucas palavras, o estudo retrata o TDP-43 como uma proteína em equilíbrio entre a organização útil do RNA e o aglomerado prejudicial, com a ligação cooperativa ao RNA rico em GU funcionando como um mecanismo de segurança. Quando essa rede de proteção falha — por causa de sequências de RNA alteradas, mutações na proteína ou estresse celular — os mesmos domínios que normalmente compactam longos segmentos de RNA podem, em vez disso, promover a formação de agregados tóxicos. Para não especialistas, a conclusão principal é que manter o tipo certo de interações entre TDP-43 e RNA pode ser uma estratégia promissora para prevenir ou retardar o aglomeramento proteico observado na ELA e em doenças cerebrais relacionadas.
Citação: Feng, Y., Joshi, V., Pankivskyi, S. et al. From TDP-43/RNA complex formation to disease-linked TDP-43 aggregation through a structural and cellular approach. Nat Commun 17, 1631 (2026). https://doi.org/10.1038/s41467-026-68346-y
Palavras-chave: agregação de TDP-43, proteínas de ligação ao RNA, ELA, interações proteína–RNA, neurodegeneração