Clear Sky Science · pt
Engenharia de ligantes com precisão atômica em nanopartículas de ouro via transferência de massa em interfase
Por que partículas de ouro minúsculas importam para a saúde
A imagem médica depende cada vez mais de nanopartículas — partículas minúsculas milhares de vezes menores que um fio de cabelo — para iluminar órgãos e tumores profundos no corpo. Este estudo mostra como cientistas podem agora ajustar a camada externa de partículas de ouro ultrapequenas quase átomo por átomo, de modo que o mesmo núcleo emissor possa ser direcionado a diferentes órgãos, especialmente deslocando-se do fígado e do baço para os rins. Esse controle pode ajudar a projetar agentes de imagem e vetores de fármaco mais seguros que cheguem exatamente onde os médicos desejam e sejam eliminados do corpo de forma mais limpa.
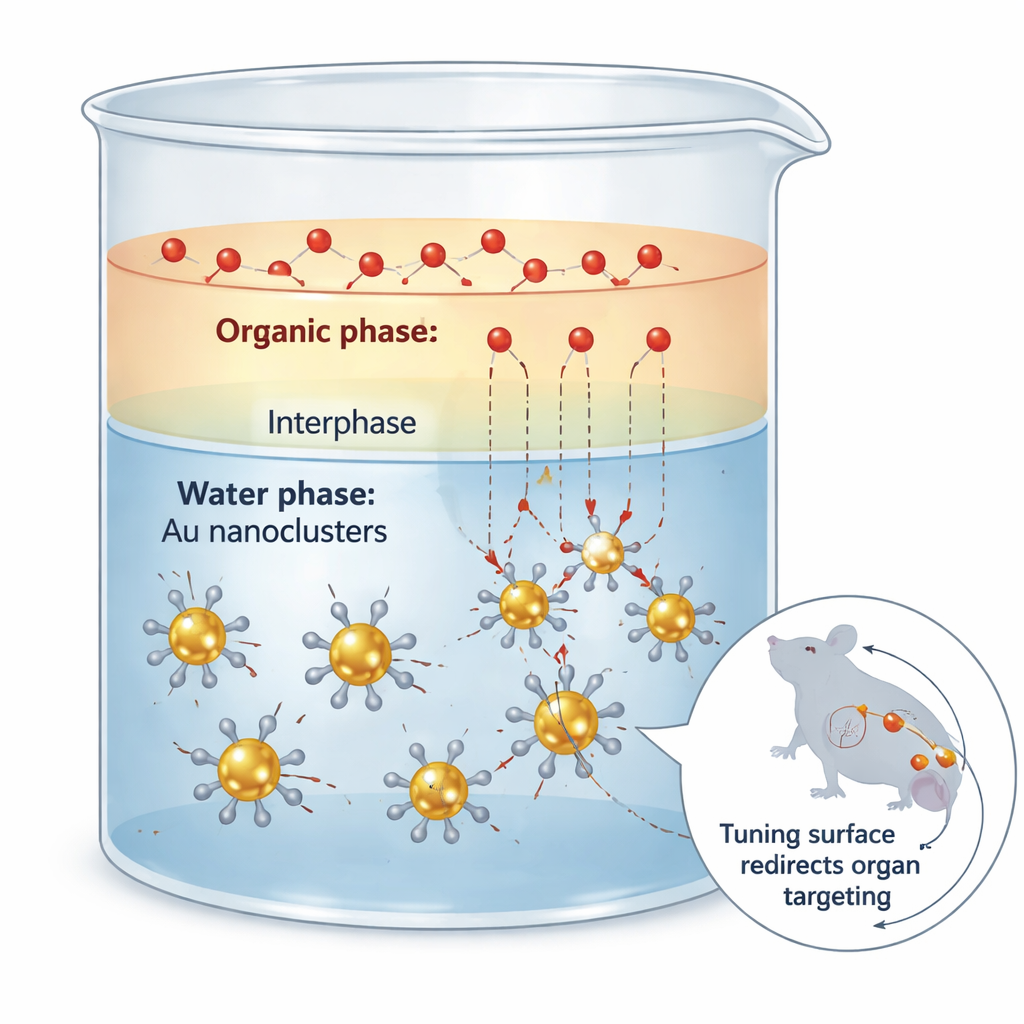
O desafio de “vestir” nanoclusters de ouro
Nanoclusters de ouro são partículas ultrapequenas que se comportam mais como grandes moléculas do que como grãos metálicos. Eles podem emitir luz na janela do infravermelho próximo II, que penetra profundamente no tecido e fornece imagens nítidas com baixo ruído de fundo. No entanto, quase tudo sobre como esses clusters se comportam no organismo — para onde viajam, por quanto tempo circulam e como são eliminados — depende não do ouro em si, mas dos ligantes orgânicos, ou moléculas da "casca", presas à sua superfície. Métodos tradicionais para mudar essa casca costumam agir como cirurgia grosseira: a reação é rápida demais, o revestimento fica irregular e o núcleo de ouro pode ser parcialmente corroído, arruinando tanto a estrutura quanto as propriedades ópticas.
Desacelerando o trânsito entre dois líquidos
Os pesquisadores abordaram esse problema explorando uma ideia física simples: resistência à transferência de massa na fronteira entre dois líquidos que não se misturam totalmente. Eles colocaram os clusters de ouro na água e os ligantes entrantes à base de enxofre em um solvente orgânico como acetato de etila. Na região fina onde os dois líquidos se misturam parcialmente, os ligantes difundem-se lentamente em direção aos clusters e trocam-se com a casca original. Medições cinéticas cuidadosas mostraram que a indesejada "etching" (corrosão) do núcleo de ouro é extremamente sensível à concentração de ligante livre, enquanto a troca desejada é muito menos sensível. Usando a configuração biphasica para manter baixos níveis de ligante livre, mas continuamente reabastecidos, a equipe suprimiu a corrosão em cerca de sessenta vezes, preservando ao mesmo tempo a maior parte da taxa útil de troca.
Construindo um conjunto molecular preciso
Com esse método assistido por interfase, os autores puderam substituir ligantes superficiais em um cluster de ouro modelo, Au25, de forma altamente controlada. Partiram de clusters protegidos por um ligante ácido sulfônico carregado negativamente e trocaram por uma variedade de novos tiol-ligantes contendo ácidos carboxílicos, aminas, hidroxilas, grupos nitro e anéis aromáticos hidrofóbicos. Espectrometria de massa revelou misturas limpas e bem definidas, como clusters Au25 com números específicos de cada tipo de ligante, em vez de distribuições largas e confusas. O método também funcionou para outros tamanhos de cluster e famílias de ligantes, sugerindo que é uma estratégia geral para fabricar nanoclusters de ouro robustos e sob medida para diferentes aplicações.
Guiando nanopartículas do fígado para os rins
O teste mais marcante dessa precisão veio de experimentos de imagem in vivo em camundongos. Ao introduzir gradualmente um ligante carregado positivamente, p-aminotiophenol, na casca originalmente carregada negativamente, a equipe criou uma série de clusters cuja carga superficial geral passou de fortemente negativa para quase zwitteriônica (grupos positivos e negativos equilibrados). Todas as versões brilhavam de forma semelhante em testes de laboratório, mas sua biodistribuição em camundongos diferiu dramaticamente. Clusters puramente negativos acumulavam-se principalmente no fígado e no baço. À medida que mais ligantes positivos eram adicionados, havia menos sinal nesses órgãos e mais nos rins e na bexiga, indicando maior eliminação renal. Quando um ligante neutro com grupo hidroxila foi usado em vez da amina, essa mudança não ocorreu, ressaltando o papel especial das cargas positivas em redirecionar as partículas.
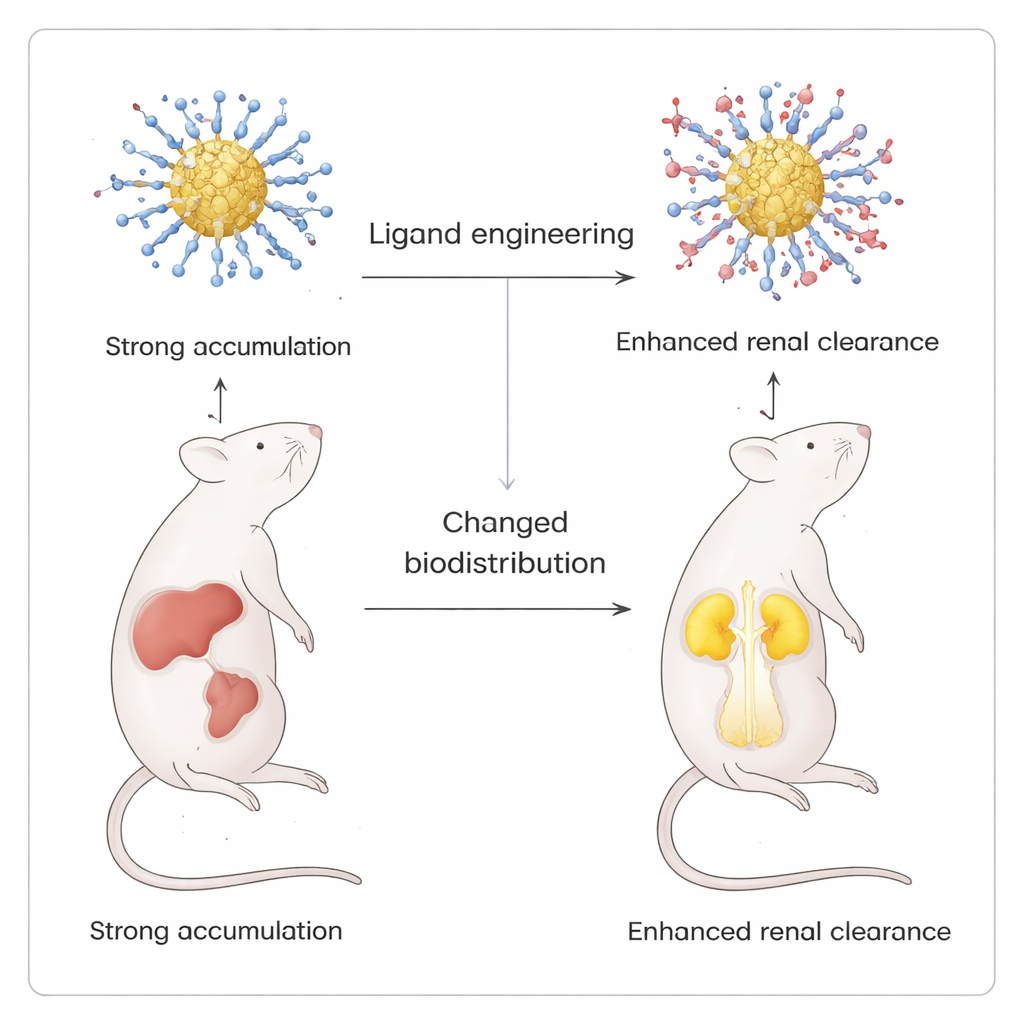
O que isso significa para medicamentos futuros
Para não especialistas, a ideia principal é que os cientistas encontraram uma maneira de "vestir" nanoclusters de ouro emissores com revestimentos moleculares que podem ser ajustados quase uma molécula por vez, sem danificar a partícula subjacente. Usando uma montagem suave de dois líquidos, eles podem controlar tanto a química quanto o destino final dessas partículas dentro do corpo. Esse nível de controle torna possível projetar agentes de imagem e potenciais vetores de fármacos que iluminem órgãos específicos e em seguida sejam eliminados pelos rins, em vez de permanecerem no fígado e no baço, abrindo caminho para uma nanomedicina mais segura e previsível.
Citação: Zhang, B., Xiao, F., Song, X. et al. Atomically precise ligand engineering of gold nanoparticles via interphase mass transfer. Nat Commun 17, 1630 (2026). https://doi.org/10.1038/s41467-026-68345-z
Palavras-chave: nanoclusters de ouro, engenharia de ligantes, bioimagem, nanomedicina, biodistribuição