Clear Sky Science · pt
A atividade de DOT1L limita a velocidade de alongamento da transcrição e favorece a pausa da RNAPII para facilitar a mutagênese pela AID
Como nossas células imunes ajustam edições arriscadas no DNA
O nosso sistema imunológico gera anticorpos potentes ao deliberadamente mutar seu próprio DNA, uma estratégia arriscada que às vezes pode favorecer o câncer. Este estudo investiga uma questão aparentemente simples, mas de grande implicação: o que controla onde e com que eficiência essas mutações intencionais ocorrem? A resposta gira em torno de uma proteína chamada DOT1L, que ajusta a velocidade de leitura dos genes nas células B e, fazendo isso, ajuda a direcionar a maquinaria de mutação para os locais corretos.
Ligando a mutação para aprimorar anticorpos
Quando as células B encontram uma infecção, elas aprimoram seus anticorpos de duas maneiras. Introduzem pequenas mudanças na região de ligação do anticorpo para melhorar a afinidade pelos germes e trocam a cauda do anticorpo para alterar a forma como o sistema imune responde. Ambas as melhorias começam com uma enzima chamada AID, que faz cortes e altera o DNA em genes que estão sendo ativamente lidos. Embora a AID seja crucial para a boa imunidade, ela também pode atingir outros genes, criando quebras perigosas que impulsionam cânceres hematológicos. Trabalhos anteriores mostraram que a AID prefere genes muito transcritos e regulados por potentes interruptores de DNA chamados superenhancers, mas isso não explicava totalmente por que apenas um subconjunto específico de genes é realmente vulnerável.
Um marcador de cromatina que sinaliza genes sensíveis à AID
Os autores focaram em proteínas que se situam próximas à AID no núcleo. Usando uma técnica de rotulagem por proximidade em células humanas, eles descobriram que a AID se agrupa perto da DOT1L, uma enzima que marca um ponto específico nas histonas ao redor do DNA. Essa marcação, uma modificação química na histona H3 na posição K79, é comum em genes ativos. Em células B de camundongo, genes frequentemente mutados pela AID — incluindo genes de anticorpos e alvos fora do alvo ligados ao câncer — apresentam níveis particularmente altos dessas marcas feitas pela DOT1L. Quando os pesquisadores desativaram a DOT1L em linhagens de células B ou bloquearam sua atividade com um fármaco, a troca de classe dos anticorpos diminuiu, assim como as quebras de DNA induzidas pela AID e as fusões propensas ao câncer entre genes de anticorpos e o gene de crescimento cMyc. Importante: a função catalítica da DOT1L, e não apenas sua presença, era necessária: versões mutantes incapazes de colocar a marca na histona não conseguiram restaurar a troca normal de classe dos anticorpos.
Desacelerando o leitor de genes para dar tempo à AID
À primeira vista, isso é intrigante porque a DOT1L está associada a genes ativos, e, ainda assim, removê‑la não desligou simplesmente esses genes. Usando um método que captura o RNA recém-sintetizado, a equipe descobriu que células B sem DOT1L, na verdade, produziram mais transcritos nascentes em muitos genes marcados pela DOT1L — embora houvesse um pouco menos da principal enzima de leitura de genes, a RNA polimerase II, posicionada nesses genes. Ao combinar essa medida de RNA nascente com mapas de ocupação da polimerase, os autores inferiram que, em condições normais, as marcas de histona da DOT1L atuam como pequenos lombos de desaceleração. Elas retardam a polimerase enquanto esta se move ao longo do gene e estendem pausas curtas perto do início e no corpo de genes marcados pela DOT1L. Sem a DOT1L, a polimerase corre mais rápido e pausa por períodos mais curtos. Como a AID precisa de janelas breves em que o DNA fica exposto e a polimerase demora, essa aceleração paradoxalmente reduz a capacidade da AID de se prender e executar sua função, mesmo que a transcrição total aumente.
Desacoplando atividade gênica do risco de mutação
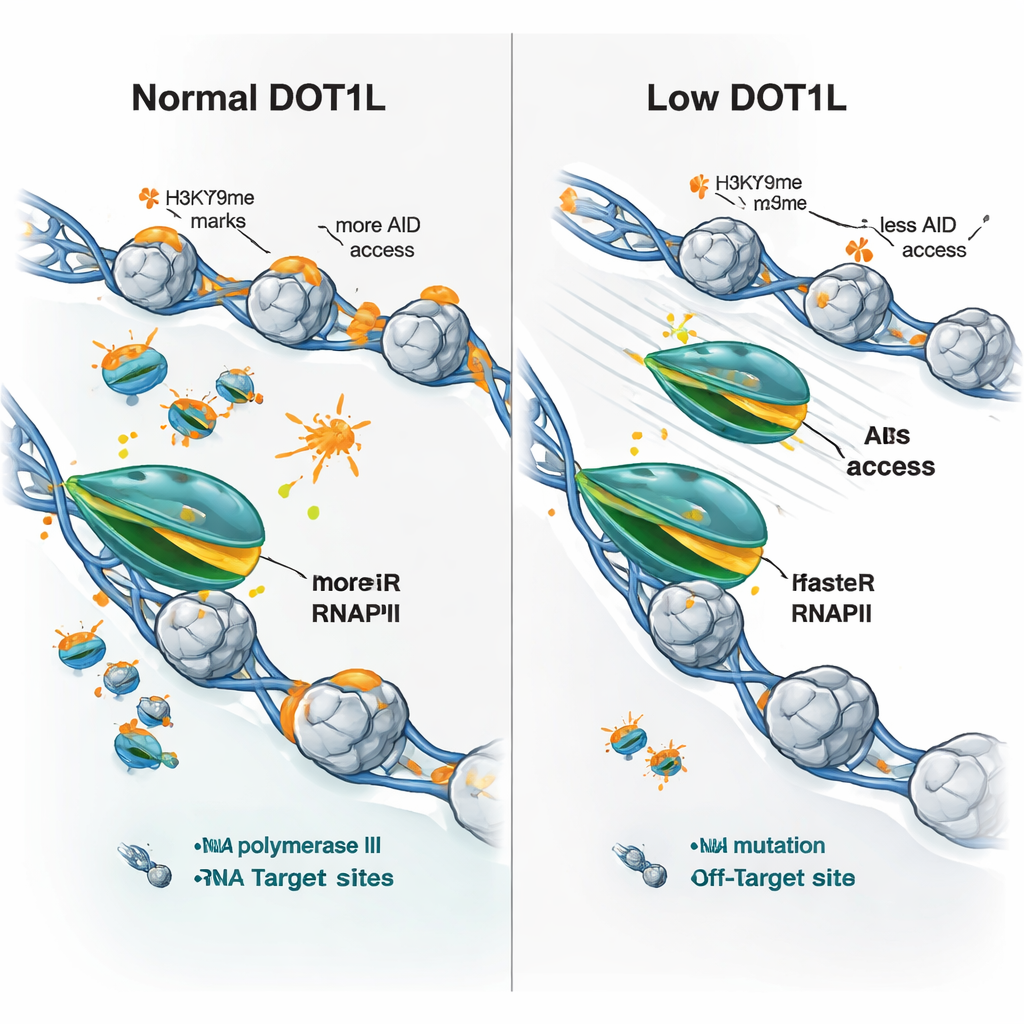
Os pesquisadores então questionaram se essas mudanças na velocidade poderiam explicar o padrão misto de expressão gênica observado quando a DOT1L é perdida — alguns genes aumentam, outros diminuem. Eles descobriram que virtualmente todos os genes marcados pela DOT1L compartilhavam uma característica nas células knockout: elongação mais rápida pela RNA polimerase II. Mas o resultado dependia do estado inicial. Genes lentos e fracamente expressos tenderam a produzir mais RNA quando a polimerase acelerou, enquanto genes longos e altamente ativos com polimerases já rápidas às vezes produziram menos, provavelmente porque a passagem excessivamente rápida prejudica o processamento ou a conclusão eficientes. Crucialmente, tanto em genes de anticorpos quanto em alvos clássicos fora do alvo da AID, a perda de DOT1L levou a um movimento mais rápido da polimerase, menos evidência de “engasgos” da polimerase e redução significativa da ocupação da AID, mesmo quando os próprios genes não foram desativados.
Por que isso importa para imunidade e câncer
Em conjunto, o trabalho descreve a DOT1L como um controlador de tráfego sutil para a maquinaria que lê genes em células B. Ao instalar marcas específicas nas histonas, a DOT1L desacelera ligeiramente a RNA polimerase II e prolonga suas pausas, criando um ambiente transcricional onde a AID pode se engajar produtivamente nos genes de anticorpos — e, infelizmente, em um conjunto limitado de outros genes vulneráveis — para introduzir mutações. Quando a DOT1L está ausente ou inibida, a polimerase atravessa os genes mais rapidamente, deixando a AID com menos oportunidades de agir, o que enfraquece a diversificação de anticorpos e simultaneamente reduz o risco de certas rearranjos prejudiciais. Essa visão mecanística explica por que a perda de DOT1L pode tanto aumentar quanto diminuir a expressão gênica e conecta o controle fino da velocidade da transcrição diretamente aonde nosso sistema imune ousa reescrever seu próprio DNA.
Citação: Subramani, P.G., Seija, N., Ridani, J. et al. DOT1L activity limits transcription elongation velocity and favors RNAPII pausing to facilitate mutagenesis by AID. Nat Commun 17, 1623 (2026). https://doi.org/10.1038/s41467-026-68332-4
Palavras-chave: diversificação de anticorpos, enzima AID, DOT1L, transcrição gênica, células B