Clear Sky Science · pt
Projeto computacional de ciclopropanases generalistas com seletividade estereodivergente
Por que estruturas pequenas de três anéis importam para medicamentos
Ciclopropanos — anéis de carbono de três membros — são blocos construtores diminutos e tensionados que podem alterar dramaticamente como um fármaco se comporta no organismo. O arranjo 3D exato dos átomos (sua estereoquímica) pode determinar se uma molécula se torna um medicamento útil ou um análogo inativo ou até prejudicial. Este artigo descreve uma estratégia computacional para projetar enzimas capazes de produzir de forma confiável todas as quatro formas 3D possíveis desses anéis a partir dos mesmos materiais de partida, abrindo caminho para uma exploração mais rápida e limpa de candidatos a fármacos.
De uma receita para quatro resultados diferentes
Quando uma dupla ligação simples (um olefina) reage com um doador de carbeno como um composto diazo, o resultado pode ser um anel de ciclopropano. Mas esse anel pode adotar quatro formas estereoisoméricas distintas, cada uma com os mesmos átomos, porém dispostos de maneira diferente no espaço. Os químicos querem acesso a cada uma dessas formas porque elas podem interagir de modo muito distinto com alvos biológicos e influenciar propriedades chave do fármaco, como absorção, metabolismo e segurança. Catalisadores de pequenas moléculas tradicionais às vezes conseguem esse controle, mas fazê‑lo com enzimas — os catalisadores da natureza — tem sido difícil, especialmente quando se busca alta seletividade e tolerância a muitos substratos diferentes.
Projetando enzimas na tela do computador
Os autores desenvolveram um fluxo de trabalho computacional multiestado baseado no mecanismo para resolver esse problema. Primeiro, usaram cálculos quânticos para modelar os fugazes estados de transição — as estruturas de alta energia ao longo do caminho reacional — para a formação de cada um dos quatro estereoisômeros de ciclopropano. Esses modelos foram então colocados nos sítios ativos de diferentes proteínas contendo heme, e o software de projeto de proteínas Rosetta foi usado para avaliar quão bem cada proteína estabilizava ou desestabilizava cada estado de transição. Crucialmente, a pontuação de projeto recompensava mutações que favoreciam o estado de transição desejado (projeto positivo) e desfavoreciam os concorrentes (projeto negativo), ensinando efetivamente a enzima a “preferir” um produto 3D em relação aos outros.
Construindo uma caixa de ferramentas completa de enzimas
Usando essa abordagem, a equipe criou uma família de enzimas ciclopropanases “generalistas”. A partir da mioglobina, redesenharam seu sítio ativo para obter variantes que produzem o trans-(1R,2R) ciclopropano com seletividade muito alta e boa atividade em mais de 20 olefinas diferentes, incluindo substratos desafiadores não ativados e pobres em elétrons. Uma mioglobina previamente projetada já fornecia o produto complementar trans-(1S,2S). Para alcançar os dois produtos cis, os autores recorreram a outras proteínas heme. Remodelaram a enzima bacteriana P450cam para obter variantes que dão seletivamente o produto cis-(1S,2R), e reaproveitaram a indolamina 2,3‑dioxygenase‑1 humana (IDO1) — não utilizada antes para química de carbeno — para favorecer o produto cis-(1R,2S). No total, esses quatro biocatalisadores podem fornecer todos os estereoisômeros do mesmo conjunto de produtos de ciclopropano, frequentemente com até 99% de controle tanto da diastereomeria quanto da enantiomeria.
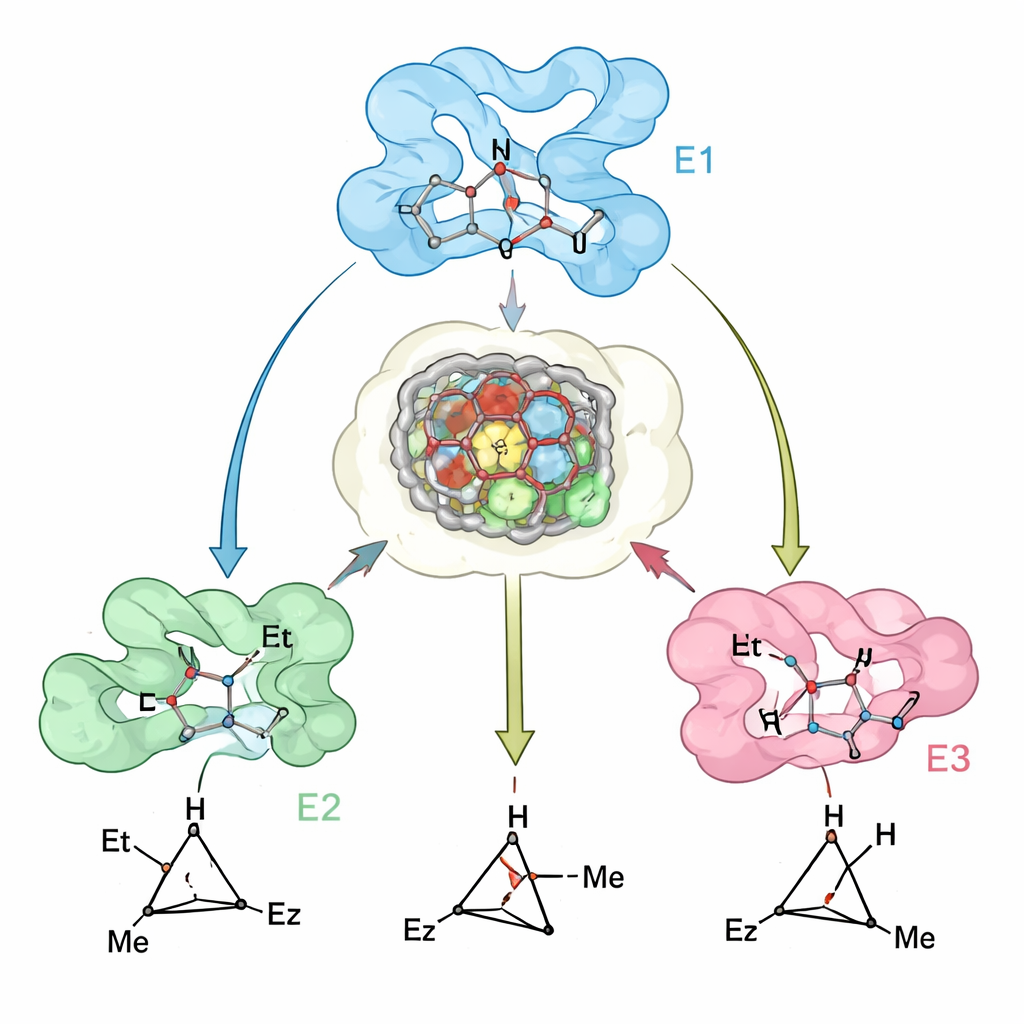
Vendo como o projeto corresponde à realidade
Para testar quão bem seus modelos computacionais refletiam enzimas reais, os pesquisadores resolveram estruturas cristalinas de uma variante chave de mioglobina e as compararam com as estruturas previstas. O acordo foi próximo, e os dados experimentais destacaram uma característica sutil, mas importante: o sítio ativo da proteína está pré‑organizado para acolher o estado de transição preferido, enquanto pequenos deslocamentos em alças e hélices próximas tornam energeticamente desfavorável a ligação do estado de transição “errado”. Onde as previsões foram menos precisas — como para alguns substratos volumosos — as discrepâncias puderam ser rastreadas a movimentos da espinha dorsal que não foram totalmente capturados na modelagem, sugerindo caminhos claros para melhorar métodos de projeto futuros.
O que isso significa para futuros medicamentos e catalisadores
Ao combinar modelagem de estados de transição baseada em física com redesenho inteligente de proteínas, este trabalho demonstra que os resultados estereoquímicos de reações catalisadas por enzimas podem ser programados de antemão, em vez de descobertos apenas por evolução via tentativa e erro. O conjunto resultante de ciclopropanases oferece aos químicos uma maneira prática de sintetizar conjuntos completos de estereoisômeros de ciclopropano a partir de uma ampla gama de olefinas de partida, simplificando muito os estudos de relação estrutura–atividade na descoberta de fármacos e na síntese de produtos naturais. A mesma estratégia deve ser adaptável a outros tipos de enzimas e classes de reação, acelerando a criação de biocatalisadores que proporcionem controle 3D preciso sobre moléculas complexas.
Citação: Shen, Z., Siriboe, M.G., Ren, X. et al. Computational design of generalist cyclopropanases with stereodivergent selectivity. Nat Commun 17, 1620 (2026). https://doi.org/10.1038/s41467-026-68327-1
Palavras-chave: biocatálise, ciclopropanação, projeto de enzimas, estereoquímica, proteínas heme