Clear Sky Science · pt
A glicerol-3-fosfato aciltransferase agrava a toxicidade induzida pela α-sinucleína ao aumentar a peroxidação lipídica
Por que as gorduras no cérebro importam para o Parkinson
A doença de Parkinson costuma ser descrita como um problema envolvendo uma proteína chamada alfa‑sinucleína que se aglomera e prejudica as células cerebrais que controlam o movimento. Este estudo mostra que as gorduras do cérebro — em especial a forma como são sintetizadas e danificadas — desempenham um papel surpreendentemente poderoso na toxicidade da alfa‑sinucleína. Ao identificar uma enzima de síntese lipídica que piora a lesão neuronal, o trabalho aponta para uma via nova e farmacologicamente acessível que pode complementar esforços existentes para combater o Parkinson em sua raiz.
Uma proteína que se comporta mal no Parkinson
Pessoas com Parkinson perdem progressivamente neurônios produtores de dopamina em uma região profunda do cérebro que coordena o movimento. Dentro dessas células moribundas, os cientistas frequentemente encontram depósitos densos chamados corpos de Lewy, repletos da proteína alfa‑sinucleína. Em famílias raras, mutações ou cópias extras do gene da alfa‑sinucleína causam diretamente Parkinson, mas variantes genéticas comuns nesse gene aumentam o risco apenas modestamente. Isso sugere que outros genes e vias modulam o grau de dano causado pela alfa‑sinucleína. Cada vez mais, as evidências apontam para os lipídios — gorduras e moléculas semelhantes a gorduras que formam membranas e reservatórios energéticos — como parceiros-chave tanto na aglomeração da alfa‑sinucleína quanto na morte neuronal.
Encontrando uma enzima lipídica poderosa em modelos de mosca-das-frutas
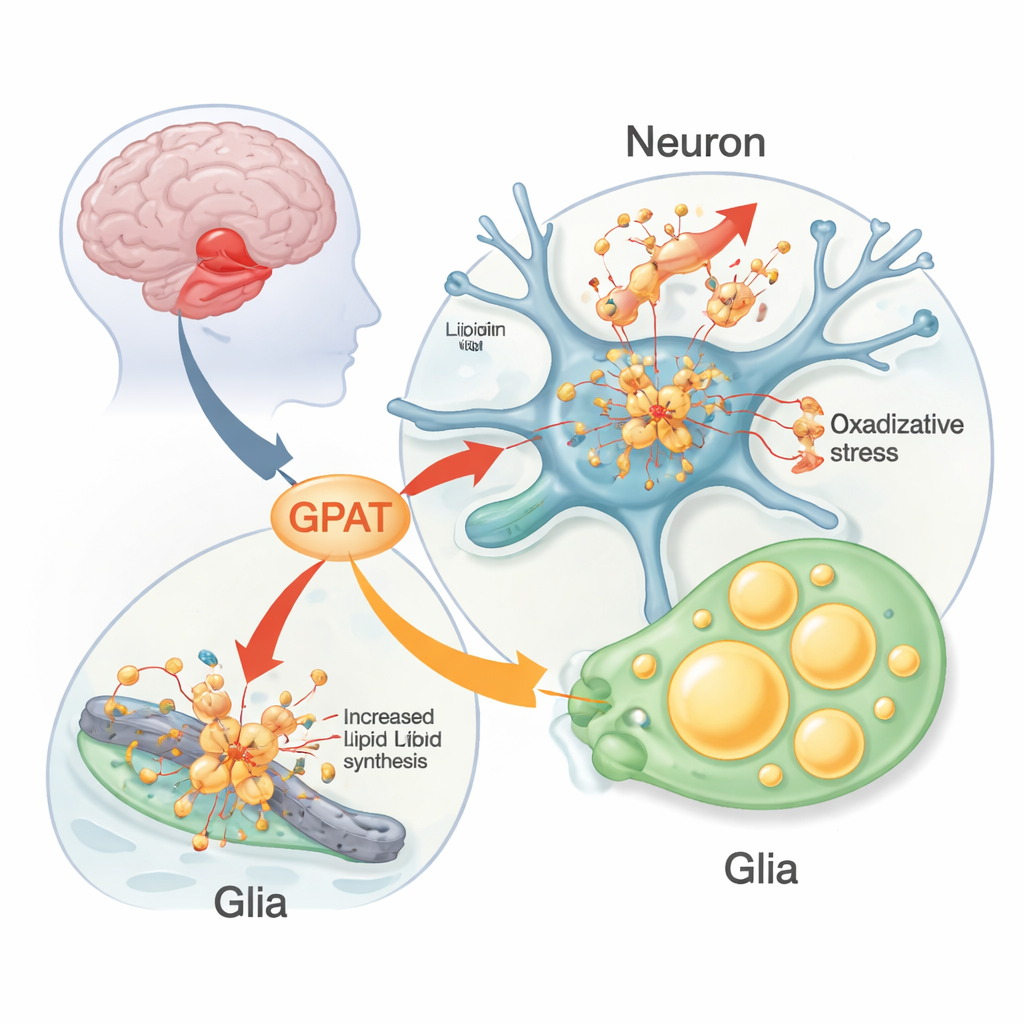
Os pesquisadores usaram moscas-das-frutas geneticamente modificadas para expressar alfa‑sinucleína humana em seu sistema nervoso como um ensaio vivo. Essas moscas desenvolvem problemas semelhantes ao Parkinson: perda de neurônios produtores de dopamina, dificuldade para escalar e ritmos de atividade diária perturbados. A equipe alterou sistematicamente versões de mosca de genes de risco humanos para Parkinson para ver quais mudavam o impacto da alfa‑sinucleína. Um gene sobressaiu: mino, que codifica uma forma mitocondrial da enzima glicerol-3‑fosfato aciltransferase (GPAT). A GPAT atua no ponto de entrada da síntese de fosfolipídios e triglicerídeos — os lipídios que formam membranas e gotículas de gordura. Quando a equipe reduziu a atividade de mino em neurônios, as moscas com alfa‑sinucleína mantiveram mais neurônios produtores de dopamina e se locomoveram melhor por mais tempo; aumentar a expressão de mino teve o efeito oposto, prejudicial.
Gorduras danificadas, mitocôndrias estressadas e gotículas de gordura em células gliais
Aprofundando-se, os cientistas descobriram que a GPAT influenciava quanto dano oxidativo se acumulava nos lipídios cerebrais. Em moscas com alfa‑sinucleína mantidas em temperatura mais alta (o que agrava as características da doença), a peroxidação lipídica — a “ferrugem” química das gorduras — aumentou nas membranas cerebrais. Reduzir mino diminuiu esse dano, enquanto sua superexpressão o aumentou; na ausência de alfa‑sinucleína, alterar mino teve pouco efeito. Marcadores de morte celular na região visual do cérebro espelharam esse padrão. A equipe também observou um acúmulo marcante de gotículas lipídicas — pequenas esferas de armazenamento de gordura — não nos próprios neurônios, mas nas células gliais vizinhas. Essas gotículas aumentaram com a idade nas moscas com alfa‑sinucleína e foram moduladas por enzimas que sintetizam ou degradam triglicerídeos, destacando uma parceria metabólica ativa entre neurônios e glia sob estresse.
Reconfiguração metabólica e aglomeração da alfa‑sinucleína
Medições de metabólitos em cérebros de mosca revelaram que a expressão de alfa‑sinucleína estava ligada a um estrangulamento no ciclo de produção de energia da célula: citrato e isocitrato, dois intermediários do ciclo do ácido tricarboxílico (TCA), acumularam-se fortemente, enquanto etapas subsequentes mudaram de forma mais modesta. Os níveis de lactato também aumentaram, consistente com uma glicólise intensificada. Ao mesmo tempo, um perfil detalhado de lipídios mostrou mudanças no equilíbrio dos fosfolipídios de membrana e na composição de seus ácidos graxos, favorecendo espécies mais propensas ao dano oxidativo. Quando a equipe reduziu várias enzimas GPAT — mino nas mitocôndrias e enzimas relacionadas no retículo endoplasmático — a alfa‑sinucleína ainda se acumulou, mas sua tendência a formar oligômeros de ordem superior (agregados multiproteicos) diminuiu, e as mitocôndrias exibiram menos sinais de estresse por espécies reativas de oxigênio e de “envelhecimento”.
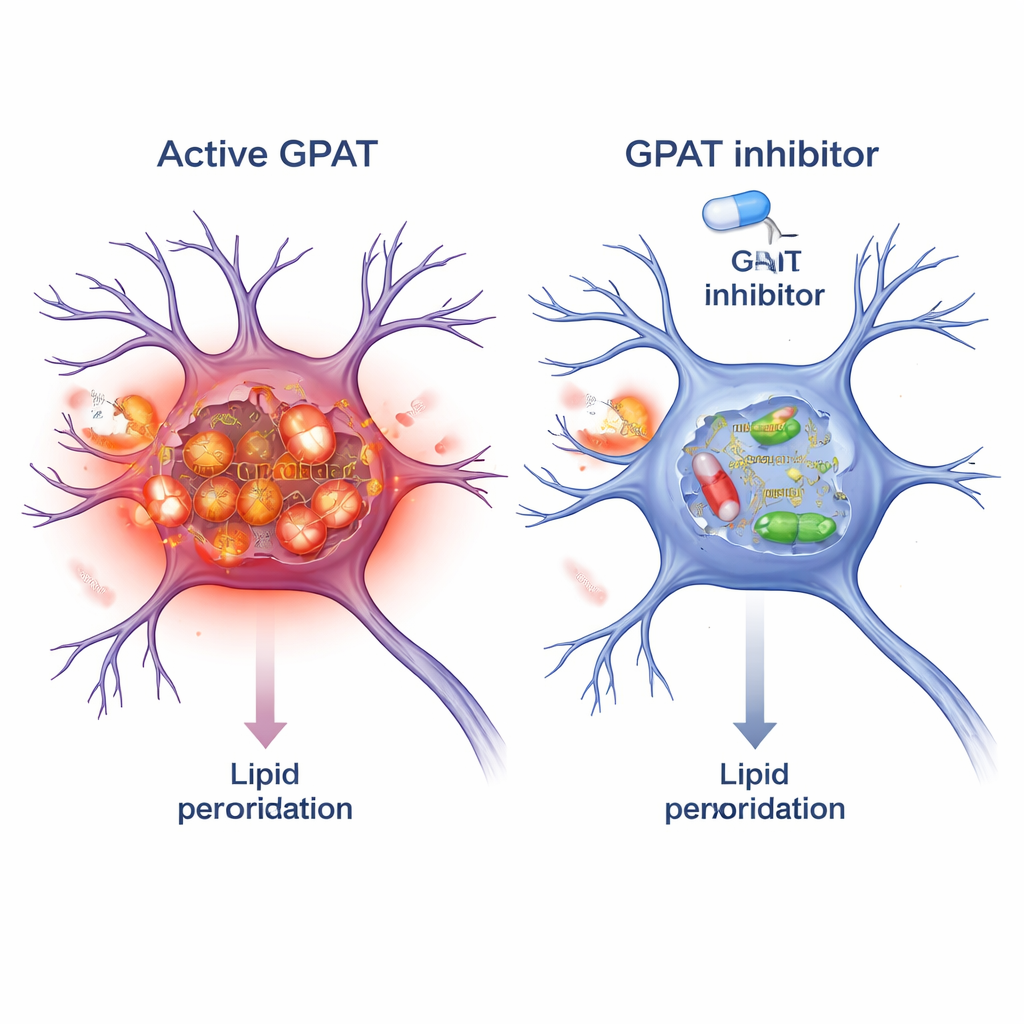
Bloquear a GPAT como estratégia protetora
Como a GPAT é uma enzima, ela pode ser alvo de pequenas moléculas. Os pesquisadores testaram o FSG67, um inibidor de GPAT já desenvolvido para obesidade e diabetes. Em moscas com alfa‑sinucleína, adicionar FSG67 ao alimento reproduziu os benefícios do silenciamento genético da GPAT: melhora na locomoção, maior sobrevivência de neurônios dopaminérgicos, menos oligômeros tóxicos de alfa‑sinucleína e redução do estresse oxidativo mitocondrial. Para verificar se o conceito se estendia a mamíferos, trataram neurônios de cérebro de camundongo em cultura com fibrilas pré-formadas de alfa‑sinucleína, que nucleiam agregados tóxicos. O co-tratamento com FSG67 reduziu o acúmulo de alfa‑sinucleína fosforilada e diminuiu múltiplos marcadores independentes de peroxidação lipídica nessas células neuronais.
O que isso significa para pessoas com Parkinson
Em termos simples, este trabalho mostra que a forma como o cérebro lida com gorduras pode aumentar ou reduzir a toxicidade da alfa‑sinucleína. Quando a GPAT está altamente ativa, lipídios mais vulneráveis são incorporados em membranas e gotas de armazenamento, tornando-os mais suscetíveis à oxidação; esse ambiente lipídico danificado parece favorecer formas nocivas de alfa‑sinucleína e sobrecarregar as mitocôndrias, as usinas de energia da célula. Reduzir a GPAT — seja geneticamente ou com um fármaco — desloca o equilíbrio para menos “ferrugem” lipídica, menos agregados proteicos tóxicos e neurônios mais saudáveis. Embora essas descobertas sejam iniciais e derivem de moscas e de células de camundongo em cultura, elas destacam o metabolismo lipídico, e a GPAT em particular, como um ângulo promissor para terapias do Parkinson que poderiam complementar estratégias que miram diretamente a alfa‑sinucleína.
Citação: Ren, M., Lim, G.G.Y., Tang, W. et al. Glycerol 3-phosphate acyltransferase exacerbates α-synuclein-induced toxicity by increasing lipid peroxidation. Nat Commun 17, 1618 (2026). https://doi.org/10.1038/s41467-026-68325-3
Palavras-chave: Doença de Parkinson, alfa-sinucleína, peroxidação lipídica, inibidor de GPAT, neurodegeneração