Clear Sky Science · pt
Estrutura do complexo SHOC2-KRAS-PP1C revela determinantes específicos de isoformas RAS e oferece insights para direcionar a montagem do complexo por inibidores de RAS
Como as células decidem quando crescer
Nossas células dependem de um sistema de fiação interna para decidir quando crescer, dividir-se ou permanecer inativas. No centro desse sistema estão as proteínas RAS, pequenos interruptores moleculares que frequentemente falham no câncer. Este estudo investiga em profundidade como um grupo particular de proteínas — SHOC2, RAS e PP1C — se unem para acionar um interruptor chave de crescimento, e como os medicamentos modernos contra o câncer podem ser ajustados para bloquear esse processo de modo mais eficaz e evitar que os tumores contornem o tratamento.
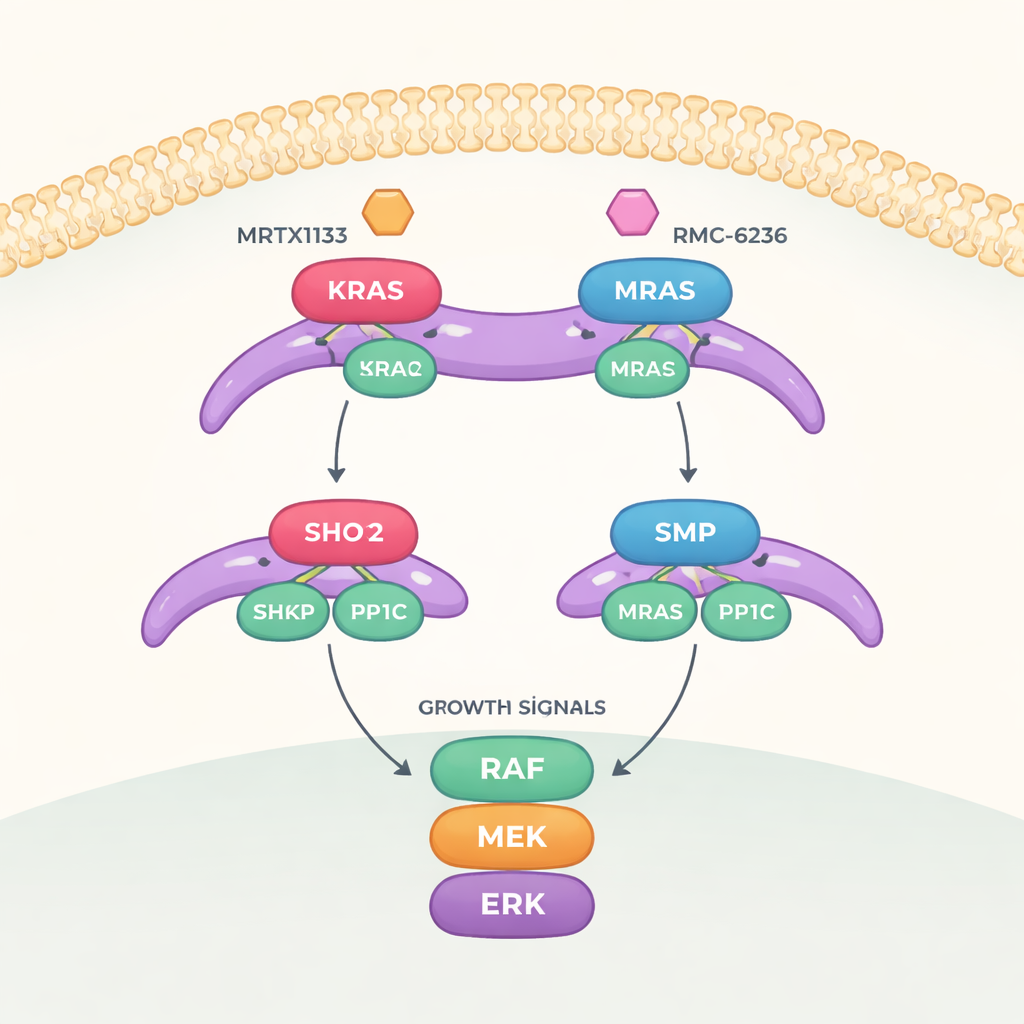
Um interruptor de crescimento com três partes críticas
O trabalho concentra-se em uma via de sinalização chamada via MAPK, que transmite mensagens de crescimento da superfície celular até o núcleo. Para ativar totalmente essa via, outra proteína chamada RAF precisa ser mudada de um estado “desligado” para um estado “ligado”. Esse comutador é controlado por um complexo tripartido formado por SHOC2 (um andaime que mantém as peças juntas), PP1C (uma enzima que remove uma marca de fosfato) e uma proteína RAS ativa. Quando montado, esse trio remove uma marca de fosfato específica da RAF, permitindo que ela ative a cascata de crescimento a jusante.
Por que um parceiro de afinidade mais baixa ainda importa no câncer
Existem vários tipos de proteínas RAS. MRAS forma um complexo muito estável com SHOC2 e PP1C, enquanto os mais conhecidos motores do câncer KRAS, HRAS e NRAS formam versões mais fracas do mesmo complexo. Surpreendentemente, células cancerosas impulsionadas por KRAS, HRAS ou NRAS mutantes mostram forte dependência de SHOC2, mesmo que seus complexos sejam menos estáveis. Grandes conjuntos de dados de triagem genética mostram que muitos tumores com certas mutações em RAS — especialmente aquelas em posições-chave como Q61 e G13 — são altamente sensíveis à perda de SHOC2, o que indica que essa montagem é essencial para sua sobrevivência.
Revelando a forma do complexo com KRAS
Até agora, os cientistas haviam observado apenas a estrutura em alta resolução do complexo baseado em MRAS, de afinidade alta. A versão mais fraca com KRAS se desfazia com facilidade demais para ser capturada. Neste estudo, os autores usaram mutações associadas a doenças que reforçam sutilmente os contatos entre os componentes para estabilizar o complexo SHOC2–KRAS–PP1C tempo suficiente para imaginar por criomicroscopia eletrônica. Eles descobriram que a arquitetura geral corresponde de perto ao complexo com MRAS, mas o KRAS carece de vários pequenos elementos estruturais que o MRAS usa para segurar SHOC2 e PP1C com mais firmeza. Como resultado, o complexo com KRAS apresenta menos área de contato e forma menos ligações, o que explica por que é intrinsecamente menos estável, embora permaneça altamente importante em tumores onde o KRAS está hiperativo.
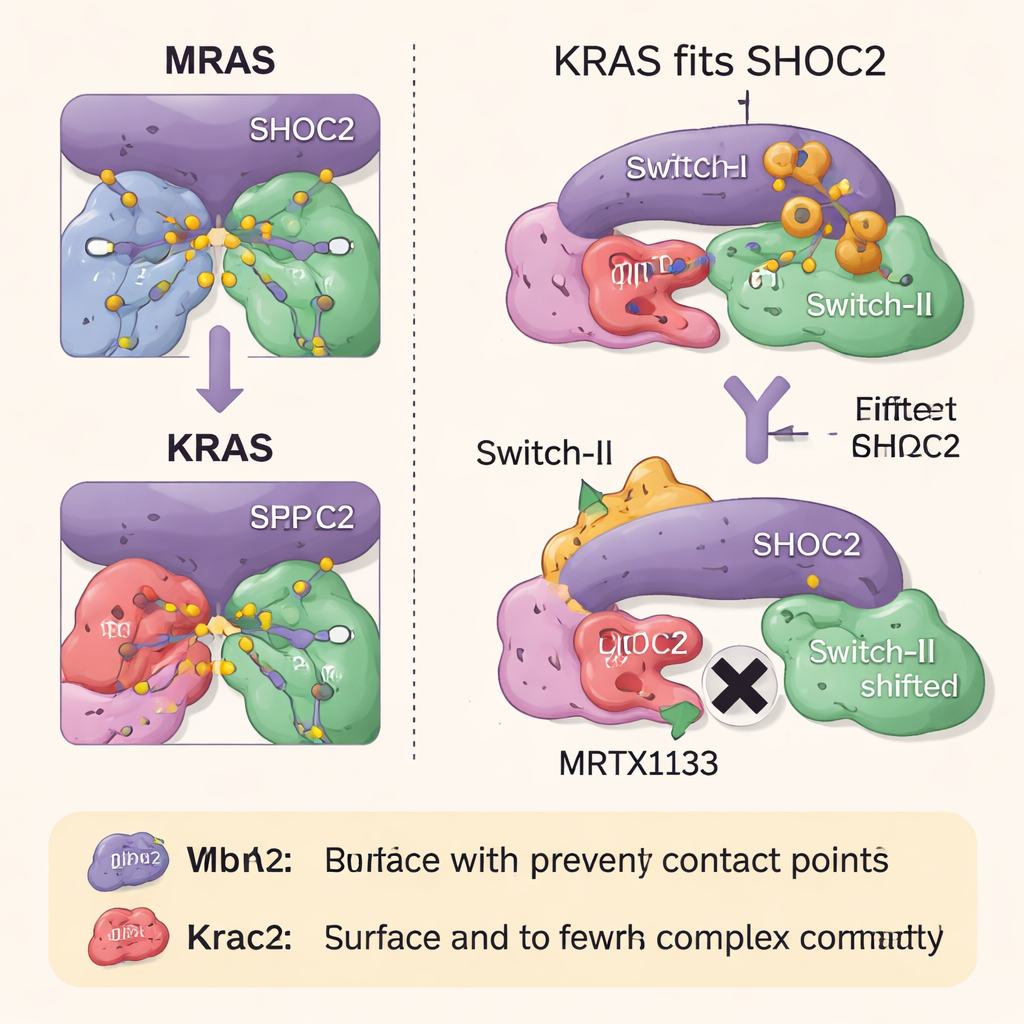
Como os fármacos contra RAS bloqueiam a montagem do complexo
A equipe então explorou como duas classes de fármacos direcionados a RAS influenciam esse complexo tripartido. MRTX1133, projetado para se ligar a uma cavidade perto de uma região flexível do KRAS conhecida como Switch-II, trava essa região em uma conformação que entra em conflito com a superfície de SHOC2. Isso impede fortemente a formação de novos complexos SHOC2–KRAS–PP1C, embora seja menos eficaz em desmontar complexos já existentes. Um segundo fármaco, RMC-6236, atua em conjunto com uma proteína auxiliar (ciclogenina A) e também bloqueia as mesmas superfícies do KRAS necessárias para a ligação a SHOC2. Nenhum dos dois fármacos, porém, liga-se naturalmente ao MRAS, de modo que o complexo de alta afinidade com MRAS permanece intacto e pode ajudar a reativar a via de crescimento quando o KRAS é inibido.
Rumo ao duplo direcionamento para prevenir resistência
Para testar se o direcionamento duplo é possível, os pesquisadores projetaram uma versão de MRAS cuja cavidade de Switch-II foi alterada para que MRTX1133 pudesse agora ligar-se. Esse mutante ainda formou um complexo forte com SHOC2 e PP1C, mas o fármaco passou a bloquear sua montagem e reduziu sua capacidade de ativar RAF em ensaios in vitro. Juntamente com dados sobre compostos que se ligam a SHOC2, esses resultados mostram que é realista projetar fármacos que desliguem tanto os complexos baseados em KRAS quanto os baseados em MRAS. Para um leigo, a mensagem central é que células cancerosas usam múltiplos interruptores estreitamente relacionados para manter os sinais de crescimento fluindo, especialmente quando um interruptor é alvo de droga. Ao entender as formas e contatos precisos dentro desses conjuntos proteicos, os pesquisadores podem agora planejar terapias que atinjam simultaneamente ambas as rotas de reserva, tornando mais difícil para cânceres dirigidos por RAS se adaptarem e desenvolverem resistência ao tratamento.
Citação: Bonsor, D.A., Finci, L.I., Potter, J.R. et al. Structure of SHOC2-KRAS-PP1C complex reveals RAS isoform-specific determinants and insights into targeting complex assembly by RAS inhibitors. Nat Commun 17, 1614 (2026). https://doi.org/10.1038/s41467-026-68319-1
Palavras-chave: sinalização RAS, inibidores de KRAS, via MAPK, complexos proteicos, resistência a fármacos