Clear Sky Science · pt
Regulação por pH mediada por lipídios reversível em conexina-46/50 por cryo-EM
Por que canais celulares minúsculos importam para a saúde e a doença
A cada segundo, nossas células trocam sinais elétricos e pequenas moléculas através de túneis microscópicos chamados junções comunicantes. Esses canais ajudam o coração a bater em sincronia, o cérebro a eliminar subprodutos tóxicos e o cristalino do olho a permanecer transparente. Quando as condições dentro das células ficam ácidas, como ocorre durante AVC, ataque cardíaco ou formação de catarata, muitos desses canais se fecham — mas como eles detectam e respondem à acidez tem sido um mistério antigo. Este estudo usa microscopia crioeletrônica de alta resolução para revelar, quase átomo por átomo, como canais específicos no cristalino se fecham em resposta ao ácido e como esse processo pode ser totalmente reversível.
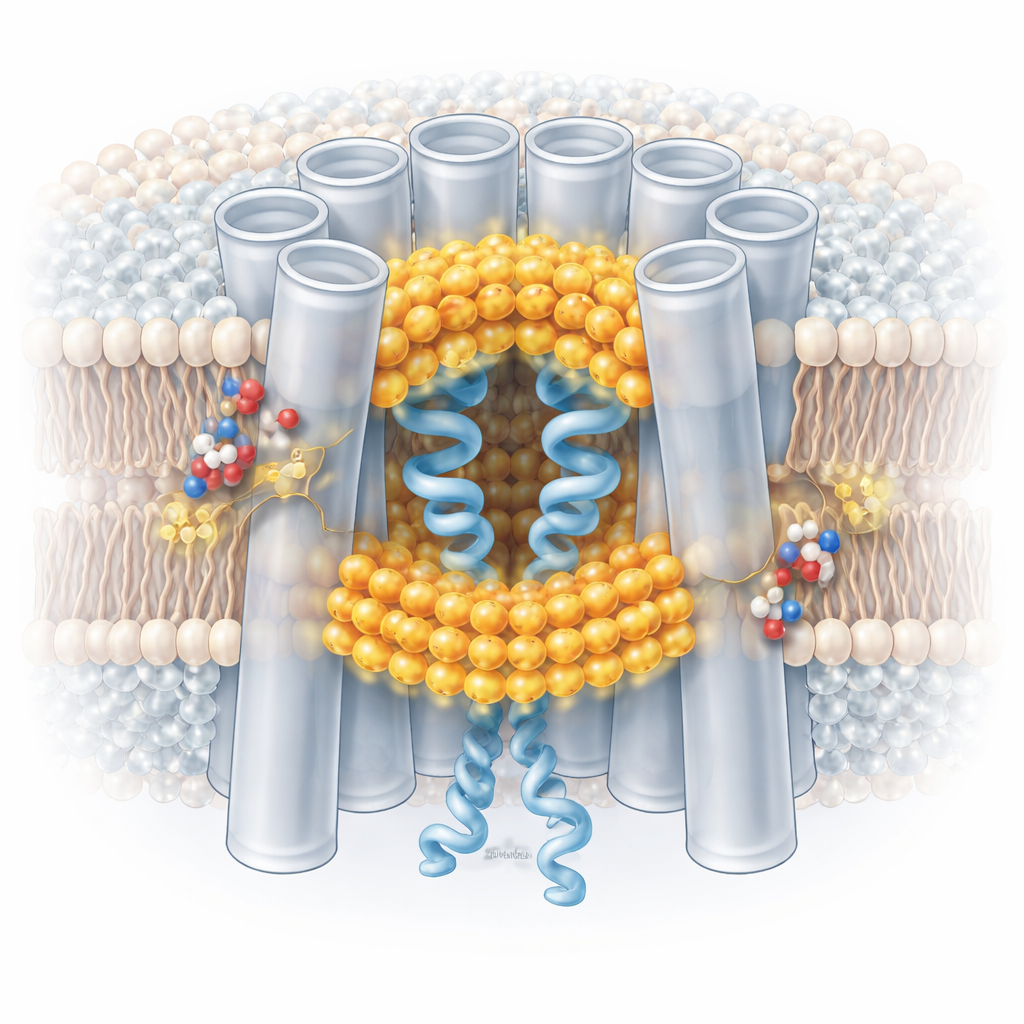
Túneis celulares que mantêm os tecidos sincronizados
As junções comunicantes são formadas por proteínas chamadas conexinas, que se organizam em canais em forma de anel atravessando as membranas de duas células vizinhas. Este trabalho foca em um par de conexinas intimamente relacionadas, conexina-46 e conexina-50, que formam canais no cristalino do olho. Esses canais permitem que íons e pequenas moléculas fluam diretamente entre células, ajudando a manter a clareza do cristalino e a saúde geral do tecido. Quando as células estão sob estresse, no entanto, os mesmos canais podem se tornar vias para sinais prejudiciais. Para proteger os tecidos, as junções comunicantes se fecham quando o interior da célula se torna mais ácido. Entender o mecanismo em escala fina dessa “regulação por pH” é importante para decifrar como os tecidos sobrevivem ao estresse e por que certas mutações levam a doenças como as cataratas.
Observando canais em movimento com cryo-EM
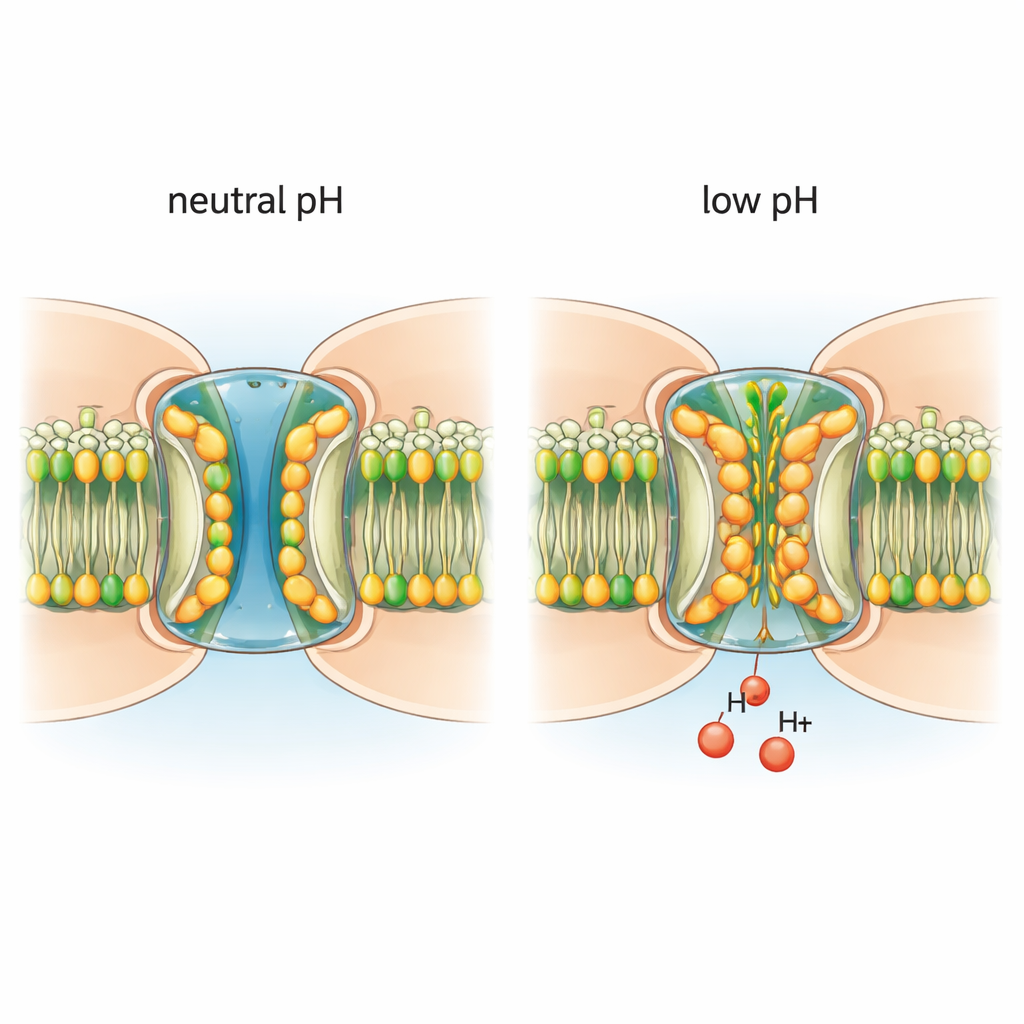
Os pesquisadores purificaram canais nativos de conexina-46/50 de cristalinos de ovelhas envelhecidas e os incorporaram em uma membrana modelo. Usando microscopia crioeletrônica, eles imagearam os canais em resolução quase atômica sob condições neutras, que favorecem um poro aberto, e sob condições levemente ácidas, que desencadeiam o fechamento. Em pH neutro, os canais adotam em grande parte um estado aberto estável, com um túnel central largo o suficiente para íons e pequenas moléculas e com um segmento flexível, o domínio N-terminal, revestindo a entrada do poro. Nessas condições o poro está limpo: nenhuma molécula extra bloqueia a passagem, e os lipídios da membrana circundante permanecem organizados em camadas regulares.
O ácido atrai lipídios para dentro do poro
Quando o ambiente foi levemente acidificado, a arquitetura do canal mudou de forma marcante. Moléculas lipídicas da membrana circundante foram atraídas para dentro do poro, deslizando entre e sob os segmentos N-terminais. Esses lipídios invasores formam um “gaxeto” hidrofóbico em duas camadas que empurra os domínios N-terminais para dentro, estreitando o canal e ajudando a bloquear o tráfego. Lipídios adicionais se alojam entre subunidades proteicas vizinhas em suas interfaces, aparentemente servindo como caminhos de entrada da membrana para o poro. Importante, quando os canais foram colocados em um ambiente detergente que carece de uma membrana lipídica verdadeira, o pH baixo deixou de induzir essas mudanças estruturais. Isso demonstra que lipídios reais não são meros observadores: eles são parceiros necessários no processo de regulação por pH.
Um interruptor de segurança reversível e finamente ajustado
Ao rastrear milhões de partículas individuais de canais, os autores descobriram que o pH baixo não simplesmente alterna os canais de totalmente abertos para totalmente fechados. Em vez disso, ele desloca a população para uma mistura de estados: algumas subunidades dentro de um canal exibem conformações bloqueadas estabilizadas por lipídios, enquanto outras permanecem mais abertas. O comportamento de fechamento é em grande parte não cooperativo — cada bloco de construção do canal pode responder de forma relativamente independente. Condições ácidas favorecem essas conformações bloqueadas, mas quando o pH retorna ao neutro, os lipídios do poro recuam para a membrana e os canais retornam ao estado aberto. Aminoácidos conservados chamados histidinas, que ganham carga positiva em pH baixo, parecem ajudar a recrutar e estabilizar os lipídios interfaciais que iniciam esse processo, oferecendo um sensor molecular plausível para o pH.
Implicações para cataratas e proteção dos tecidos
Esses resultados apoiam um modelo no qual os lipídios atuam como tampões móveis que controlam reversivelmente o fluxo através das junções comunicantes em resposta à acidez. No cristalino, tal mecanismo pode ajudar a isolar células danificadas e impedir a disseminação de sinais tóxicos, mas um fechamento crônico ou mal regulado também pode contribuir para a formação de catarata relacionada à idade. Como intrusões lipídicas semelhantes foram observadas em famílias de canais relacionadas, o trabalho sugere um princípio mais geral: sob estresse, as próprias membranas celulares podem fornecer componentes dinâmicos que ajudam a ligar ou desligar canais vitais, oferecendo novas ideias para fármacos que estabilizem tanto os estados abertos quanto os fechados em doenças.
Citação: Jarodsky, J.M., Myers, J.B. & Reichow, S.L. Reversible lipid-mediated pH-gating of connexin-46/50 by cryo-EM. Nat Commun 17, 1606 (2026). https://doi.org/10.1038/s41467-026-68311-9
Palavras-chave: junções comunicantes, conexina 46/50, regulação por pH, catarata, cryo-EM