Clear Sky Science · pt
Transcriptômica dinâmica de célula única revela formação de rede neural guiada por lsamp em S. japonicum macho que impulsiona a reprodução feminina
Por que a vida amorosa de um parasita importa
A esquistossomose é uma doença parasitária que adoece mais de 250 milhões de pessoas, principalmente em regiões mais pobres com acesso médico limitado. A enfermidade é impulsionada não pelas picadas ou toxinas dos vermes, mas pelo enorme número de ovos postos pelas fêmeas dentro do corpo. Surpreendentemente, as fêmeas só conseguem amadurecer e começar a pôr ovos após acoplarem-se a um macho. Este estudo formula uma pergunta simples, porém crucial: o que, exatamente, o macho faz para ativar a fertilidade da fêmea — e seria possível desligar esse interruptor para deter a doença?
Mapeando um mundo oculto célula a célula
Para responder a isso, os pesquisadores construíram um detalhado “atlas celular” do caramujo sanguíneo Schistosoma japonicum durante a janela-chave em que machos e fêmeas se emparelham e se desenvolvem sexualmente. Usando RNA-seq de célula única, uma técnica que lê quais genes estão ativos em células individuais, eles analisaram mais de 100.000 células de vermes coletados em quatro pontos no tempo após a infecção em camundongos. Identificaram 76 tipos celulares distintos, incluindo vários tipos de neurônios, células-tronco e células reprodutivas. Isso permitiu acompanhar como populações celulares específicas se expandem, encolhem ou mudam de identidade à medida que os vermes crescem e passam a se reproduzir.
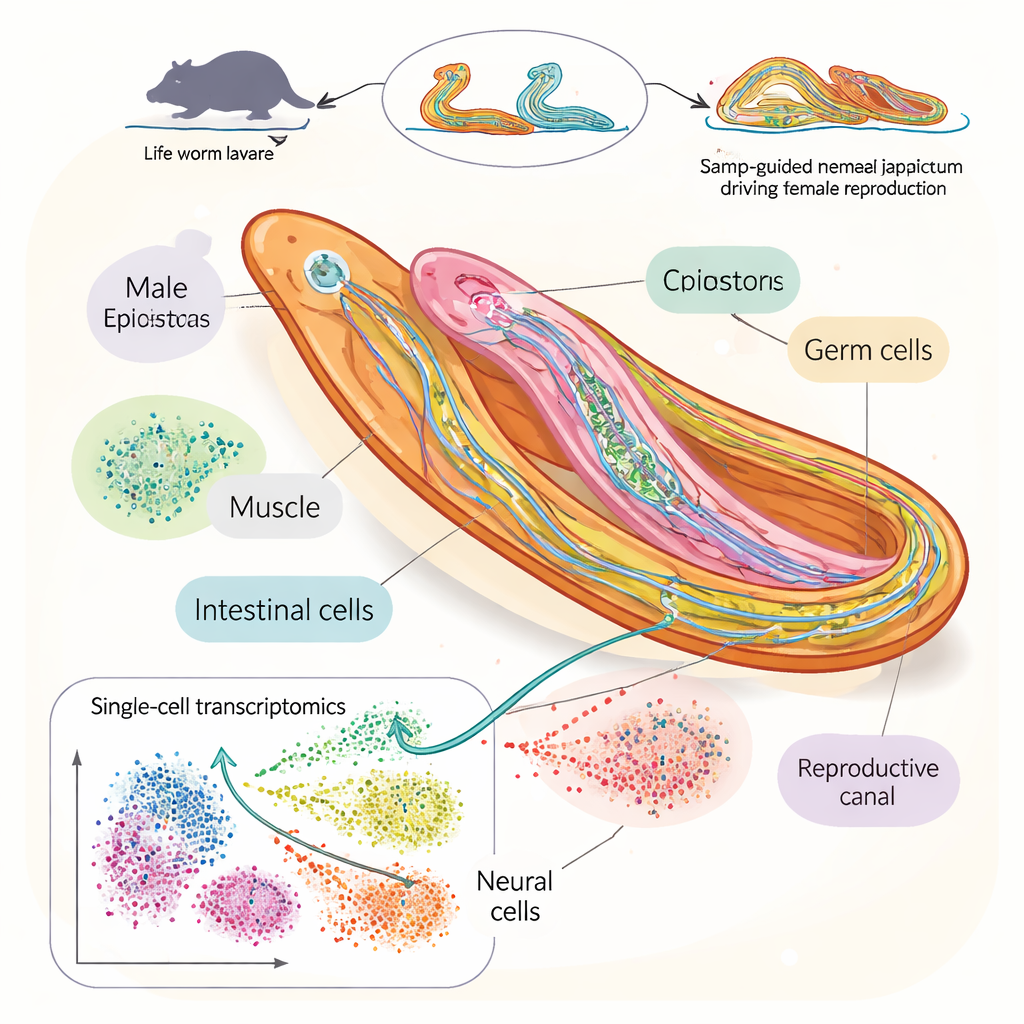
Acompanhando a ascensão de ovos e espermatozoides
Ao aprofundar-se nas células dos testículos, ovários e tecidos relacionados, a equipe reconstruiu o desenvolvimento em etapas de espermatozoides e óvulos. Eles mostraram como células-tronco germinativas dão origem a células reprodutivas tardias por meio de programas de atividade gênica distintos em machos e fêmeas. Nas fêmeas, os genes que sustentam o crescimento dos ovos enfatizam produção e empacotamento de proteínas, enquanto nos machos há maior ênfase em estruturas como cílios e microtúbulos que ajudam o movimento do esperma. O estudo também mapeou como o enorme órgão de suporte de ovos nas fêmeas, o vitelário, se desenvolve por estágios intermediários e identificou novos marcadores genéticos que revelam o grau de maturidade de cada tecido reprodutor.
Um circuito neural exclusivo de machos em um canal de preensão
Uma das descobertas mais surpreendentes veio do sistema nervoso. Em vez de uma coleção frouxa de neurônios, o atlas revelou cinco linhagens neuronais claramente definidas, incluindo várias que diferiam entre machos e fêmeas. Três tipos neuronais — denominados N2.2, N3.2 e N4.3 — estavam fortemente enriquecidos em machos e agrupados dentro do canal ginecofórico, um sulco especializado que o macho usa para acomodar a fêmea. Entre eles, os neurônios N4.3 se destacaram por expressarem um gene chamado nrps, que produz a enzima responsável por gerar BATT, um pequeno peptídeo feromônio previamente mostrado como estimulador do desenvolvimento sexual feminino. Em outras palavras, essas células N4.3 são as “estações de sinal” do macho para ativar a fertilidade da fêmea.
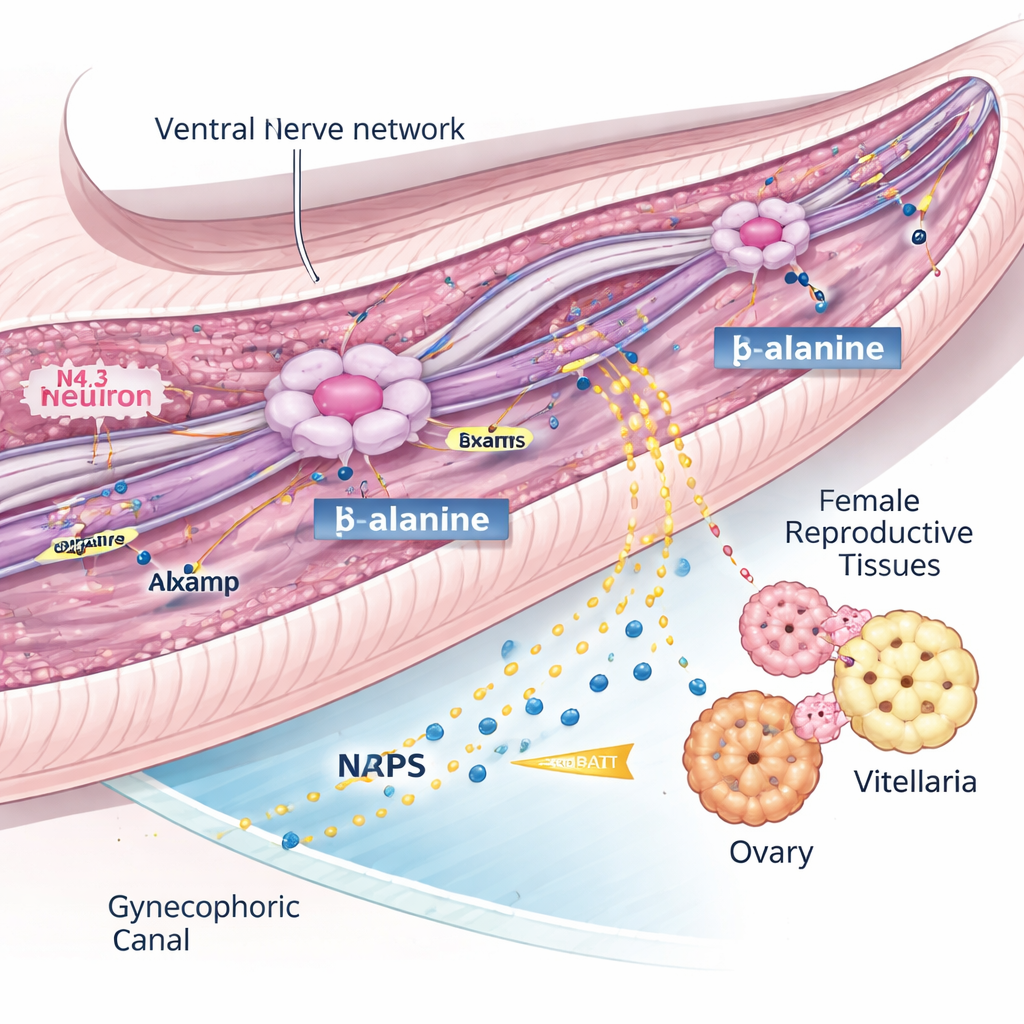
Uma molécula guia que mantém o sinal fluindo
Para entender como esses neurônios N4.3 funcionam, os pesquisadores buscaram genes que parecessem orientar seu desenvolvimento e função. Eles se concentraram em lsamp, um gene conhecido em outros animais por auxiliar neurônios a se conectarem e a manterem seus axônios. Em vermes machos, lsamp era ativado nos mesmos neurônios N4.3 que produzem a enzima BATT, e sua atividade aumentou acentuadamente à medida que os vermes amadureciam. Usando interferência por RNA para reduzir lsamp nos machos, a equipe observou que as fêmeas emparelhadas não conseguiram desenvolver plenamente ovários e vitelários e puseram quase nenhum ovo. Ainda assim, os neurônios N4.3 continuaram presentes, o gene nrps permaneceu ativo e os ingredientes químicos brutos para BATT não foram alterados. Em vez disso, os machos deficientes em lsamp exibiram fibras nervosas danificadas e transporte de vesículas interrompido ao longo de microtúbulos estabilizados, e produziram muito menos BATT dentro do corpo e no meio circundante. Isso sugere que lsamp é vital para manter uma rede nervosa ventral que entrega um precursor chave, provavelmente β-alanina, aos neurônios N4.3 para que eles possam sintetizar feromônio suficiente para ativar a fêmea.
Diminuindo o interruptor reprodutivo
Para não especialistas, a mensagem principal é que a capacidade deste parasita de causar doença depende de uma conversa íntima entre machos e fêmeas, conduzida por uma rede neural especializada e um feromônio minúsculo. O estudo mostra que uma única molécula guia, lsamp, ajuda a construir e manter a fiação nervosa ventral do macho; quando essa fiação falha, o macho não consegue mais enviar um sinal químico forte o bastante para maturar totalmente os órgãos reprodutores da fêmea, e a produção de ovos cai drasticamente. Ao traçar as células do parasita em alta resolução e revelar esse circuito neural exclusivo de machos, o trabalho aponta para novas formas de bloquear a produção de ovos — oferecendo uma estratégia potencial para conter a esquistossomose, cuja tratamento atual depende de um único medicamento envelhecido.
Citação: You, Y., Cheng, S., Chen, X. et al. Dynamic single-cell transcriptomics reveals lsamp-guided neural network formation in male S. japonicum driving female reproduction. Nat Commun 17, 1602 (2026). https://doi.org/10.1038/s41467-026-68305-7
Palavras-chave: esquistossomose, transcriptômica de célula única, reprodução de parasitas, circuitos neurais, sinalização por feromônios