Clear Sky Science · pt
Mecanismo de resistência do SARS-CoV-2 a antivirais à base de análogos de nucleotídeos
Como o vírus engana medicamentos antivirais essenciais
O vírus da COVID-19 pertence a um grupo raro de vírus de RNA que conseguem revisar seu material genético, o que o torna incomumente apto a resistir a alguns dos nossos melhores antivirais. Este estudo investiga em nível atômico como o SARS-CoV-2 detecta e remove uma classe amplamente usada de medicamentos chamada análogos de nucleotídeos, explicando por que fármacos que funcionam bem contra outros vírus frequentemente têm desempenho inferior contra infecções por coronavírus.
Uma disputa pela molécula de RNA viral
O SARS-CoV-2 copia seu genoma de ~30.000 letras de RNA usando uma grande máquina molecular chamada complexo de replicação–transcrição. No seu núcleo está a RNA‑dependente RNA polimerase (RdRp), que sintetiza novas fitas de RNA, e uma unidade separada, a exonuclease (ExoN), que revisa e aparará erros. Muitos comprimidos antivirais, incluindo fármacos originalmente desenvolvidos para hepatite C, imitam tão de perto os blocos construtores naturais do RNA que a RdRp os insere, mas com modificações sutis que travam a cópia ou introduzem erros. Infelizmente, os coronavírus têm ExoN, que pode reconhecer esses impostores depois que eles estão na cadeia de RNA e cortá‑los, resgatando a replicação viral.
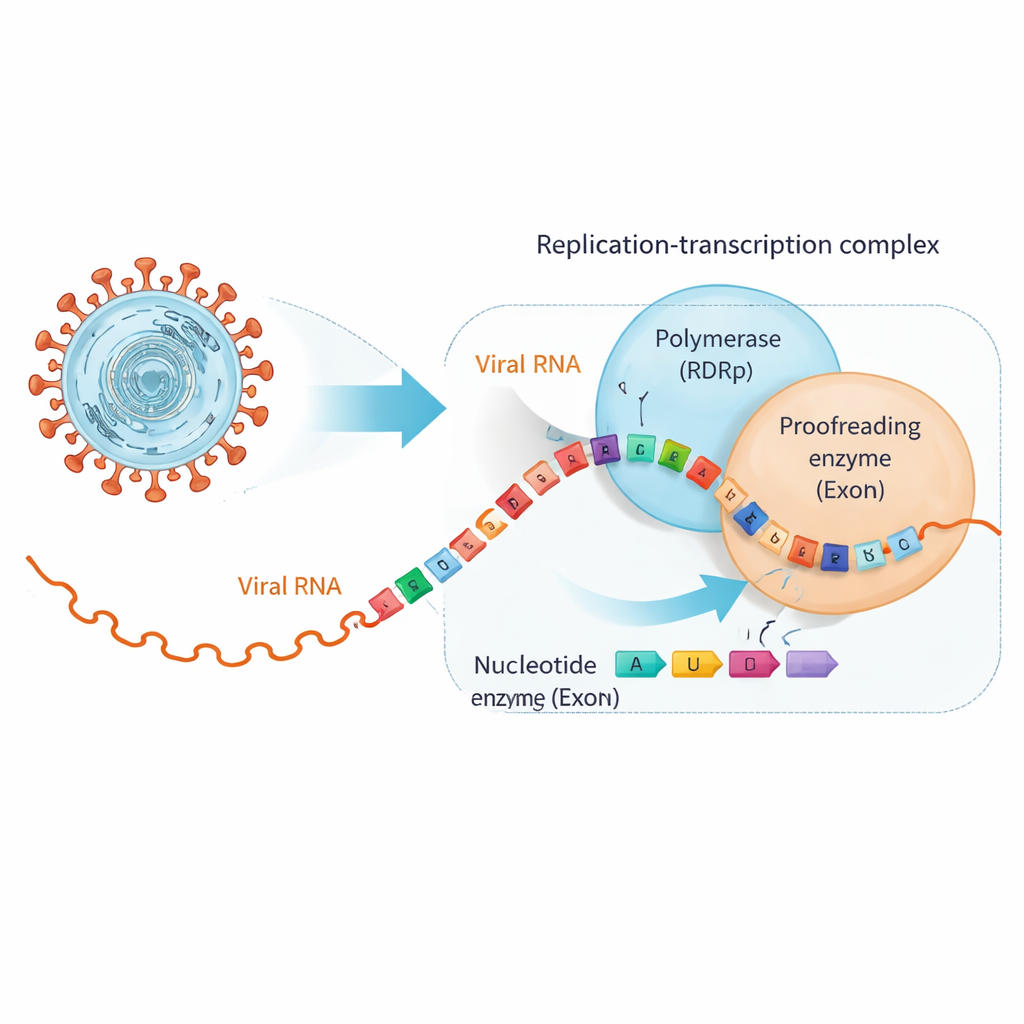
Quando fármacos úteis fazem o RNA mudar de parceiro
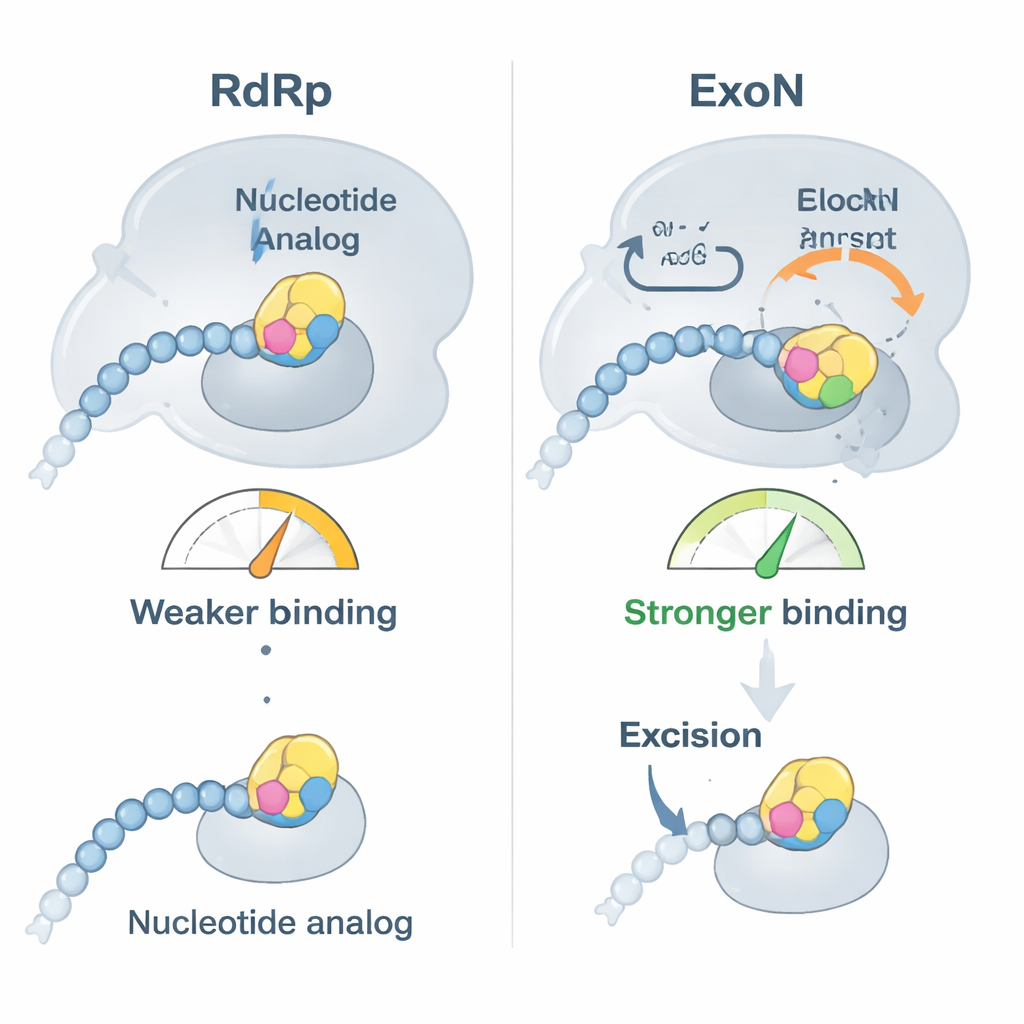
Os pesquisadores focaram em dois antivirais clinicamente importantes, bemnifosbuvir e sofosbuvir, ambos projetados para agir como blocos de construção defeituosos do RNA. Primeiro eles mostraram que a polimerase do SARS‑CoV‑2 insere facilmente esses análogos na extremidade de uma fita de RNA e então em grande parte para de estender a cadeia, como pretendido. No entanto, testes de ligação revelaram uma reviravolta: uma vez que um análogo está na ponta do RNA, o RNA deixa de se ligar tão firmemente à polimerase e, em vez disso, se liga mais fortemente à ExoN. Em efeito, o RNA modificado pelo medicamento é empurrado para fora da máquina de cópia e entregue ao revisor, que então tem a chance de remover o nucleotídeo problemático e permitir que a replicação continue.
Correção que é desacelerada, mas não interrompida
Experimentos bioquímicos ao longo do tempo mostraram que a ExoN realmente remove bemnifosbuvir e sofosbuvir do RNA, mas mais lentamente do que remove nucleotídeos normais. Em reações sem células, ambos os análogos bloquearam fortemente a síntese adicional de RNA — contudo, quando uma ExoN ativa foi adicionada, uma fração significativa das cadeias de RNA paradas foi resgatada e estendida. Um mutante de ExoN desativado não conseguiu fazer isso, confirmando que a atividade de correção é responsável por desfazer grande parte do efeito dos fármacos. A presença da polimerase juntamente com a ExoN acelerou na verdade a remoção dos análogos, sugerindo que as duas enzimas virais trabalham em conjunto para limpar obstáculos e manter a replicação em andamento.
Observando o revisor em resolução atômica
Para entender como a ExoN reconhece e responde a esses fármacos, a equipe usou criomicroscopia eletrônica de alta resolução para resolver estruturas do complexo ExoN ligado a fitas de RNA terminadas em bemnifosbuvir ou sofosbuvir. Essas estruturas, nítidas o suficiente para ver grupos químicos individuais, revelaram que o anel de açúcar modificado de cada fármaco se ajusta a um bolso hidrofóbico formado por uma pequena alça da proteína ExoN. Esse encaixe mais firme explica a ligação mais forte do RNA contendo o medicamento à ExoN. Mas isso também tem um efeito colateral inesperado: ao puxar essa alça, os fármacos perturbam o arranjo preciso de uma alça catalítica próxima que mantém um resíduo de histidina chave no lugar. Quando essa histidina se afasta do sítio de corte, o centro ativo da ExoN fica parcialmente desativado, desacelerando, mas não impedindo completamente, a excisão do análogo.
Um interruptor embutido que ajusta a correção viral
Mutar aminoácidos individuais dentro da alça sensível confirmou sua importância. Alterações em quatro resíduos conservados reduziram muito a capacidade da ExoN de cortar tanto extremidades de RNA padrão quanto extremidades terminadas por fármacos, e também modificaram qual nucleotídeo final a ExoN prefere remover. Isso identifica a alça como um regulador alostérico — um interruptor mecânico embutido que detecta que tipo de nucleotídeo está na ponta do RNA e ajusta a atividade da enzima. As estruturas mostram adicionalmente que a ExoN reconhece diferentes bases (A, U, C ou G) por meio de ligações de hidrogênio flexíveis, mas tem mais dificuldade em acomodar bases semelhantes à guanina, o que é relevante porque o bemnifosbuvir mimetiza a guanosina.
O que isso significa para futuras pílulas contra COVID-19
Para não especialistas, a mensagem chave é que o SARS‑CoV‑2 carrega um sofisticado “verificador ortográfico” que pode arrancar certos fármacos de seu genoma depois que eles já fizeram seu papel de travar a replicação. Bemnifosbuvir e sofosbuvir enfraquecem a máquina de cópia do vírus, mas ao mesmo tempo direcionam o RNA para o revisor que pode desfazer parcialmente seus efeitos. Ao revelar exatamente como o revisor viral agarra esses fármacos, e como uma pequena alça reguladora alterna a enzima entre estados mais ativos e menos ativos, este trabalho oferece um roteiro para projetar novos nucleotídeos antivirais que ou se liguem mal à ExoN, a prendam em uma conformação inativa, ou explorem sua dificuldade em lidar com estruturas semelhantes à guanina. Moléculas de próxima geração assim poderiam ser muito mais difíceis para o vírus “apagar”, melhorando nossa capacidade de tratar COVID‑19 e futuros surtos de coronavírus.
Citação: Liu, C., Li, Y., Cao, X. et al. Mechanism of SARS-CoV-2 resistance to nucleotide analog-based antivirals. Nat Commun 17, 1601 (2026). https://doi.org/10.1038/s41467-026-68304-8
Palavras-chave: SARS-CoV-2, resistência a antivirais, análogos de nucleotídeos, correção de RNA, replicação do coronavírus