Clear Sky Science · pt
Desencadeamento de hidroximassa por ácido de Lewis permite oxidação eletroquímica seletiva da ureia a nitrito com produção concomitante de hidrogênio economizadora de energia
Transformando Resíduos em Produtos Químicos Úteis e Combustível Limpo
A ureia é mais conhecida como componente da urina e de fertilizantes, mas em águas residuais ela se torna um poluente persistente. Este estudo mostra como a ureia pode ser transformada de um passivo em um recurso: usando um catalisador projetado com inteligência, os autores convertem ureia em nitrito, um produto químico valioso para fertilizantes e medicamentos, enquanto produzem simultaneamente hidrogênio com consumo de eletricidade menor do que a eletrólise convencional da água. O trabalho oferece um vislumbre de estações de tratamento futuras que limpam a água, fabricam produtos úteis e geram energia limpa ao mesmo tempo.
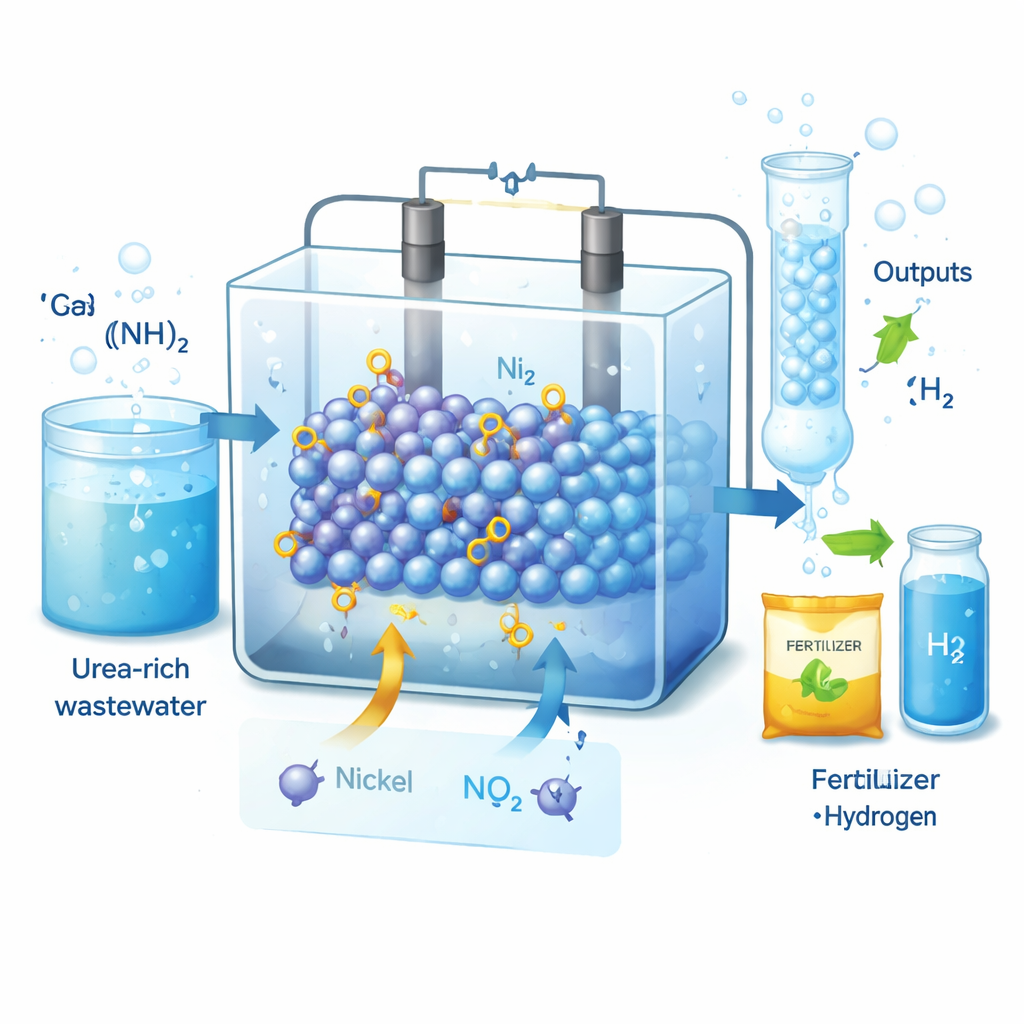
Por que Nitrito e Hidrogênio Importam
O nitrito é um ingrediente chave na agricultura, na conservação de alimentos e na indústria farmacêutica, e a demanda global é medida em milhões de toneladas por ano. Hoje, a maior parte do nitrito é produzida pelo processo Ostwald, que opera em alta temperatura, consome grande quantidade de energia e libera óxidos de nitrogênio poluentes. Ao mesmo tempo, águas residuais domésticas e industriais carregam grande carga de ureia, representando 70–80% dos poluentes de nitrogênio. Se essa ureia pudesse ser convertida eletroquimicamente em nitrito enquanto também gera gás hidrogênio, poderíamos tanto limpar a água quanto fornecer dois produtos de alto valor—desde que o processo seja eficiente e seletivo o bastante.
Guiando as Reações pelo Caminho Certo
Quando a ureia é oxidada em solução alcalina, ela pode seguir dois caminhos principais. Um leva a gás nitrogênio inerte e dióxido de carbono; o outro, mais desejável, leva a nitrito e nitrato, que são produtos comercializáveis. O problema é que a maioria dos catalisadores à base de níquel, os mais usados nessa reação, não é muito seletiva—eles tendem a produzir uma mistura de produtos e ainda desperdiçar energia promovendo a reação de evolução de oxigênio, que gera oxigênio gasoso sem retorno econômico. Os autores propuseram redesenhar a superfície do catalisador de modo que íons hidróxido, a espécie reativa OH⁻ em meio alcalino, sejam concentrados e direcionados de forma a favorecer o corte das ligações carbono–nitrogênio e a formação de nitrito, em vez de permitir que os átomos de nitrogênio se acoplem formando N₂.
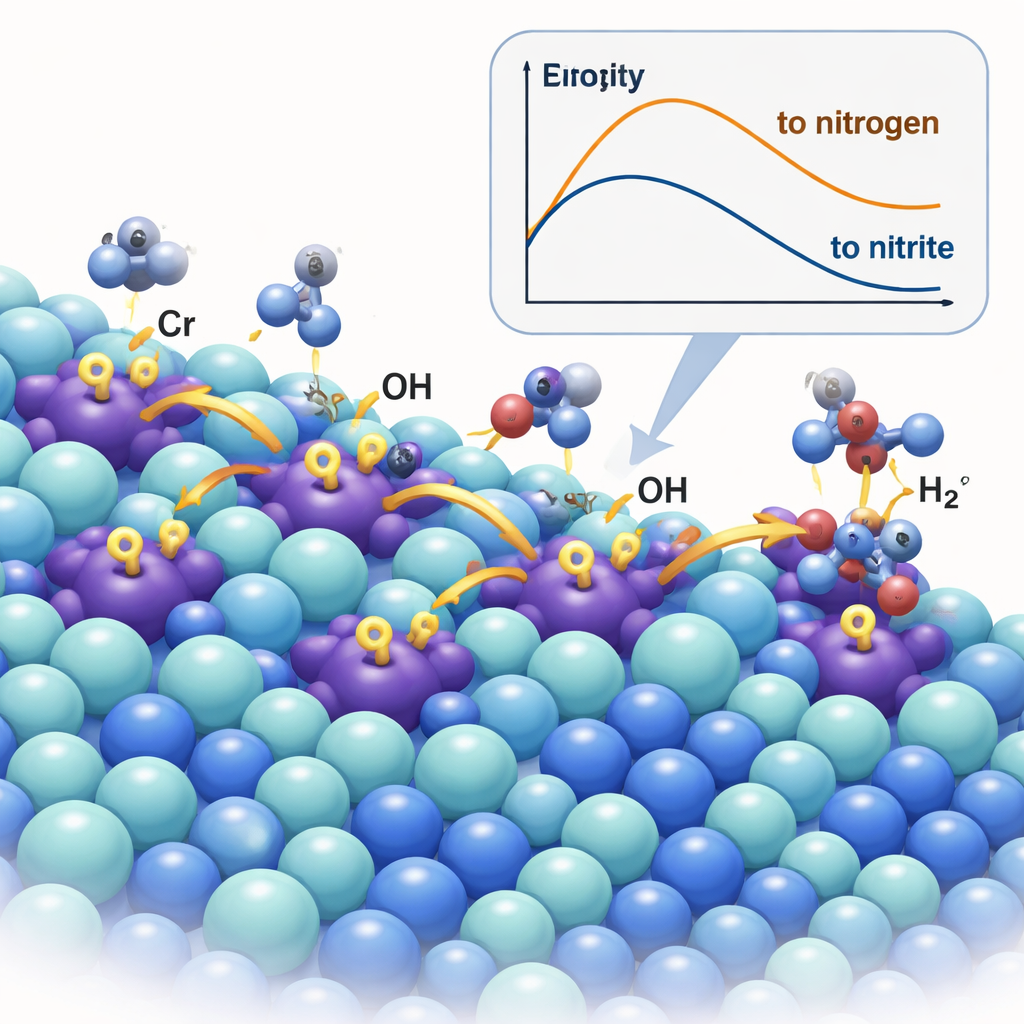
Um Catalisador que Bombeia Espécies Reativas
A equipe criou um novo material dopando sulfeto de níquel (Ni₃S₂) com uma pequena quantidade de cromo, formando Cr–Ni₃S₂. Íons de cromo atuam como os chamados sítios ácido de Lewis—centros pobres em elétrons que atraem fortemente íons hidróxido. Usando microscopia avançada, técnicas de raios X e espectroscopia, os pesquisadores confirmaram que átomos de Cr se incorporam à rede do sulfeto de níquel e a comprimem e distorcem sutilmente, alterando a distribuição eletrônica. Em condições de reação, os sítios de cromo atuam como pequenas bombas: capturam OH⁻ e então o “derramam” para sítios vizinhos de níquel, onde ocorre a oxidação da ureia. Medidas in situ por Raman e infravermelho, bem como experimentos de rotulagem isotópica, traçaram diretamente esse derramamento de hidróxido de Cr para Ni e mostraram que ele acelera a formação de sítios ativos de oxihidróxido de níquel (NiOOH) que impulsionam a química desejada.
Altos Rendimentos, Menor Energia e Boa Estabilidade
Porque o OH⁻ é entregue eficientemente aos locais corretos, o catalisador Cr–Ni₃S₂ converte ureia em nitrito com seletividade impressionante. Em densidades de corrente relevantes para a indústria, ele alcança um rendimento de nitrito de cerca de 121 miligramas por hora por centímetro quadrado, com eficiências faradaicas para nitrito acima de 80%, mantendo a reação concorrente de evolução de oxigênio abaixo de 1,5%. O catalisador permanece estável por centenas de horas de operação contínua com vazamento de cromo desprezível. O mesmo material também reduz dramaticamente a tensão necessária quando emparelhado com um cátodo evolucionador de hidrogênio em um dispositivo de eletrólise assistida por ureia, reduzindo o custo elétrico da produção de hidrogênio para aproximadamente 3,7 quilowatt-hora por metro cúbico de H₂—menos do que a eletrólise alcalina convencional. Análises técnico-econômicas sugerem que, a 400 miliampères por centímetro quadrado, processar uma tonelada de ureia nesse sistema poderia gerar da ordem de US$ 1.200 em valor líquido quando tanto o nitrito quanto o hidrogênio são contabilizados.
Da Célula de Laboratório a Dispositivos Energéticos Práticos
Para demonstrar o potencial no mundo real, os autores construíram uma célula de fluxo para eletrólise contínua assistida por ureia e uma bateria Zn–ureia–ar. Na bateria, substituir a usual reação de evolução de oxigênio durante o carregamento pela oxidação da ureia reduziu a tensão de carga em quase 0,3 volts enquanto mantinha desempenho estável por mais de 100 horas. Isso significa que o dispositivo pode tanto tratar correntes contendo ureia quanto fornecer armazenamento de eletricidade com maior eficiência energética. A mesma estratégia de design com sítios de ácido de Lewis também funcionou quando outros metais como estanho e titânio, ou um hospedeiro diferente como sulfeto de cobre, foram usados, sugerindo que a abordagem é amplamente aplicável.
Uma Ideia Simples por Trás de uma Reação Complexa
Para não especialistas, a ideia central é que os pesquisadores aprenderam a direcionar onde e como um ingrediente reativo comum—o hidróxido—se posiciona e se move sobre a superfície do catalisador. Ao adicionar sítios de cromo que atuam como fortes atratores e retransmissores de OH⁻, eles facilitam que moléculas de ureia sejam fatiadas em nitrito em vez de serem completamente oxidadas a gás nitrogênio. Ao mesmo tempo, essa via exige menos energia elétrica e produz naturalmente hidrogênio. Essencialmente, o trabalho mostra que o projeto atômico cuidadoso dos “padrões de tráfego” em catalisadores pode transformar águas residuais em fonte tanto de produtos químicos quanto de energia limpa.
Citação: Fan, C., Zhang, M., Li, Y. et al. Lewis acid-triggered hydroxyl spillover enables selective urea electrooxidation to nitrite with concurrent energy-saving hydrogen production. Nat Commun 17, 1585 (2026). https://doi.org/10.1038/s41467-026-68302-w
Palavras-chave: oxidação da ureia, produção de nitrito, geração de hidrogênio, eletrocatálise, valorização de águas residuais