Clear Sky Science · pt
Variantes de novo no gene do fator de splicing SF3B1 estão associadas a transtornos do neurodesenvolvimento
Quando Um Gene Desorganiza o Projeto Inicial do Cérebro
Por que algumas crianças desenvolvem dificuldades de aprendizagem, convulsões ou problemas de alimentação mesmo quando a gravidez e o parto parecem normais? Este estudo examina um único gene, chamado SF3B1, que ajuda as células a processar mensagens genéticas. Os pesquisadores mostram que mudanças novas e espontâneas nesse gene podem embaralhar de forma sutil como as células cerebrais leem as instruções do DNA, levando a uma síndrome do neurodesenvolvimento antes não reconhecida.
Um Editor Mestre das Mensagens Genéticas
Cada célula do nosso corpo precisa converter o texto genético bruto em instruções claras antes de poder fabricar proteínas. Essa etapa de edição, conhecida como splicing de RNA, remove segmentos não codificantes e junta as partes úteis. SF3B1 é um componente central da “máquina de splicing” celular. Até agora, alterações em SF3B1 eram conhecidas principalmente por seu papel em cânceres, onde células tumorais adquirem mutações nesse gene ao longo da vida. O novo trabalho faz uma pergunta diferente: o que acontece quando uma alteração prejudicial em SF3B1 está presente desde a concepção em todas as células do corpo?
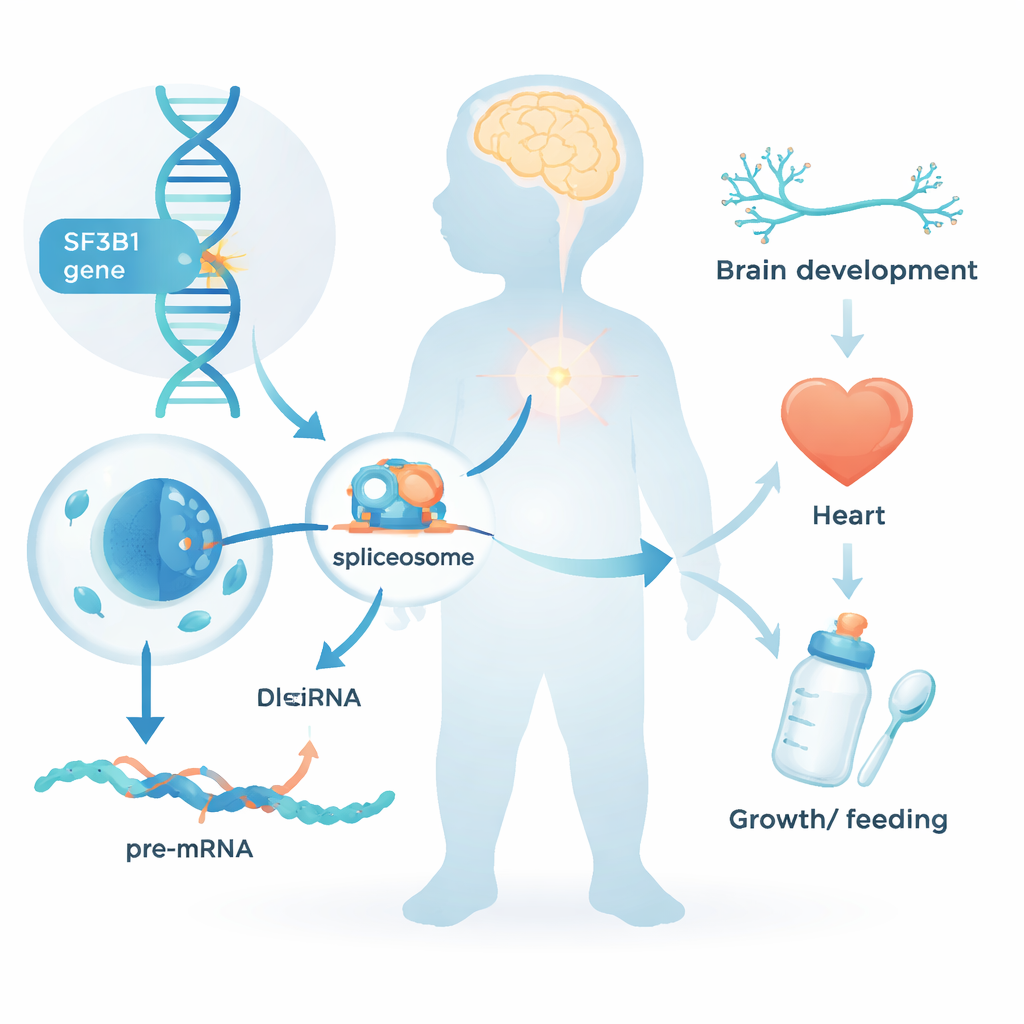
Uma Síndrome Infantil Recentemente Reconhecida
A equipe reuniu dados de 26 crianças e jovens adultos que todos carregavam variantes raras de SF3B1, em sua maioria surgindo de novo—isto é, não herdadas de nenhum dos pais. Quase todos apresentavam problemas de neurodesenvolvimento: atrasos em aprender a sentar, andar ou falar; deficiência intelectual em sua maioria de grau leve a moderado; e, em cerca de metade dos casos, convulsões. Muitos tinham tônus muscular reduzido e precisavam de ajuda extra para se alimentar, às vezes por sonda gástrica. As feições faciais eram sutilmente incomuns, mas não idênticas entre as crianças; uma característica notavelmente comum foi o palato alto ou fendido. Vários participantes também tinham defeitos cardíacos, restrição de crescimento ou cabeça pequena, mostrando que o impacto das alterações em SF3B1 vai além do cérebro.
Dois Tipos de Alterações Genéticas, Dois Padrões Clínicos
Os pesquisadores distinguiram dois grandes tipos de variantes em SF3B1. Um grupo incluiu alterações de “perda de função”, como sinais de parada prematura, que provavelmente reduzem a quantidade de proteína SF3B1 funcional. O segundo grupo continha variantes missense, nas quais um único aminoácido da proteína é alterado. Ao agrupar as características médicas das crianças, a equipe observou que aquelas com variantes missense tendiam a ter problemas mais graves e complexos, incluindo uma taxa maior de anomalias cardíacas e gastrointestinais, baixa estatura e microcefalia. Variantes de perda de função, em contraste, às vezes foram herdadas de um dos pais levemente afetado ou até aparentemente saudável, sugerindo que simplesmente ter menos SF3B1 pode ser compatível com sintomas relativamente leves em alguns indivíduos.
Erros de Ajuste Fino em Vez de Uma Falha Completa
Para entender o que as variantes missense fazem dentro das células, os cientistas as recriaram em linhagens celulares de laboratório. Surpreendentemente, essas proteínas SF3B1 alteradas ainda conseguiam realizar o trabalho básico de splicing o suficiente para resgatar células nas quais o SF3B1 normal havia sido silenciado. Isso descartou uma explicação simples de perda de função. Usando sequenciamento profundo de RNA, a equipe então examinou todo o conjunto de mensagens celulares. Eles descobriram que as variantes missense deslocaram sutilmente o splicing de centenas de genes, especialmente ao alterar quais sítios de splicing eram escolhidos nas extremidades dos éxons e ao causar, ocasionalmente, salto de éxons. A escala da perturbação foi menor do que a observada com a clássica mutação associada ao câncer SF3B1 K700E, mas ainda substancial: muitos dos genes afetados estão envolvidos no desenvolvimento do cérebro, na fiação neural e em processos fundamentais como o manuseio de RNA e a síntese proteica.
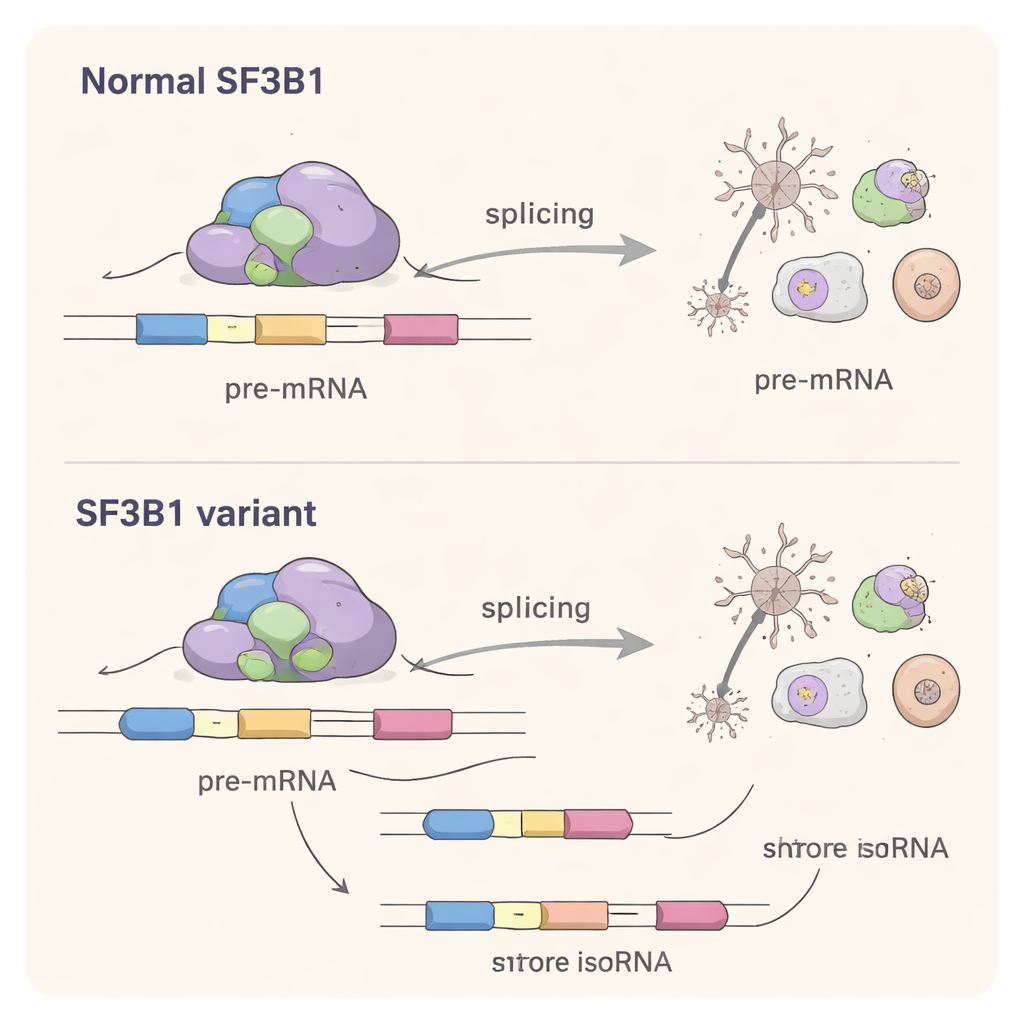
Um Mecanismo Compartilhado Entre Câncer e Transtornos Cerebrais
Embora a maioria das variantes de SF3B1 associadas ao neurodesenvolvimento ocorra em posições diferentes das bem‑conhecidas mutações cancerígenas, elas perturbam o mesmo processo central: o reconhecimento preciso dos sítios de splicing no RNA. O estudo mostra que essas variantes do desenvolvimento têm sua própria “assinatura de splicing”, escolhendo sítios de splicing alternativos que costumam ficar mais próximos dos normais do que aqueles favorecidos no câncer. Isso sugere um mecanismo de mudança de função, em que a proteína mutada compete com a cópia normal e empurra a máquina de splicing a escolhas ligeiramente erradas em muitos genes ao mesmo tempo.
O Que Isso Significa para Famílias e Pesquisas Futuras
Para as famílias afetadas, o trabalho identifica SF3B1 como uma nova causa de transtornos do neurodesenvolvimento que agora pode ser testada em clínicas genéticas, potencialmente encerrando longas buscas diagnósticas. Mais amplamente, adiciona SF3B1 a uma lista pequena, mas crescente, de genes de splicing cujas alterações podem provocar tanto câncer quanto transtornos cerebrais infantis, dependendo de quando e como o gene é alterado. Ao mapear como variantes específicas de SF3B1 remodelam o splicing de RNA, o estudo lança bases para futuras terapias destinadas a corrigir o splicing incorreto de forma direcionada.
Citação: Uguen, K., Bergot, T., Scott-Boyer, MP. et al. De novo variants in the splicing factor gene SF3B1 are associated with neurodevelopmental disorders. Nat Commun 17, 1569 (2026). https://doi.org/10.1038/s41467-026-68284-9
Palavras-chave: Splicing de RNA, SF3B1, transtornos do neurodesenvolvimento, variantes de novo, spliceosomopatias