Clear Sky Science · pt
Hidrogel viscoelástico primador de macrófagos CAR para tratamento de fibrose pulmonar
Transformando os faxineiros do corpo em equipes de reparo de precisão
A fibrose pulmonar é uma doença pulmonar devastadora em que o tecido pulmonar normal e elástico é gradualmente substituído por cicatriz rígida. As pessoas têm dificuldade para respirar, e os medicamentos atuais na maioria das vezes apenas desaceleram o declínio. Este estudo explora uma ideia nova: converter as próprias células de limpeza do corpo, os macrófagos, em “faxineiros inteligentes” geneticamente programados e, em seguida, aumentar seu poder com um gel macio especialmente projetado. Juntas, essas abordagens ajudam as células a caçar os agentes formadores de cicatriz e até a afrouxar o tecido rígido nos pulmões danificados.
Quando a cura se torna prejudicial
Em pulmões saudáveis, os fibroblastos ajudam a manter a delicada rede de colágeno que sustenta os alvéolos. Na fibrose pulmonar, essas células ficam hiperativas, depositando filamentos espessos de colágeno que comprimem os espaços aéreos. Medicamentos existentes podem atenuar esses processos, mas raramente os reverter. Os autores concentram-se em uma marca na superfície celular chamada proteína de ativação de fibroblastos (FAP), que é abundante em fibroblastos hiperativos e rara em tecido normal. Se células imunes pudessem ser treinadas para reconhecer a FAP, talvez pudessem remover seletivamente os fibroblastos “descontrolados” que impulsionam a cicatrização, poupando as células saudáveis ao redor.
Reprogramando macrófagos para mirar nos construtores de cicatriz
Macrófagos são células imunes circulantes que normalmente englobam células mortas, microrganismos e detritos celulares. A equipe as equipou com um receptor antigênico quimérico (CAR) que reconhece a FAP, criando macrófagos CAR (CAR‑Ms). Em placas de cultura, esses CAR‑Ms engoliram eficientemente fibroblastos ricos em FAP e os mataram, enquanto em grande parte ignoravam células com FAP reduzida. Também degradaram géis ricos em colágeno mais vigorosamente do que macrófagos não modificados, sugerindo um duplo benefício: eliminar as células que criam a cicatriz e quebrar diretamente a matriz cicatricial. Esses efeitos foram observados tanto em linhagens celulares padrão quanto em macrófagos primários de camundongos, que se aproximam mais da situação real nos tecidos. 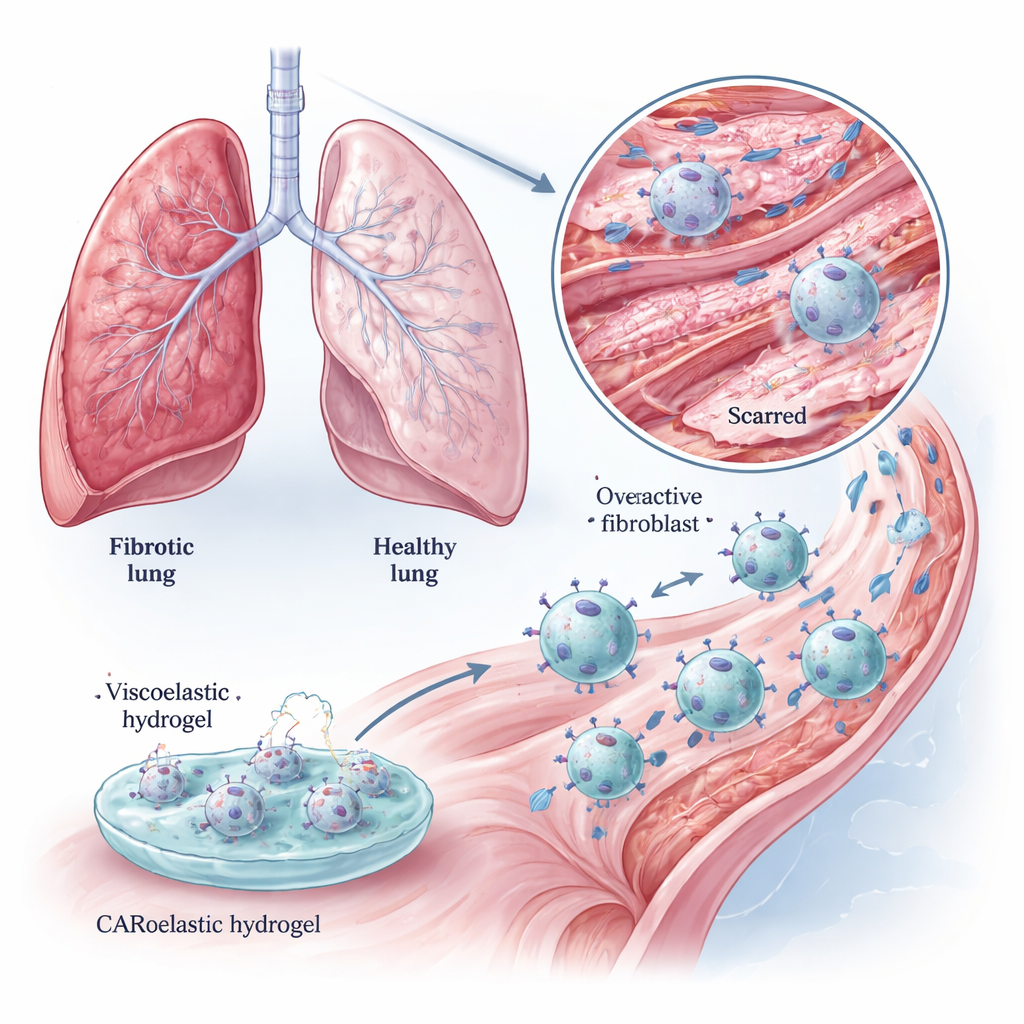
Priming de células imunes com um gel viscoelástico e macio
Engenharia genética de células é poderosa, mas complexa. Os pesquisadores, portanto, perguntaram se um estímulo puramente físico — um hidrogel viscoelástico e macio — poderia ajustar ainda mais o comportamento dos CAR‑Ms. Construíram um hidrogel de gelatina–alginato cujo “módulo de perda”, uma medida de como ele relaxa lentamente sob tensão, podia ser afinado sem alterar a rigidez global. Quando CAR‑Ms foram brevemente cultivados em géis com a viscoelasticidade adequada, sua capacidade de matar fibroblastos alvo aumentou mais do que com estimulantes químicos comuns, e o aumento durou pelo menos dois dias. Esses “Gel‑CAR‑Ms” também ativaram genes ligados à ativação imune e remodelamento tecidual, enquanto reduziram a expressão de genes associados à fibrose, sugerindo que a experiência no gel imprimiu uma identidade mais anti‑cicatriz nas células.
Como uma superfície mais macia reprograma o comportamento celular
Para entender por que o gel importava, a equipe examinou o estado físico dos receptores CAR na superfície celular. Uma sonda fluorescente revelou que os CAR‑Ms primados no hidrogel tinham menor tensão de membrana — a “pele” externa da célula estava mais relaxada. Nestas condições, as moléculas CAR se espalharam de aglomerados apertados para unidades mais isoladas, em pares ou individualizadas. Testes bioquímicos mostraram que esses receptores dispersos favoreciam formas que disparavam sinalização interna mais facilmente, particularmente em vias como ERK que controlam ativação e capacidade de matar. Imitar a queda de tensão com uma pequena molécula reproduziu o mesmo espalhamento dos receptores e melhorou a morte de células‑alvo, apoiando a ideia de que o relaxamento mecânico da membrana é suficiente para “pré‑armar” as células antes mesmo de encontrarem seus alvos. 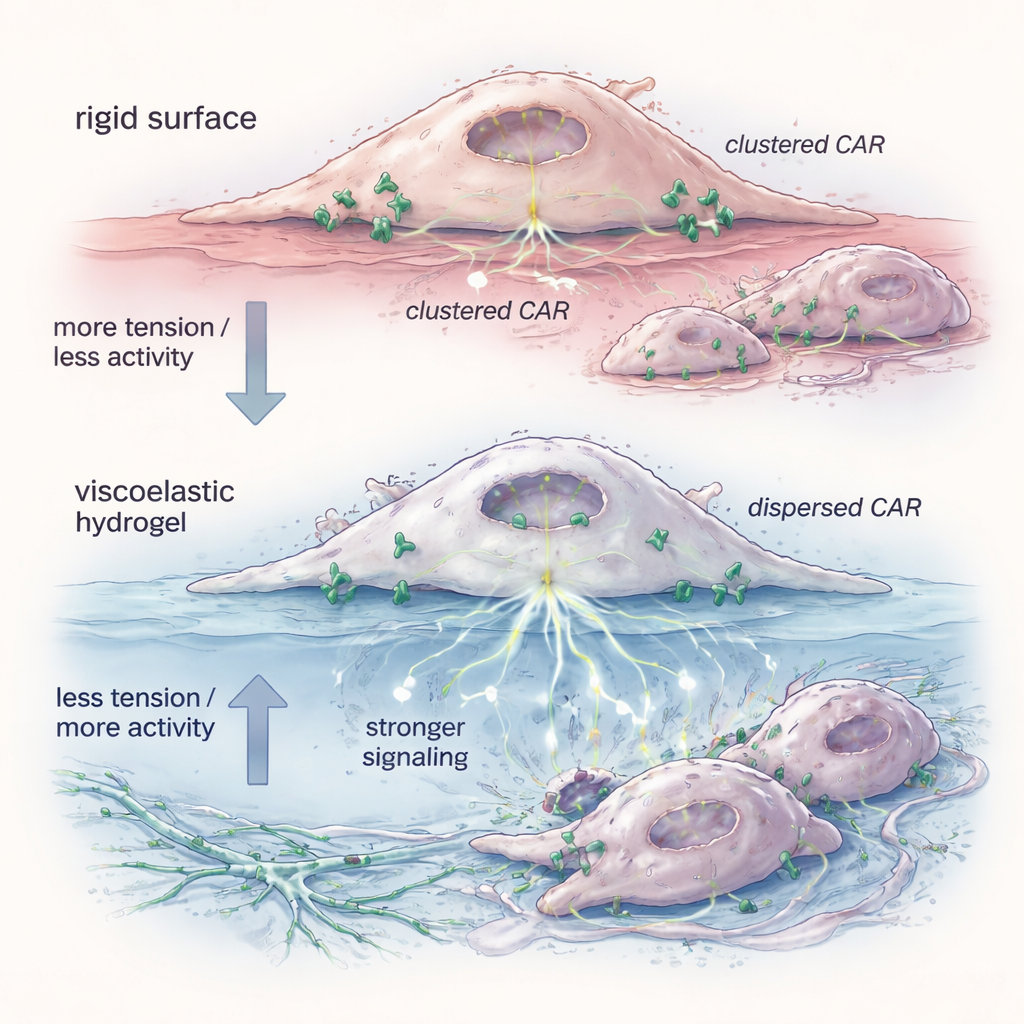
Reparando pulmões cicatrizados em camundongos
O teste definitivo foi realizado em um modelo murino de fibrose pulmonar induzida por droga. Os animais receberam macrófagos comuns, CAR‑Ms padrão ou Gel‑CAR‑Ms primados no hidrogel. Todos os camundongos tratados melhoraram em comparação com controles não tratados, mas os Gel‑CAR‑Ms tiveram o melhor desempenho: seus pulmões continham menos colágeno, espaços aéreos mais normais e menos fibroblastos positivos para FAP. Análises genéticas do tecido pulmonar mostraram que os Gel‑CAR‑Ms reduziram sinais inflamatórios e a expressão de genes relacionados à cicatriz de forma mais eficaz do que os CAR‑Ms padrão. As células rastreadas persistiram no pulmão por pelo menos uma semana, e verificações de segurança estendidas por 12 semanas não encontraram danos significativos a órgãos, alterações sanguíneas ou sinais de autoimunidade.
Uma nova direção para terapias celulares anti‑fibrose
Para não especialistas, a mensagem principal é que a combinação de engenharia celular direcionada e materiais inteligentes pode transformar células imunes inatas em ferramentas altamente eficazes, porém não excessivamente complexas em termo genético, de combate à cicatriz. Ao repousar brevemente macrófagos engenheirados sobre um gel macio cuidadosamente ajustado, os pesquisadores “pré‑definiram” mecanicamente seus receptores de superfície para um modo mais responsivo. Em camundongos com fibrose pulmonar, isso se traduziu em melhor remoção de fibroblastos nocivos, degradação do excesso de colágeno e restauração parcial da estrutura pulmonar normal — sem problemas de segurança evidentes. Embora muito trabalho ainda seja necessário antes de testes em humanos, essa estratégia sugere que afinar o ambiente físico de células terapêuticas pode um dia tornar os tratamentos para doenças pulmonares fibróticas mais potentes e precisos.
Citação: Zhang, Y., Liu, Z., Kong, W. et al. Viscoelastic hydrogel primed CAR-macrophage for pulmonary fibrosis treatment. Nat Commun 17, 1663 (2026). https://doi.org/10.1038/s41467-025-68033-4
Palavras-chave: fibrose pulmonar, terapia com macrófagos CAR, hidrogel viscoelástico, proteína de ativação de fibroblastos, mecanobiologia celular