Clear Sky Science · pt
Base molecular para a inibição da metilação de DNA de novo por TCL1A
Como as Células Decidem o Que Lembrar
Todas as células do seu corpo carregam essencialmente o mesmo DNA, ainda que células do cérebro, do sangue e da pele se comportem de maneira bem diferente. Uma forma de as células “lembraram” sua identidade é por meio de marcadores químicos adicionados ao DNA, um processo chamado metilação do DNA. Este estudo revela, em detalhe atômico, como uma pequena proteína chamada TCL1A pode desligar as enzimas que escrevem essas marcas metílicas. Como tanto a metilação do DNA quanto o TCL1A estão ligados ao câncer e a distúrbios reprodutivos, entender essa disputa molecular pode, no futuro, inspirar novas terapias.
A Máquina de Marcação do DNA na Célula
A metilação do DNA funciona como uma marca a lápis nas margens do genoma, ajudando a silenciar certos genes e a estabilizar o genoma durante o desenvolvimento celular. Duas enzimas, DNMT3A e DNMT3B, são as principais “escritoras” que colocam novas marcas metílicas durante o desenvolvimento inicial e quando células-tronco se especializam. Se essas enzimas são mutadas ou desreguladas, o padrão das marcas de DNA pode ficar embaralhado, contribuindo para síndromes do desenvolvimento e cânceres hematológicos. TCL1A é uma proteína mais conhecida por seu papel em cânceres de células imunes, onde costuma ser produzida em excesso. Trabalhos anteriores sugeriram que TCL1A pode se ligar a DNMT3A e DNMT3B e reduzir sua atividade, mas ninguém sabia exatamente como isso acontecia.
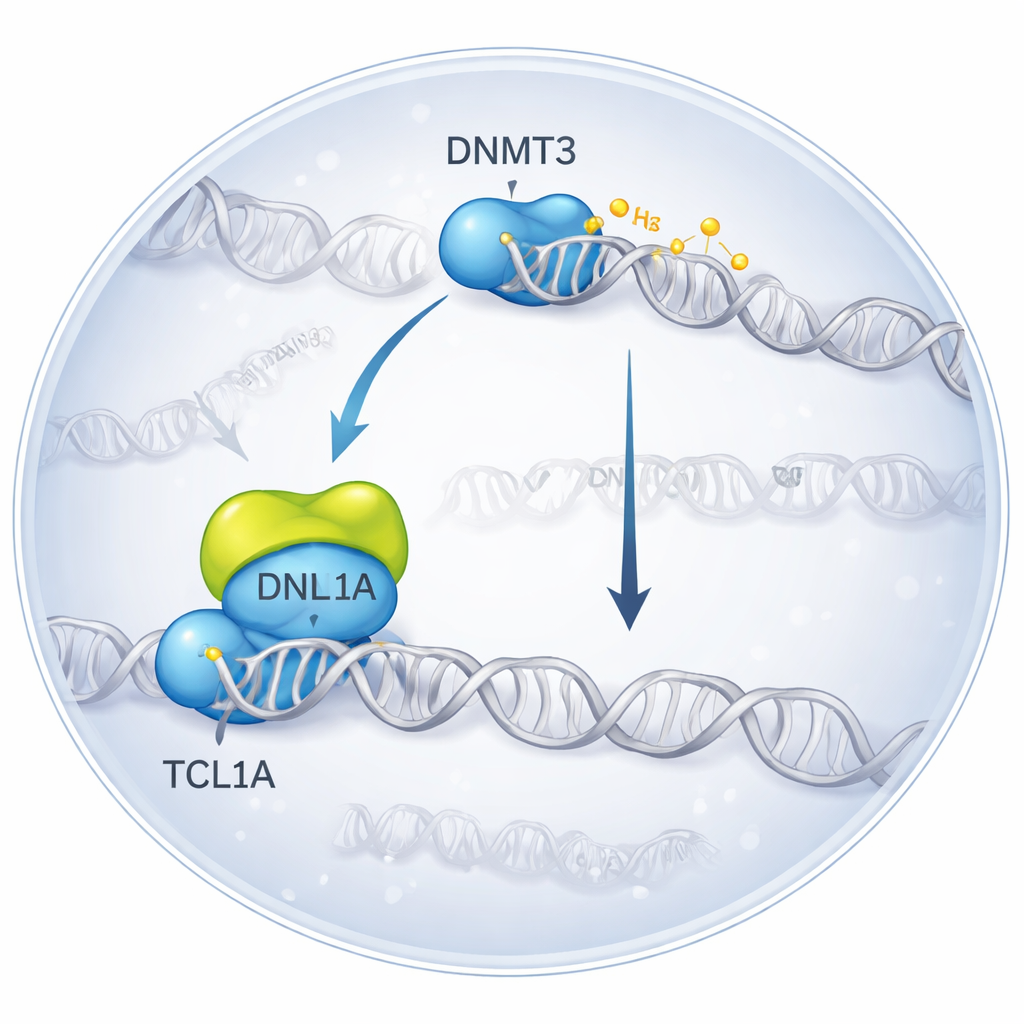
Cristalizando um Encontro Molecular em 3D
Os pesquisadores utilizaram criomicroscopia eletrônica, uma técnica que imagina moléculas congeladas rapidamente, para visualizar o complexo formado quando DNMT3A se liga ao TCL1A. Eles descobriram que duas moléculas de DNMT3A se emparelham e, de cada lado, um dímero de TCL1A se acopla à porção catalítica de DNMT3A — a região que normalmente interage com proteínas auxiliares e com o DNA. Essa superfície de ligação se sobrepõe ao ponto onde outro parceiro, o DNMT3L, costuma se unir para aumentar a atividade da DNMT3A. Em testes bioquímicos, a adição de TCL1A reduziu fortemente a capacidade tanto da DNMT3A quanto da DNMT3B de metilar o DNA, mesmo na presença de DNMT3L, confirmando que o complexo estrutural corresponde a um estado fortemente inibido.
Uma Mudança de Forma Que Trava a Enzima
Analisando mais de perto, a equipe observou que a ligação do TCL1A não se limita a cobrir o sítio ativo como uma tampa. Em vez disso, ela provoca uma mudança sutil, porém de grande alcance, na forma da DNMT3A. Duas regiões flexíveis da enzima, conhecidas como o loop de reconhecimento do alvo e o loop catalítico, afastam-se das posições que ocupam quando a DNMT3A está ligada ao DNA. Na forma ativa, esses loops se acomodam junto ao DNA e formam um bolso para uma pequena molécula combustível chamada SAM, que doa o grupo metil. Com o TCL1A ligado, o loop catalítico dobra-se dentro do bolso do SAM e o bloqueia, além de dificultar o acesso do DNA à enzima. Medidas de ligação confirmaram que a DNMT3A em complexo com TCL1A não consegue mais se prender ao DNA ou ao SAM detectavelmente.
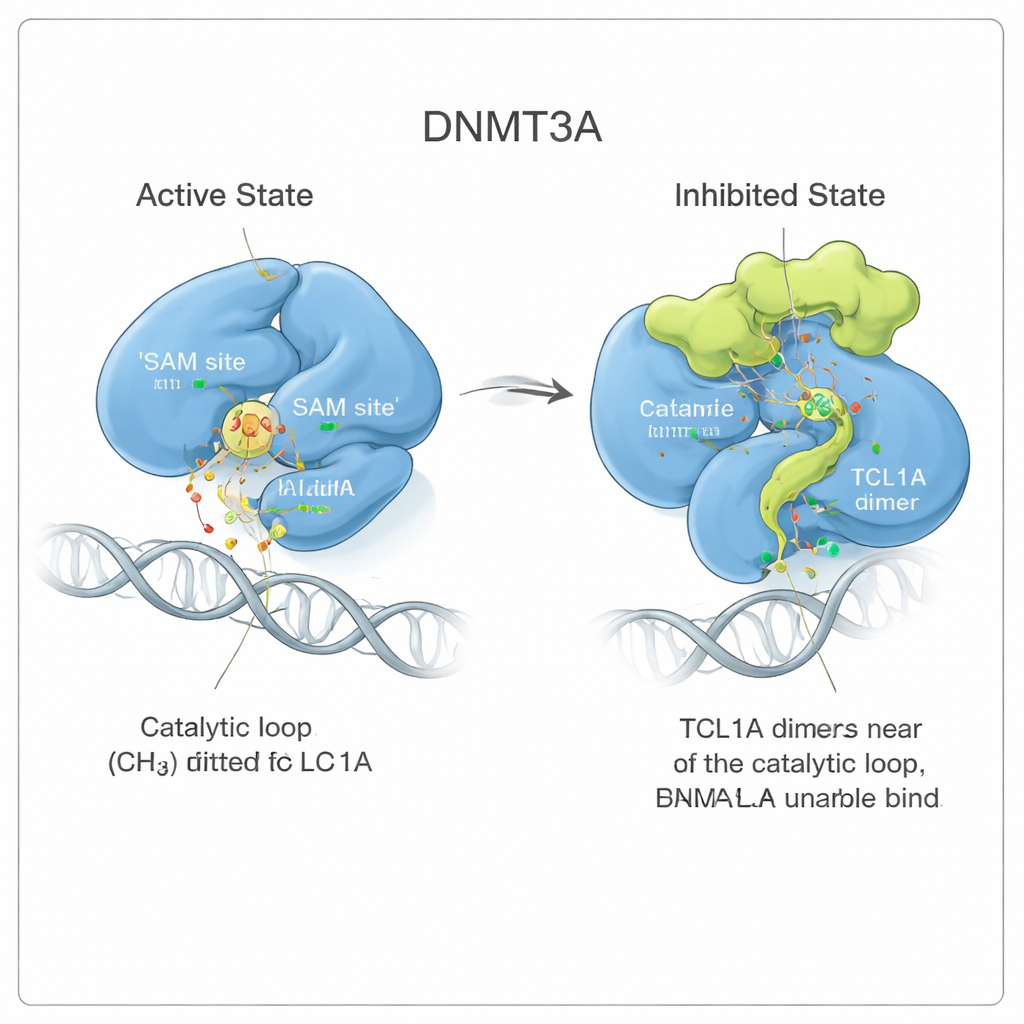
Observando um Bloqueio Dinâmico em Movimento
Para entender quão estável é essa conformação inibida, os autores realizaram longas simulações de dinâmica molecular, essencialmente filmes baseados em física das moléculas em solução. Quando a DNMT3A estava ligada ao seu ativador DNMT3L, o loop catalítico permaneceu firme em sua posição ativa. Na presença do TCL1A, esse loop tornou-se muito mais móvel, vibrando mas ocupando repetidamente o bolso do SAM como algas marinhas que giram e ainda assim entopem um ralo. Esse movimento constante reduziu o espaço disponível para o SAM em mais de dez vezes, apoiando um modelo em que o TCL1A explora a flexibilidade natural da DNMT3A para impor uma forma de inibição dinâmica, em vez de rígida.
Consequências para Células em Desenvolvimento e Doenças
A equipe então investigou o que esse bloqueio molecular significa para células reais. Eles modificaram células-tronco embrionárias de camundongo para produzir TCL1A humano durante uma fase em que as células normalmente aumentam a metilação do DNA ao iniciarem a diferenciação. Mapas de metilação em todo o genoma mostraram que células que superexpressavam TCL1A não alcançaram o nível elevado usual de metilação do DNA, assemelhando-se fortemente a células nas quais os genes Dnmt3a e Dnmt3b foram ambos derrubados (knockout). Uma versão mutante do TCL1A que se liga mal às enzimas DNMT3 teve pouco efeito, destacando que a interação física é essencial. Esses achados ligam o mecanismo estrutural a amplas mudanças epigenéticas ao longo do genoma.
O Significado Para a Saúde
Em conjunto, o trabalho revela como o TCL1A pode agir como um freio poderoso nas enzimas que estabelecem novas marcas de metilação do DNA. Ao se acoplar em uma interface crítica, o TCL1A reposiciona loops flexíveis na DNMT3A e na DNMT3B de modo que elas não conseguem mais se ligar ao molde de DNA nem ao combustível químico, levando a uma perda global de marcas metílicas nas células. No desenvolvimento normal, esse tipo de controle refinado pode ajudar a equilibrar quando e onde a metilação é adicionada. Quando o TCL1A está fora do lugar ou é produzido em excesso, como em certos cânceres sanguíneos e raros distúrbios reprodutivos, esse mesmo mecanismo pode desviar o programa epigenético da célula. Entender essa interação em resolução atômica abre a porta para projetar moléculas que imitem ou contrariem os efeitos do TCL1A, potencialmente restaurando padrões saudáveis de metilação do DNA.
Citação: Liu, Q., Li, J., Wang, X. et al. Molecular basis for the inhibition of de novo DNA methylation by TCL1A. Nat Commun 17, 2159 (2026). https://doi.org/10.1038/s41467-025-67710-8
Palavras-chave: Metilação do DNA, DNMT3A, TCL1A, epigenética, câncer