Clear Sky Science · pt
Métodos de amostragem para cristalografia de raios X de proteínas com foco especial no consumo de amostras
Observando moléculas em ação
A cristalografia de raios X permite aos cientistas ver o arranjo dos átomos em proteínas, as pequenas máquinas que movem a vida. Uma abordagem mais recente, chamada cristalografia serial, vai além: pode capturar “filmes moleculares” de proteínas em ação, como enzimas processando um fármaco ou proteínas fotossintéticas dividindo a água. Mas há um problema. Muitas proteínas importantes são difíceis de produzir e cristalizar, e experimentos atuais podem consumir de miligramas a gramas desse material precioso. Este artigo de revisão faz uma pergunta aparentemente simples: como podemos entregar cristais a feixes poderosos de raios X desperdiçando o mínimo possível de amostra?
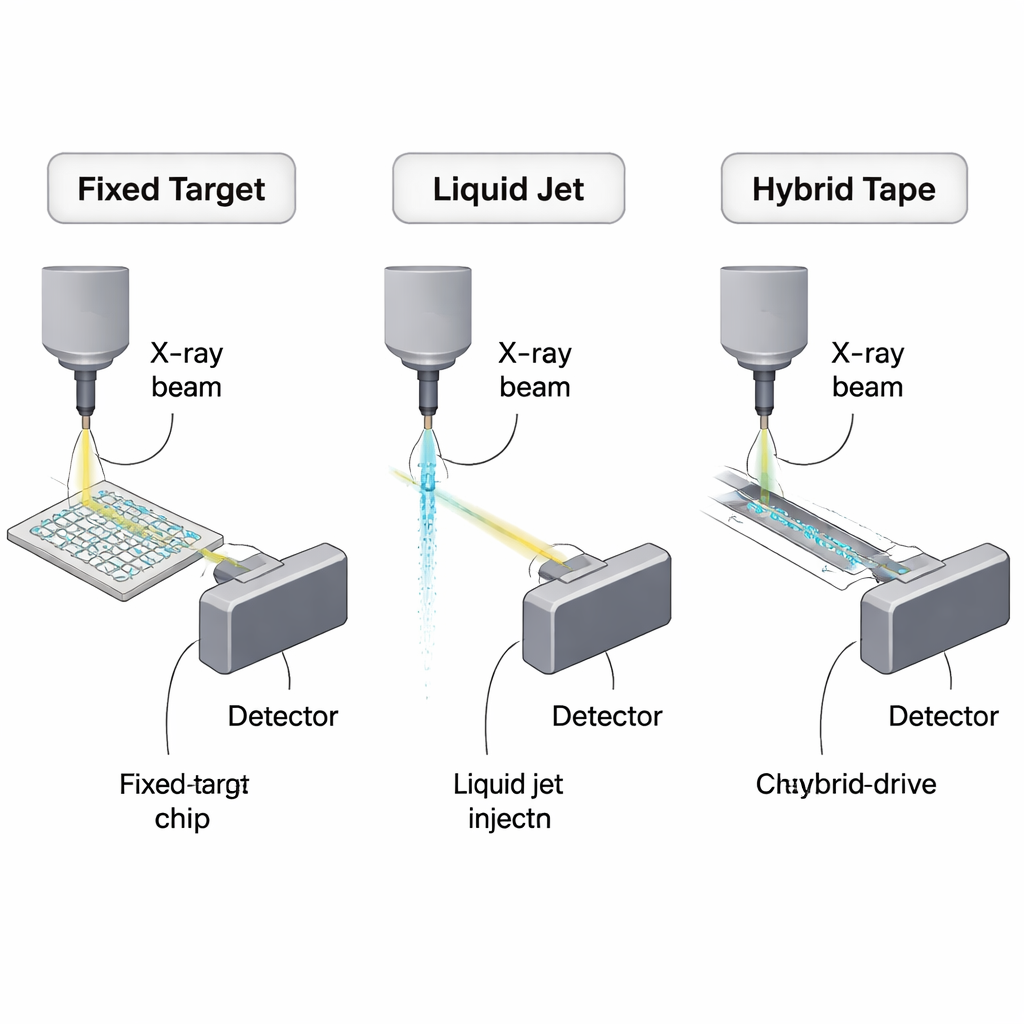
Por que a cristalografia serial precisa de melhores métodos de entrega
A cristalografia tradicional baseava‑se em um único cristal grande rotacionado em um feixe de raios X. A cristalografia serial inverte o roteiro: em vez de um cristal grande, milhares de microcristais, cada um usado apenas uma vez, são projetados ou varridos por pulsos ultrabrilhantes de raios X de sincrotrons ou lasers de elétrons livres de raios X (XFELs). Isso possibilita coleta de dados em temperatura ambiente e “instantâneos” rápidos de reações químicas, mas também significa repor cristais constantemente em taxas que acompanhem trens de pulsos que podem chegar a milhões de pulsos por segundo. Grande parte da suspensão de cristais nunca chega ao feixe e é descartada, portanto reduzir o consumo de amostra tornou‑se um desafio técnico e econômico central para a área.
Alvos fixos: pequenos chips que aproveitam cada gota
Uma estratégia importante é imobilizar microcristais em pequenos suportes sólidos chamados alvos fixos. Em vez de pulverizar cristais pelo feixe, pesquisadores os organizam em matrizes sobre chips de silício ou polímero e movem o chip de modo que cada cristal seja trazido uma vez ao foco dos raios X. No melhor experimento mental, cerca de 10.000 microcristais de uma proteína modelo poderiam, em princípio, fornecer um conjunto de dados completo usando apenas cerca de 450 nanogramas de proteína. Dispositivos reais ainda não são tão econômicos, mas já reduzem as necessidades para dezenas de microgramas até alguns décimos de miligrama — ordens de grandeza melhores que os primeiros experimentos seriais. A revisão compara malhas de silício, filmes poliméricos ultrafinos e chips plásticos multicamada, pesando suas forças (baixo espalhamento de fundo, crescimento de cristal no chip, compatibilidade com estudos em temperatura ambiente) contra problemas práticos como desidratação, espalhamento indesejado do material do chip e volume “morto” extra introduzido por pipetagem manual.
Jatos líquidos e correntes viscosas: rápidos, mas esfomeados
Outra família de métodos mantém os cristais suspensos em líquido e os entrega continuamente através do feixe. Bicos virtuais gasodinâmicos criam jatos finíssimos que acompanham trens de pulsos rápidos de XFEL, tornando‑se uma ferramenta de trabalho para estudos temporais e experimentos de mistura‑e‑injeção onde reações são disparadas por mistura rápida pouco antes da exposição. No entanto, como os jatos funcionam continuamente, a maior parte do fluxo nunca encontra um pulso de raios X. Mesmo com afinação cuidadosa, experimentos práticos consomem muito mais proteína que o mínimo teórico — tipicamente dezenas a centenas de microlitros de suspensão concentrada de cristais. Para amenizar o problema, pesquisadores desenvolveram designs mais eficientes, como bicos de fluxo duplo que revestem o fluxo de cristais com um líquido sacrificial, injetores por eletrofiação “MESH” que operam em taxas de fluxo mais baixas, e extrusoras de alta viscosidade que empurram cristais embebidos em géis ou fases cúbicas lipídicas a microlitros por minuto ou menos. Esses métodos viscosos são especialmente valiosos para proteínas de membrana frágeis e para estudos em temperatura ambiente em sincrotrons, mas seus fluxos mais espessos aumentam o espalhamento de fundo e são menos adequados às fontes de raios X mais rápidas.
Gotas, fitas e híbridos: casando pulsos um a um
Uma terceira classe, cada vez mais criativa, de abordagens “híbridas” combina suportes sólidos com entrega controlada de líquidos ou gotas. Sistemas com fita transportadora, por exemplo, depositam gotas ou faixas líquidas finas sobre um filme polimérico móvel que passa pelo feixe; sincronizar o movimento permite sondar etapas de reação ou exposição a gases em atrasos definidos. Sistemas de gota sob demanda vão mais além, usando dispositivos acústicos ou piezoelétricos para ejetar gotas de nanolitro ou até picolitro apenas quando um pulso de raios X é esperado, reduzindo dramaticamente o desperdício. Alguns designs misturam uma gota de ligante em uma gota pré‑posicionada contendo cristais na fita pouco antes de ela alcançar o feixe, permitindo enzimologia temporal com reagentes cuidadosamente racionados. Outros híbridos, como o método LAMA em chip, adicionam gotículas minúsculas de substrato diretamente sobre cristais pré‑montados em chips de alvo fixo. Entre esses designs, o uso relatado de proteína varia amplamente — de níveis próximos ao miligrama até alguns miligramas para séries temporais completas — mostrando tanto a promessa quanto os atuais desafios de engenharia para sincronizar gotas, cristais e pulsos de raios X.
Quão próximos estamos do mínimo teórico?
Ao comparar dezenas de experimentos publicados em alvos fixos, injetores líquidos e sistemas híbridos, os autores mostram que nenhum método existente chega perto do marco ideal de 450 nanogramas; mesmo os melhores dispositivos ainda ultrapassam em cerca de duas ordens de magnitude. Ainda assim, surgem tendências claras. Alvos fixos tipicamente usam menos proteína e são atrativos sempre que a mistura temporal não é essencial ou pode ser projetada no chip. Jatos líquidos ainda dominam os estudos XFEL temporais mais exigentes, mas continuam intensivos em amostra, especialmente quando muitos pontos temporais são necessários. Esquemas híbridos de gotas e fita oferecem algumas das maiores economias relativas, sobretudo quando o tempo das gotas é rigidamente sincronizado com a fonte de raios X. Olhando à frente, o artigo argumenta que novos avanços virão de melhor controle microfluídico, automação para eliminar etapas de manipulação desperdiçadoras, e do uso de fontes compactas de raios X e otimização orientada por dados para co‑projetar experimentos e sistemas de entrega que aproximem cada vez mais o uso de proteína do limite teórico.
Citação: Manna, A., Doppler, D., Sripati, M.P. et al. Sample delivery methods for protein X-ray crystallography with a special focus on sample consumption. Nat Commun 16, 9856 (2025). https://doi.org/10.1038/s41467-025-65173-5
Palavras-chave: cristalografia serial, cristalografia de raios X de proteínas, entrega de amostras, laser de elétrons livres de raios X, microfluídica