Clear Sky Science · pt
Redução de RAD23A prolonga a vida e mitiga a patologia em um modelo murino de proteinopatia TDP-43
Por que esta pesquisa importa para famílias e pacientes
Muitas formas de demência e doenças dos neurônios motores, incluindo esclerose lateral amiotrófica (ELA) e demência frontotemporal (DFT), envolvem proteínas nas células cerebrais que se dobram incorretamente, se agregam e lentamente envenenam os neurônios. Um dos culpados principais é uma proteína chamada TDP-43, que normalmente ajuda a gerenciar o RNA, mas torna-se tóxica quando se agrega. Este estudo faz uma pergunta promissora: podemos tornar as células cerebrais mais resilientes reduzindo outra proteína, RAD23A, que ajuda a controlar como proteínas danificadas são tratadas? Os autores mostram em camundongos que diminuir RAD23A pode prolongar a vida, melhorar o movimento e reduzir danos cerebrais em um modelo de doença impulsionada por TDP-43, sugerindo uma nova estratégia terapêutica.
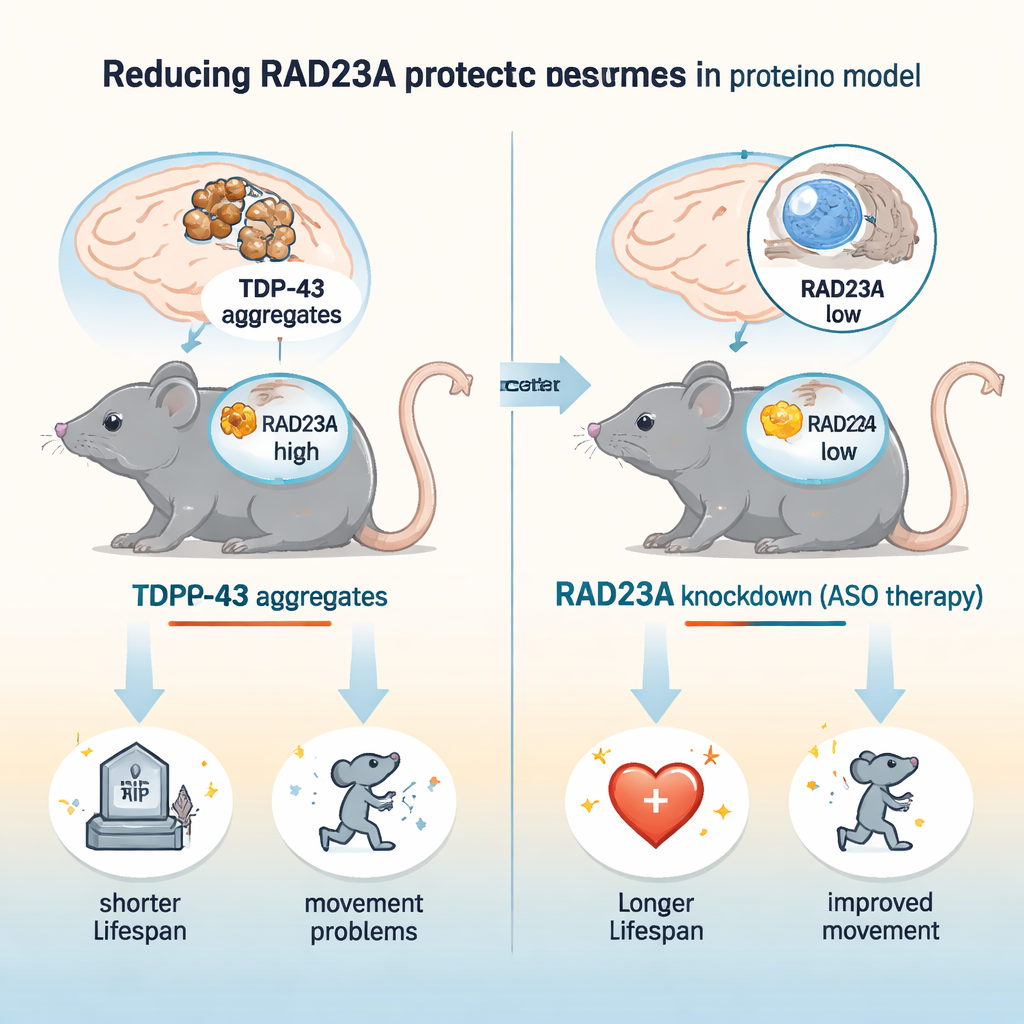
Um engarrafamento de trânsito proteico em neurônios doentes
Doenças neurodegenerativas costumam ser marcadas por acúmulos de proteínas mal dobradas que a maquinaria de descarte da célula não consegue eliminar. Na ELA e na DFT, o TDP-43 sai do núcleo, forma aglomerados pegajosos e fica fortemente marcado com ubiquitina, um sinal que normalmente direciona proteínas para o proteassomo, o principal triturador da célula. RAD23A é uma das várias proteínas “transporte” que podem levar cargas marcadas com ubiquitina ao proteassomo. Ainda assim, trabalhos anteriores em vermes e neurônios em cultura sugeriram que a perda de proteínas semelhantes a RAD23 poderia, na verdade, proteger contra o dano induzido por TDP-43 — um paradoxo que este estudo procurou explorar em um cérebro mamífero vivo.
Reduzindo RAD23A em um modelo murino de TDP-43
Os pesquisadores usaram um modelo murino bem estabelecido, chamado TAR4/4, que superexpressa TDP-43 humano em neurônios e desenvolve problemas de movimento, curvatura da coluna, tremor e morte precoce, espelhando características-chave da ELA/DFT. Eles reduziram RAD23A de duas maneiras: injetando filhotes com oligonucleotídeos antissenso (ASOs) que diminuem o RNA de Rad23a, e cruzando camundongos que carregam um knockout genético de Rad23a. Um único tratamento com ASO cortou os níveis de RAD23A no cérebro e na medula espinhal em cerca de três quartos. Nesses camundongos TDP-43, a redução de RAD23A prolongou a vida em aproximadamente 50% e atrasou o início e a gravidade de problemas de marcha, tremor, curvatura da coluna e o chamado clasping dos membros posteriores. Curiosamente, a perda genética completa de RAD23A não adicionou benefício adicional, sugerindo que a redução parcial é ideal e que a ausência total a longo prazo pode desencadear mudanças compensatórias.
Menos inflamação, manejo proteico mais limpo e um genoma mais calmo
Exames microscópicos do córtex motor mostraram que os camundongos TDP-43 perderam neurônios e desenvolveram forte ativação de astrócitos e microglia, células de suporte e imunes do cérebro. A redução de RAD23A preservou o número de neurônios e diminuiu marcadores de inflamação e morte celular. Análises bioquímicas revelaram que a superprodução de TDP-43 inundou as células com proteínas marcadas por ubiquitina e insolúveis em detergente, e arrastou subunidades do proteassomo para esses agregados, enfraquecendo a capacidade da célula de eliminar proteínas danificadas. Reduzir RAD23A diminuiu a carga total de proteínas ubiquitinadas, manteve mais proteassomos na fração solúvel e funcional, e restaurou vários tipos de atividade do proteassomo em direção ao normal. Ao mesmo tempo, a redução de RAD23A diminuiu tanto as formas totais quanto as agregadas de TDP-43, incluindo um fragmento particularmente tóxico de 25 quilodaltons, e deslocou o TDP-43 do citoplasma de volta ao núcleo. O sequenciamento de RNA em escala genômica mostrou que milhares de mudanças na expressão gênica induzidas por TDP-43 foram parcialmente revertidas quando RAD23A foi reduzido, especialmente genes envolvidos na função neuronal, produção de energia mitocondrial e vias de limpeza de agregados, como a aggrephagy.
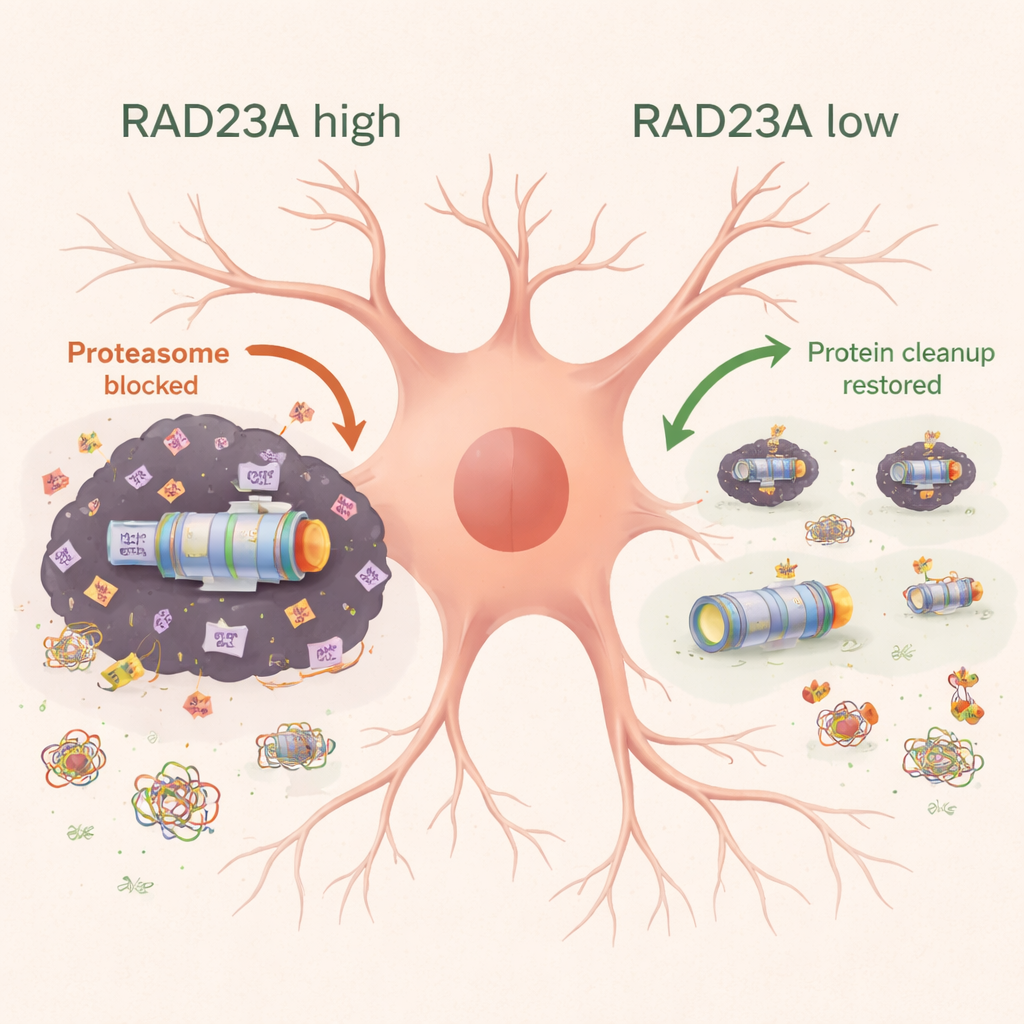
Remodelando o proteoma “insolúvel” oculto
Para examinar mais de perto os agregados persistentes que resistem a detergentes normais, a equipe usou espectrometria de massa com isótopos pesados para catalogar proteínas aprisionadas na fração insolúvel do córtex de camundongo. A expressão de TDP-43 humano atraiu componentes do proteassomo, proteínas do citoesqueleto e de transporte, e outras máquinas celulares. Quando RAD23A foi reduzido, a composição geral desse proteoma insolúvel mudou: menos proteínas relacionadas ao proteassomo e ao transporte foram sequestradas, enquanto algumas proteínas ribossomais e relacionadas ao estresse aumentaram nos agregados. Notavelmente, essa remodelação não refletiu simplesmente mudanças nos níveis de RNA, sugerindo que RAD23A influencia principalmente como proteínas existentes são repartidas entre estados solúveis e agregados, em vez de quanto de cada proteína é sintetizado.
O que isso pode significar para terapias futuras
Em conjunto, esses achados colocam RAD23A como um potente regulador da qualidade proteica em neurônios sob estresse. Ao reduzir parcialmente RAD23A em um modelo murino impulsionado por TDP-43, os autores conseguiram reduzir aglomerados proteicos tóxicos, restaurar a atividade da maquinaria de descarte proteico, silenciar mudanças deletérias na expressão gênica, limitar a inflamação cerebral e prolongar a vida e a função motora. Como o acúmulo anormal de TDP-43 é amplo em formas hereditárias e esporádicas de ELA, DFT e transtornos relacionados, direcionar RAD23A com fármacos antissenso compatíveis com humanos pode oferecer uma maneira de proteger neurônios sem bloquear diretamente o TDP-43, uma proteína essencial. Embora muito ainda precise ser testado em outros modelos e em humanos, este trabalho identifica RAD23A como uma nova e promissora alavanca em uma via comum da neurodegeneração.
Citação: Guo, X., Prajapati, R.S., Chun, J. et al. Reduction of RAD23A extends lifespan and mitigates pathology in a mouse model of TDP-43 proteinopathy. Nat Commun 17, 1820 (2026). https://doi.org/10.1038/s41467-025-65104-4
Palavras-chave: TDP-43, ELA, agregação de proteínas, proteassomo, terapia antisense