Clear Sky Science · pt
Histologia óptica de super-resolução de amostras fixadas em formalina e incluídas em parafina: desafios e oportunidades
Ver Mais em Amostras de Tecidos Conservadas
Hospitais em todo o mundo preservam finas fatias de órgãos de pacientes em blocos de cera para que doenças como câncer ou lesão renal possam ser estudadas por muitos anos. Este artigo de revisão explica como novos tipos de microscópios ópticos estão transformando essas amostras rotineiras em janelas poderosas para a doença, revelando detalhes muito menores do que os visíveis em microscópios hospitalares padrão. Esses avanços podem ajudar médicos a detectar enfermidades mais cedo, entender sua progressão e personalizar tratamentos com maior precisão.
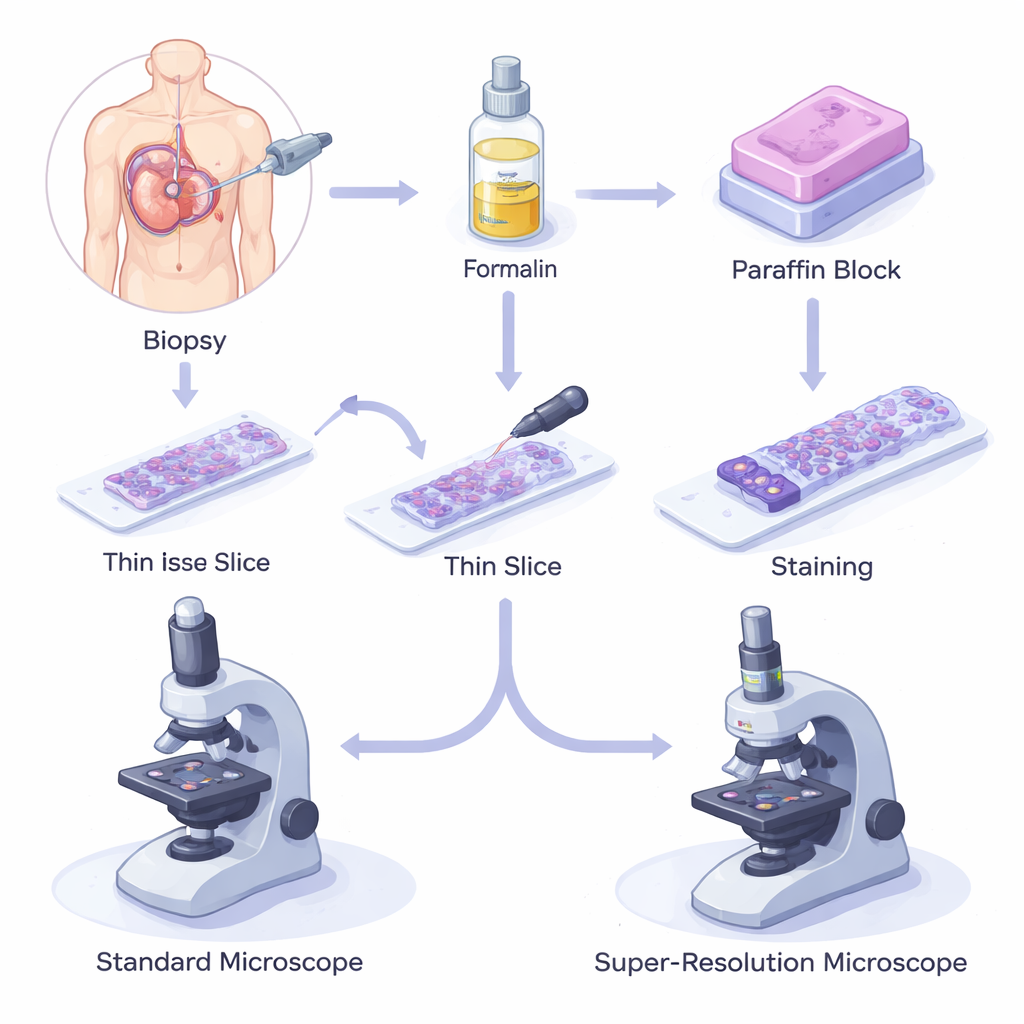
Como Tecidos Preservados em Cera Impulsionam a Medicina Moderna
Quando um paciente passa por uma biópsia, um pequeno pedaço de tecido é removido, fixado em uma substância chamada formalina para impedir a degradação e então incluído em parafina. O bloco é cortado em seções tão finas quanto um fio de cabelo, colocadas em lâminas de vidro, coradas e examinadas ao microscópio óptico. O método de fixação em formalina e inclusão em parafina (FFPE) é barato, confiável e pode preservar amostras por décadas à temperatura ambiente. Como resultado, milhões de amostras FFPE estão armazenadas em biobancos ao redor do mundo, sustentando desde pesquisas básicas em biologia até estudos avançados de genética e proteínas, e formando a espinha dorsal do diagnóstico e prognóstico modernos.
Por Que Microscópios Comuns Já Não Bastam
Microscópios ópticos tradicionais são limitados pela física da luz: detalhes menores que cerca de 250 nanômetros se tornam indistintos. Muitas estruturas relacionadas a doenças — como os filtros finos nos rins, as conexões entre neurônios ou pequenas alterações na arquitetura do DNA dentro do núcleo — estão abaixo desse limite. O fluxo de trabalho atual frequentemente combina microscopia óptica padrão para visão geral com microscopia eletrônica para detalhes na escala nanométrica, mas essa abordagem é lenta, cara e exige preparação de amostras totalmente diferente. Clínicos e pesquisadores buscam, portanto, um sistema único e flexível que possa escanear grandes áreas rapidamente e também ampliar para ver características em escala nanométrica nas mesmas seções FFPE que já utilizam.
Novas Maneiras de Afiar a Visão
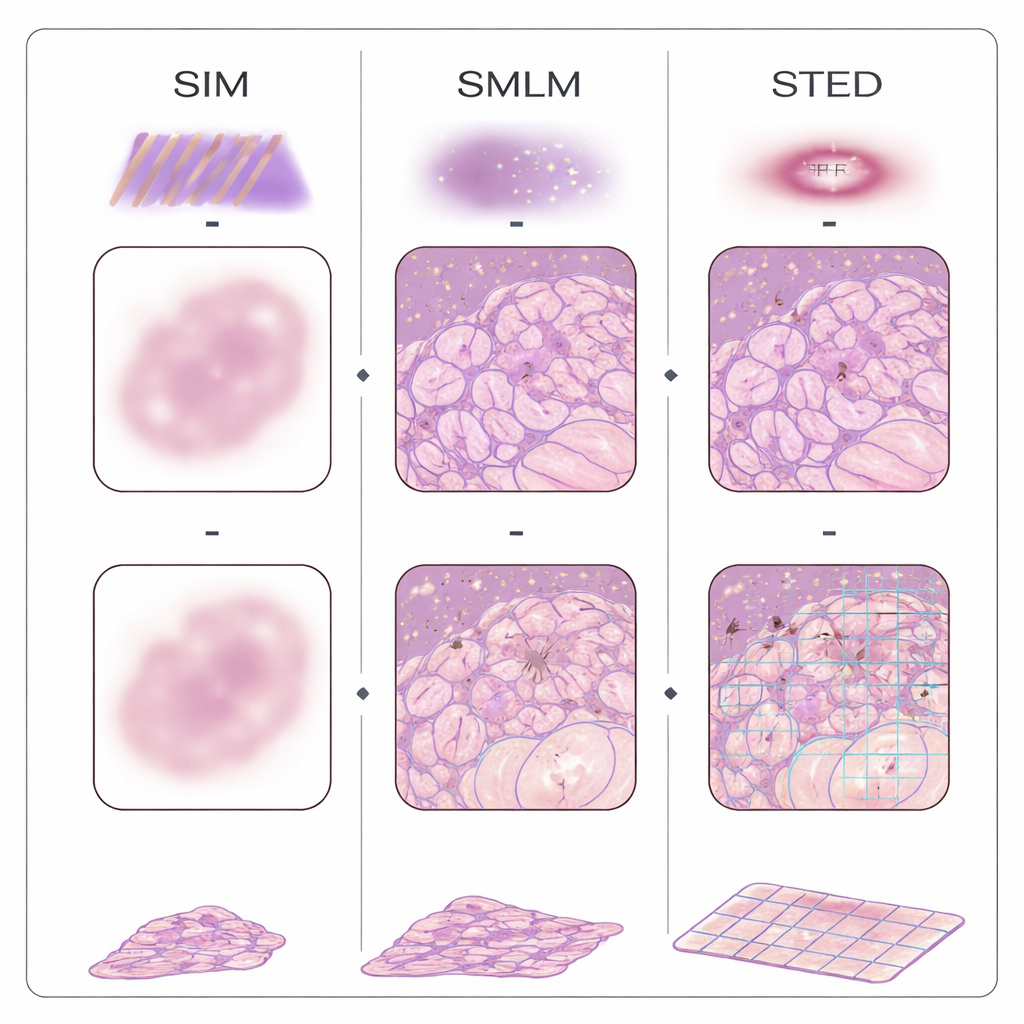
Nas últimas duas décadas, várias famílias de microscópios de “super-resolução” romperam a barreira tradicional de resolução usando marcadores fluorescentes e truques ópticos. Métodos de localização de moléculas únicas alternam entre ligar e desligar moléculas e determinam suas posições uma a uma; a iluminação estruturada projeta padrões de luz listrados sobre o tecido e usa computação para recuperar detalhes mais finos; a depleção por emissão estimulada (STED) talha um ponto emissor minúsculo usando um feixe em forma de donut; e abordagens baseadas em flutuação analisam cintilações sutis na imagem para inferir estrutura. Uma estratégia diferente, chamada microscopia de expansão, evita óptica complexa inchando fisicamente o tecido em um gel, de modo que microscópios comuns possam ver detalhes antes invisíveis. Esses métodos já foram aplicados a amostras FFPE de mama, cólon, pâncreas, rim, cérebro, pele, placenta e outros órgãos, revelando como as mitocôndrias mudam em tumores, como os filtros renais falham e como agregados de proteínas se formam na doença de Alzheimer.
Obstáculos no Caminho para o Uso Cotidiano
Apesar de promissoras, essas técnicas ainda não estão prontas para se tornar ferramentas rotineiras na maioria dos laboratórios de patologia. Muitos sistemas de super-resolução são lentos, cobrem apenas campos de visão muito pequenos ou exigem dezenas de milhares de imagens para construir uma única imagem de alta definição, o que é impraticável quando um patologista precisa avaliar grandes áreas de tecido. Os próprios tecidos FFPE são opticamente desafiadores: dispersam a luz, apresentam autofluorescência e podem esconder as moléculas que precisam ser marcadas, tudo isso podendo gerar imagens borradas ou estruturas falsas. Alguns métodos demandam corantes especiais, tampões personalizados ou tratamentos químicos em vários passos que não se encaixam facilmente nos fluxos de trabalho histológicos padrão. Além disso, instrumentos comerciais são caros e complexos de operar, e os dados resultantes exigem processamento computacional intensivo e grande capacidade de armazenamento.
Unindo Óptica Inteligente e Software Inteligente
Para superar esses obstáculos, pesquisadores estão combinando óptica aprimorada com imagem sem marcação e inteligência artificial. Métodos de alto rendimento, limitados pela difração, como ptychografia de Fourier e microscopia óptica não linear podem escanear rapidamente grandes seções FFPE, mesmo não coradas, e fornecer mapas quantitativos da estrutura tecidual. Plataformas de patologia digital agora capturam lâminas inteiras em alta resolução e usam aprendizado de máquina para detectar tumores e pontuar biomarcadores como HER2, Ki-67 e PD-L1. Modelos de deep learning podem até transformar imagens de baixa resolução em vistas de super-resolução, potencialmente reduzindo a necessidade de algum hardware especializado enquanto aproveitam melhor os arquivos de biópsias existentes.
O Que Isso Significa para Pacientes Futuros
Os autores concluem que a verdadeira “histologia de super-resolução” de amostras FFPE — combinando detalhe em escala nanométrica, alta velocidade, custo razoável e compatibilidade com rotinas de laboratório atuais — ainda não foi plenamente alcançada, mas está ao alcance. À medida que métodos ópticos se tornarem mais rápidos e robustos, e à medida que a análise baseada em IA amadurecer, essas ferramentas poderão revelar mudanças sutis e precoces em tecidos que hoje passam despercebidas, melhorar a precisão dos diagnósticos e orientar decisões de tratamento mais personalizadas. A longo prazo, transformar cada bloco de cera arquivado em um mapa de alta definição da doença poderia transformar tanto a pesquisa quanto o atendimento clínico.
Citação: Villegas-Hernández, L.E., Dubey, V.K., Acharya, G. et al. Optical super-resolution histology of formalin-fixed paraffin-embedded tissue samples: challenges and opportunities. Nat Commun 16, 9760 (2025). https://doi.org/10.1038/s41467-025-64626-1
Palavras-chave: microscopia de super-resolução, tecido FFPE, patologia digital, imagem óptica, diagnóstico do câncer