Clear Sky Science · pt
Nanoenzimas expandindo os limites da biocatálise
Pequenos ajudantes que aceleram a química
Desde a fabricação de cerveja até a digestão do jantar, nossas vidas dependem de ajudantes invisíveis chamados catalisadores, que fazem as reações químicas ocorrerem mais rapidamente. Por mais de um século, os catalisadores da biologia foram considerados apenas proteínas frágeis e, mais tarde, RNA catalítico. Esta revisão apresenta as “nanoenzimas” – minúsculas partículas projetadas que se comportam como enzimas, mas são feitas de materiais robustos como metais, óxidos e carbono. Elas suportam calor, frio e condições agressivas, e começam a remodelar a forma como pensamos sobre a química em sistemas vivos, doenças, indústria e até a origem da vida.
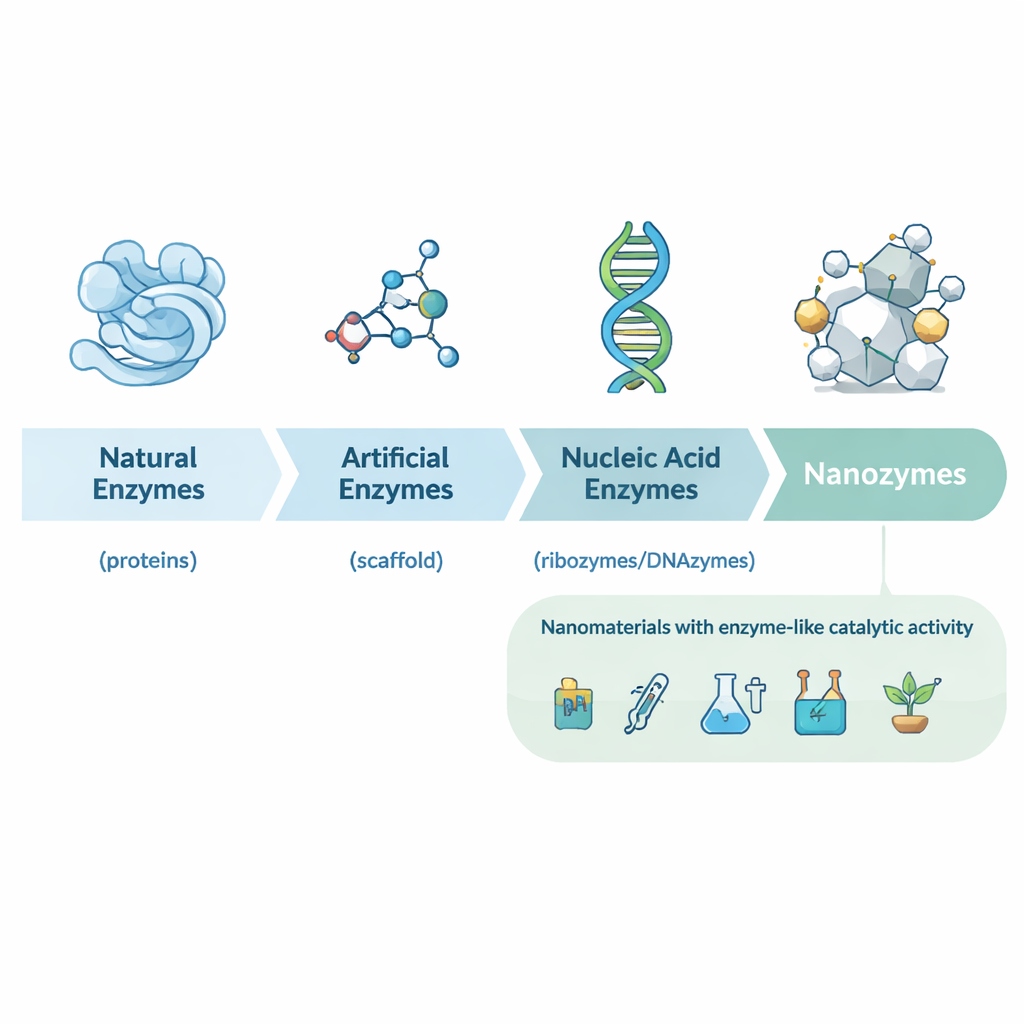
Das enzimas naturais aos nanocatalisadores projetados
O artigo percorre primeiro a história da biocatálise, desde as descobertas iniciais de enzimas proteicas em leveduras e sucos gástricos até os ribozimas (RNA catalítico) e uma ampla gama de enzimas artificiais construídas a partir de pequenas moléculas e anticorpos. Esses catalisadores tradicionais são poderosos, mas frequentemente caros, instáveis e difíceis de produzir em larga escala. No início dos anos 2000, pesquisadores descobriram que alguns nanomateriais – por exemplo, nanopartículas de óxido de ferro – podiam imitar o comportamento de enzimas clássicas como a peroxidase de rábano. Isso levou ao conceito de nanoenzimas: partículas na escala nanométrica cuja própria estrutura lhes confere atividade semelhante à de enzimas, em vez de depender de proteínas ou catalisadores de pequena molécula ligados à superfície.
O que torna as nanoenzimas diferentes
Diferentemente das enzimas, que possuem um único bolso ativo com forma precisa, as nanoenzimas expõem muitos pontos ativos em suas superfícies. Esses pontos podem estar em arestas cristalinas, defeitos ou interfaces entre dois materiais, e coletivamente podem processar muitas moléculas ao mesmo tempo. Um único sítio ativo em uma nanoenzima costuma ser menos eficiente que o de uma enzima, mas uma nanopartícula pode abrigar milhares desses sítios, de modo que seu poder catalítico total pode rivalizar ou até superar o de enzimas naturais. Sua atividade também pode ser ajustada alterando tamanho, forma, dopagem química e revestimentos de superfície – como ajustar a arquitetura e o cabeamento de uma máquina minúscula. Por serem feitos de sólidos robustos em vez de proteínas dobradas e delicadas, as nanoenzimas continuam funcionando em altas temperaturas, baixas temperaturas ou altos níveis de sal que rapidamente inativariam a maioria das enzimas.
Como as nanoenzimas funcionam e como são medidas
Os autores mostram que as nanoenzimas frequentemente seguem as mesmas regras cinéticas básicas que os bioquímicos usam para enzimas, como o comportamento de Michaelis–Menten, em que a velocidade da reação depende de quão facilmente um catalisador se liga e converte seu substrato. Mas há reviravoltas importantes. Uma partícula pode abrigar múltiplos tipos de sítios ativos, de modo que uma única nanoenzima pode realizar reações diferentes ou até conflitantes, como tanto produzir quanto destruir espécies reativas de oxigênio. Isso pode gerar curvas cinéticas complexas “fora do livro didático” que escondem múltiplos processos sob uma tendência suave. A revisão explica como os pesquisadores dissecam esses comportamentos, estimam quantos sítios ativos realmente existem e comparam a atividade geral de diferentes nanoenzimas usando unidades padronizadas, tudo isso crucial para transformar um material intrigante em uma ferramenta confiável.
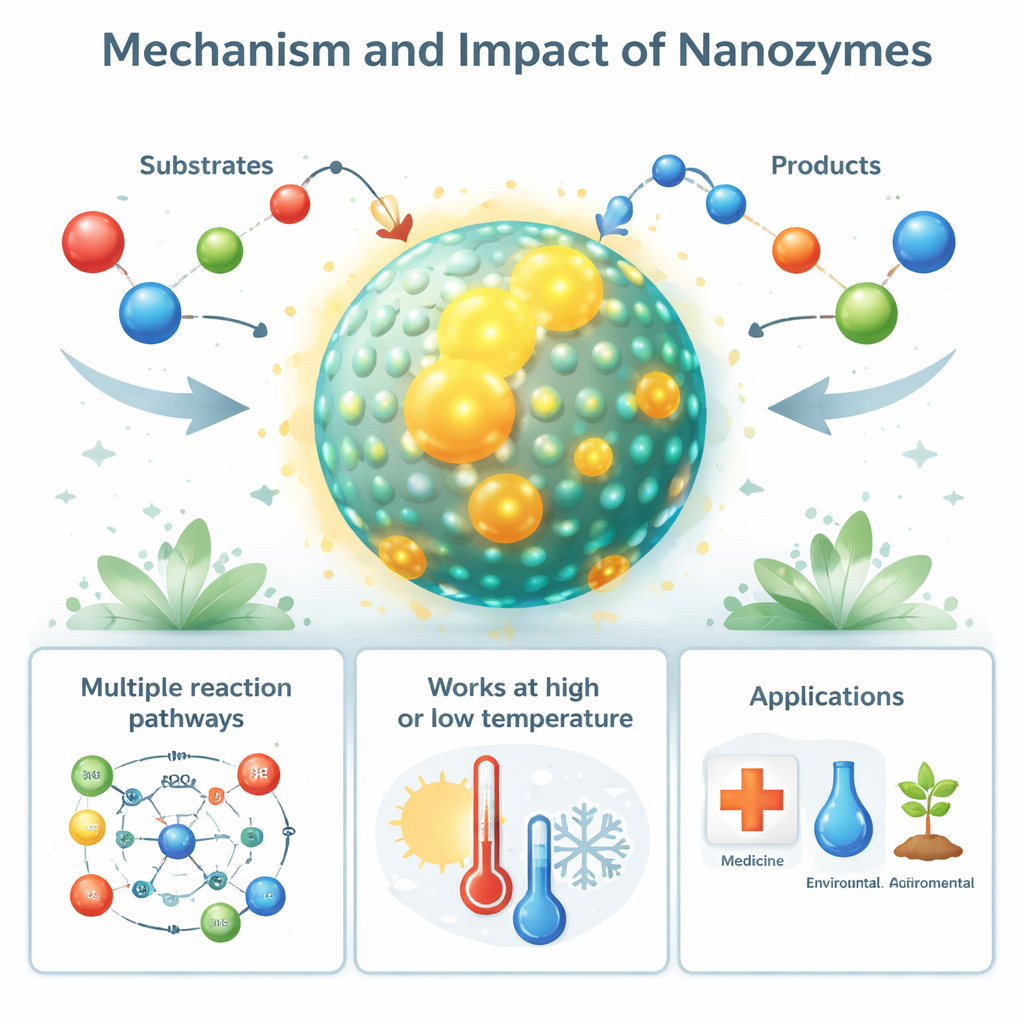
De nanoenzimas naturais a usos no mundo real
Curiosamente, o comportamento semelhante ao de nanoenzimas não se limita ao laboratório. Certas nanostruturas biológicas, como gaiolas proteicas preenchidas com ferro (ferritina) e partículas magnéticas em bactérias (magnetossomos), atuam como nanoenzimas naturais que ajudam a controlar espécies reativas de oxigênio nocivas. Mesmo fibras proteicas relacionadas a doenças, como depósitos de amiloide na doença de Alzheimer, podem adotar atividade peroxidase semelhante à de nanoenzimas e danificar células próximas. Na aplicação prática, nanoenzimas sintéticas estão sendo usadas como substitutos mais baratos e resistentes de enzimas em testes diagnósticos, biossensores e ensaios industriais. Sua capacidade de gerar ou remover espécies reativas de oxigênio está sendo aproveitada para matar células tumorais e bactérias, proteger tecidos do estresse oxidativo e ajudar culturas a resistir à seca, salinidade e poluição.
Projetando a próxima geração de catalisadores inteligentes
Olhando para o futuro, os autores destacam desafios-chave: identificar as estruturas atômicas exatas que atuam como sítios ativos, melhorar a seletividade das reações para que as nanoenzimas atuem apenas onde e quando desejado, e garantir segurança e estabilidade no interior do corpo. Apontam para imagens avançadas, simulações em nível quântico e aprendizado de máquina como ferramentas poderosas para prever e otimizar o desempenho das nanoenzimas. Como as nanoenzimas podem operar em condições extremas, responder à luz, calor, som ou campos magnéticos e, às vezes, realizar várias reações em sequência, elas podem sustentar novas terapias, tecnologias ambientais e processos industriais. A revisão conclui que as nanoenzimas ampliam a própria definição de biocatálise e podem até oferecer pistas sobre como catalisadores primitivos alimentaram a química da vida precoce.
Citação: Zhang, R., Yan, X., Gao, L. et al. Nanozymes expanding the boundaries of biocatalysis. Nat Commun 16, 6817 (2025). https://doi.org/10.1038/s41467-025-62063-8
Palavras-chave: nanoenzimas, biocatálise, nanopartículas, imitações de enzimas, espécies reativas de oxigênio