Clear Sky Science · pt
Combinando transcriptômica espacial com morfologia tecidual
Observando Tecidos de Duas Maneiras Diferentes
Médicos e cientistas cada vez mais querem saber não apenas quais genes estão ativos em um tecido, mas exatamente onde eles são ativados. Ao mesmo tempo, os microscópios hospitalares já capturam imagens ricas da estrutura tecidual que os patologistas usam diariamente. Este artigo explica como um novo campo busca conectar essas duas visões — mapas detalhados da atividade gênica e imagens comuns de microscópio — e por que essa união pode levar a diagnósticos mais precoces, melhor graduação do câncer e um entendimento mais profundo de como as doenças se desenvolvem e se espalham.
De Células Dispersas a Mapas de Atividade Gênica
Por anos, métodos poderosos de “ômica” exigiam que os tecidos fossem triturados até virar uma mistura de células individuais, o que destruía a informação sobre onde cada célula se originava. A transcriptômica espacial mudou isso ao medir a atividade gênica mantendo a posição de cada célula no tecido. O resultado é uma grade de pontos, cada um com um perfil de expressão gênica e coordenadas precisas. Por si só, esses dados genômicos espaciais já revelaram novos padrões de diversidade celular e arquitetura da doença. Mas eles não mudam depois de medidos, e repetir o experimento é caro. Em contraste, imagens de tecido coradas com corantes padrão, como a amplamente usada hematoxilina e eosina (H&E), são baratas e abundantes, e contêm pistas visuais sobre forma celular, densidade e organização tecidual.
Duas Maneiras de Combinar Imagens e Genes
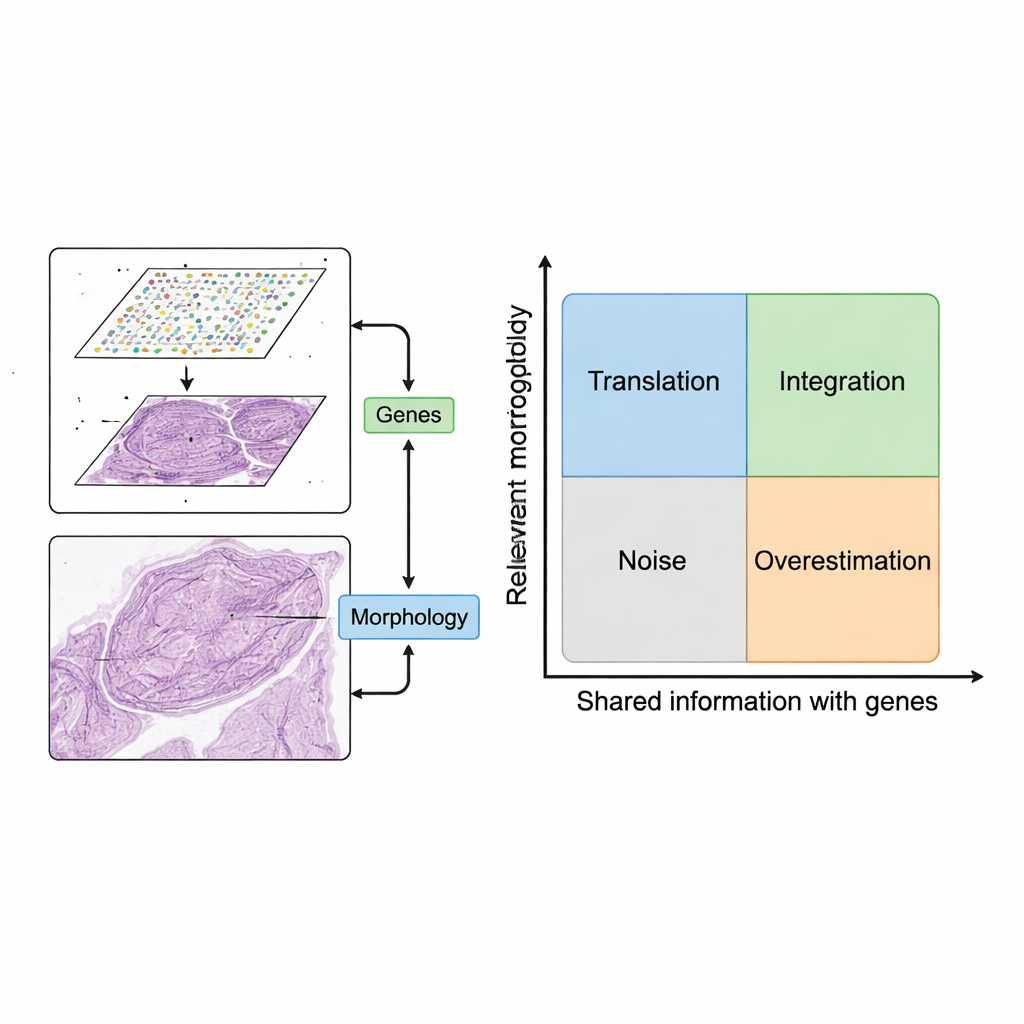
A revisão propõe um quadro simples, porém poderoso, para usar essas duas fontes de dados em conjunto. Primeiro, patches da imagem são pareados com pontos de expressão gênica próximos. Em seguida, modelos computacionais extraem características das imagens — padrões que capturam forma, textura e organização — e os comparam com padrões na expressão gênica. Os autores descrevem dois cenários desejáveis. Na “tradução”, as características da imagem acompanham de perto a atividade gênica relevante, permitindo que modelos prevejam quais genes estão ativos usando apenas a imagem do tecido. Isso pode ser usado para preencher medições gênicas faltantes, alcançar resolução mais fina que a grade original ou inferir atividade gênica a partir de lâminas clínicas rotineiras sem trabalho laboratorial adicional. Na “integração”, as características da imagem capturam informações úteis que os dados gênicos deixam passar, como mudanças estruturais lentas ou organização tecidual sutil, ajudando a definir regiões ou “domínios” mais claros dentro de um tecido.
Quando Informação Extra Ajuda — e Quando Atrapalha
Nem toda característica de imagem vale a pena ser usada. Os autores introduzem um mapa conceitual com dois eixos: quão relevante é uma característica de imagem para a questão biológica e quanto ela se sobrepõe à informação gênica. Características que não são relevantes nem relacionadas aos genes equivalem a ruído, como artefatos de coloração. Características que acompanham padrões gênicos, mas estão ligadas a genes não importantes (como genes de manutenção básicos), podem fazer modelos parecerem bons no papel, enquanto acrescentam pouco valor clínico. Ao organizar métodos em quatro quadrantes — tradução, integração, ruído e superestimação — o quadro esclarece quando combinar imagens e genes realmente adiciona insights e quando apenas repete ou obscurece o que já se sabe.
Ferramentas Atuais, Testes e Dores do Crescimento
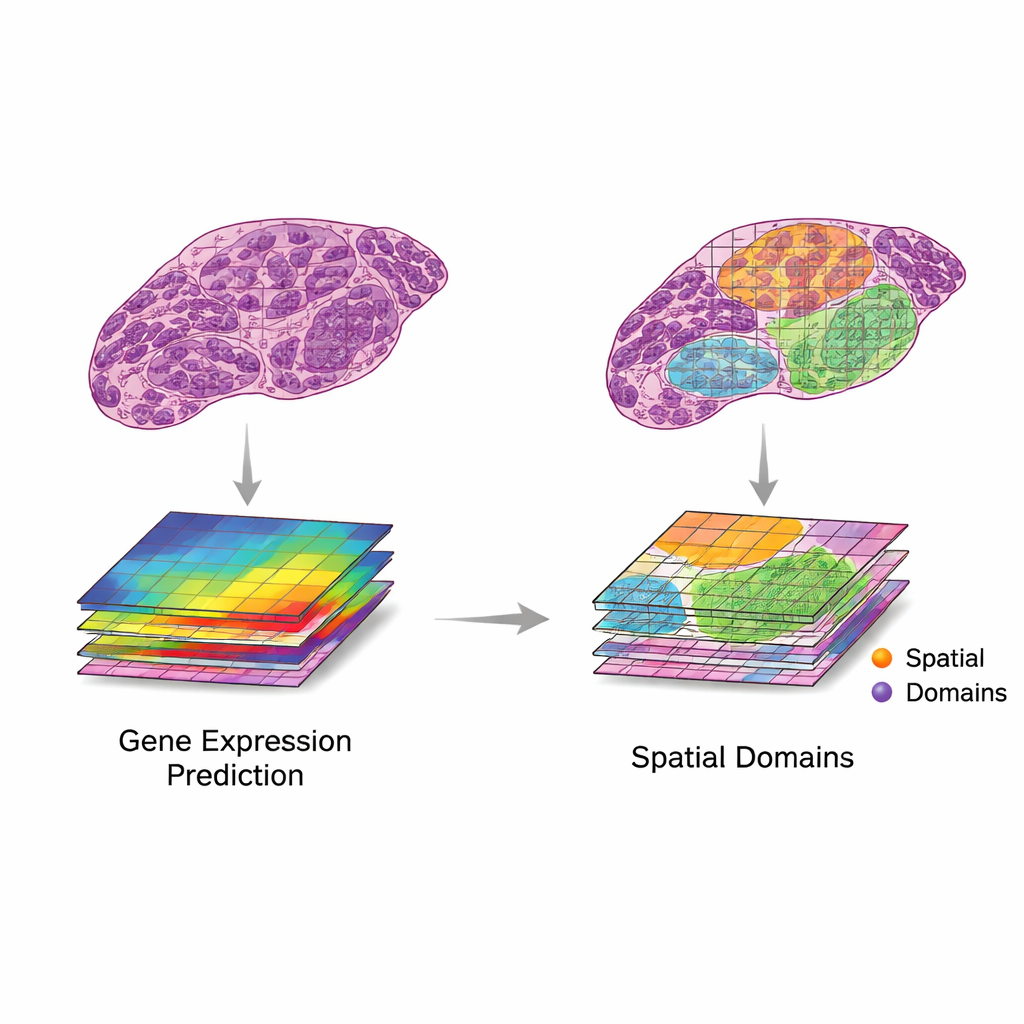
Uma onda rápida de métodos de inteligência artificial agora tenta realizar tradução e integração em dados reais. Sistemas iniciais dependiam de redes neurais convolucionais, enquanto os mais recentes usam transformers, redes neurais de grafos e modelos multiescala que podem capturar detalhes desde pequenas estruturas celulares até o contexto da lâmina inteira. Esses métodos têm sido usados para prever atividade gênica a partir de imagens H&E, gerar mapas de super‑resolução e ajudar a identificar regiões teciduais com comportamento distinto. Para avaliar desempenho, os pesquisadores dependem de medidas estatísticas, como correlação entre níveis gênicos previstos e observados, ou concordância entre regiões definidas pela IA e rótulos de patologistas especialistas. Entretanto, os conjuntos de dados ainda são pequenos e variados, e a comparação entre estudos é difícil. Muitos ganhos relatados podem refletir sobreajuste ou sucesso em genes e padrões que têm pouca importância clínica.
Para Onde Isso Pode Levar
Os autores concluem que combinar mapas gênicos espaciais com imagens de tecido é um empreendimento promissor, mas ainda em estágio inicial. Os modelos atuais frequentemente atingem apenas precisão moderada e ainda não se mostraram prontos para uso médico rotineiro. O progresso futuro provavelmente virá de melhores características de imagem, especialmente grandes “modelos fundacionais” treinados em milhões de lâminas de patologia, e de foco em genes e padrões que realmente influenciam o cuidado ao paciente. Integrações cuidadosamente desenhadas poderiam um dia revelar sinais precoces de doença ao detectar discrepâncias entre a aparência atual do tecido e o que seus genes preveem que acontecerá a seguir. Em resumo, este trabalho traça um roteiro para transformar imagens microscópicas de rotina em mapas ricos, informados por genes, que ajudam os médicos a entender e tratar doenças com mais precisão.
Citação: Chelebian, E., Avenel, C. & Wählby, C. Combining spatial transcriptomics with tissue morphology. Nat Commun 16, 4452 (2025). https://doi.org/10.1038/s41467-025-58989-8
Palavras-chave: transcriptômica espacial, morfologia tecidual, patologia digital, predição de expressão gênica, IA em imageamento