Clear Sky Science · pt
Detecção por nanoporos da conformação de proteínas e peptídeos para aplicações ponto de atendimento
Por que formas diminutas de proteínas podem mudar seu próximo exame
À medida que as populações envelhecem, doenças como Alzheimer, Parkinson, doenças cardíacas e câncer tornam-se mais frequentes. Muitas dessas enfermidades começam quando proteínas vitais e pequenos fragmentos proteicos (peptídeos) mudam sutilmente sua forma muito antes de os sintomas aparecerem. Os testes clínicos atuais normalmente medem quanto de um biomarcador está presente, não se sua forma é normal ou distorcida. Este artigo explora uma tecnologia chamada detecção por nanoporos, que pode “sentir” eletricamente a forma e a química de moléculas proteicas únicas, e argumenta que ela poderia se tornar a base de futuros testes ponto de atendimento que rodem em minutos em um pequeno dispositivo.
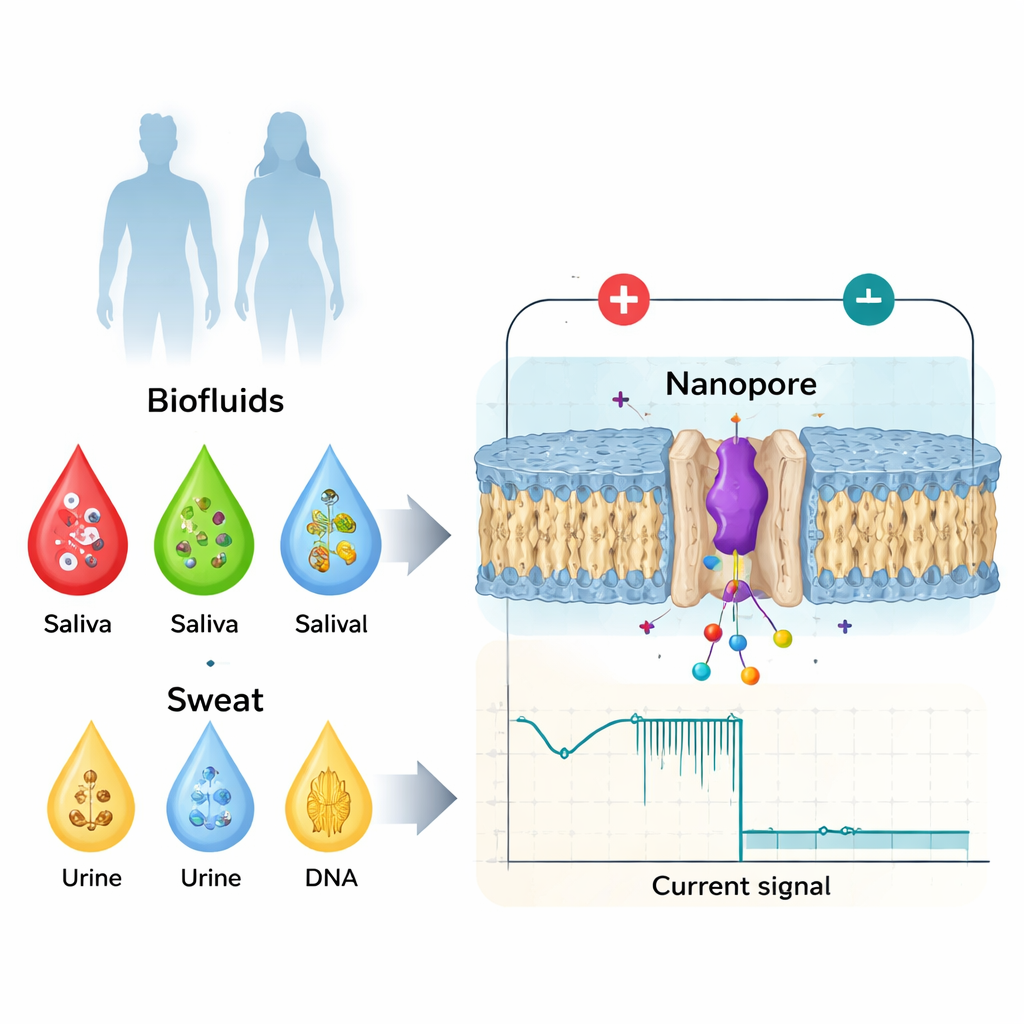
De exames sanguíneos simples a biomarcadores sensíveis à conformação
Médicos já usam muitos biomarcadores coletados do sangue, saliva, urina ou suor — como proteínas, hormônios ou pequenas moléculas — para acompanhar a saúde e a doença. Tradicionalmente, o foco tem sido em alterações evidentes: cópias extras de uma proteína, DNA danificado ou a presença de um componente viral. Mas a biologia revela-se mais sutil. A mesma proteína pode ser ativada ou desativada por pequenas alterações em sua estrutura, por marcas químicas acrescentadas após sua síntese ou por versões espelho dos seus blocos construtores. Essas mudanças pequenas podem alterar como uma proteína se liga a parceiros, forma agregados ou transmite sinais, e estão ligadas a problemas de coagulação sanguínea, doenças neurodegenerativas e câncer. Ferramentas padrão de hospital, como espectrometria de massas, testes baseados em anticorpos e imagens de alta resolução, são poderosas, mas são caras, lentas, exigem pessoal altamente treinado e geralmente não podem ser usadas como dispositivos ponto de atendimento rápidos e simples.
O que um nanoporo faz de diferente
A detecção por nanoporos inverte o problema. Em vez de fazer uma média sobre trilhões de moléculas, ela examina uma por vez enquanto passa por um pequeno orifício em uma membrana com apenas alguns bilhões de metros de largura. Uma voltagem é aplicada para que íons fluam através do poro e criem uma corrente elétrica estável. Quando uma proteína ou peptídeo entra no poro, ela bloqueia parcialmente essa corrente. A profundidade da queda de corrente, quanto tempo ela dura e os detalhes finos de sua forma dependem do tamanho, da carga e da conformação da molécula (sua dobra tridimensional). Projetando cuidadosamente o poro — usando proteínas engenhariadas ou materiais de estado sólido — os pesquisadores podem confinar biomoléculas individuais tempo suficiente para criar “impressões digitais” elétricas ricas que distinguem não apenas proteínas diferentes, mas também variantes sutis do mesmo biomarcador.
Lendo mudanças relevantes para doenças, molécula por molécula
A revisão destaca como os nanoporos já foram usados para resolver diferenças de importância médica que outros métodos têm dificuldade em ver. Eles conseguem separar peptídeos que diferem por um único aminoácido, detectar variantes de hemoglobina ligadas a doenças diretamente do sangue e distinguir peptídeos curtos semelhantes a hormônios que variam por apenas um bloco construtor ou até por uma forma espelho desse bloco. Nanoporos também podem detectar modificações pós-traducionais — pequenas marcas químicas como grupos fosfato, açúcares ou sulfato — que ajudam a controlar se proteínas envolvidas em Alzheimer, Parkinson, coagulação sanguínea ou câncer se comportam de forma normal ou patológica. Em alguns experimentos, uma única enzima ou proteína de ligação é mantida dentro do poro, e mudanças em seu sinal elétrico revelam, em tempo real, como ela se liga a parceiros ou realiza reações, potencialmente expondo vias disfuncionais na doença.
Rumo a testes rápidos à beira do leito
Como cada evento de bloqueio corresponde a uma molécula, dispositivos de nanoporos podem ser extremamente sensíveis, detectando tão poucos quanto milhares de cópias de um biomarcador em um fluido complexo. Os autores discutem estratégias para superar obstáculos-chave para uso clínico: aumentar a taxa de captura de moléculas raras, estabilizar membranas ou usar poros híbridos sólido–biológicos, e empregar aprendizado de máquina para classificar automaticamente padrões elétricos complexos em categorias diagnósticas claras. Eles também mostram como abordagens indiretas — como anexar etiquetas de DNA ou parceiros de ligação — podem amplificar sinais fracos ou permitir a medição simultânea de múltiplos biomarcadores, ao mesmo tempo em que preservam grande parte do detalhe conformacional que torna os nanoporos únicos.
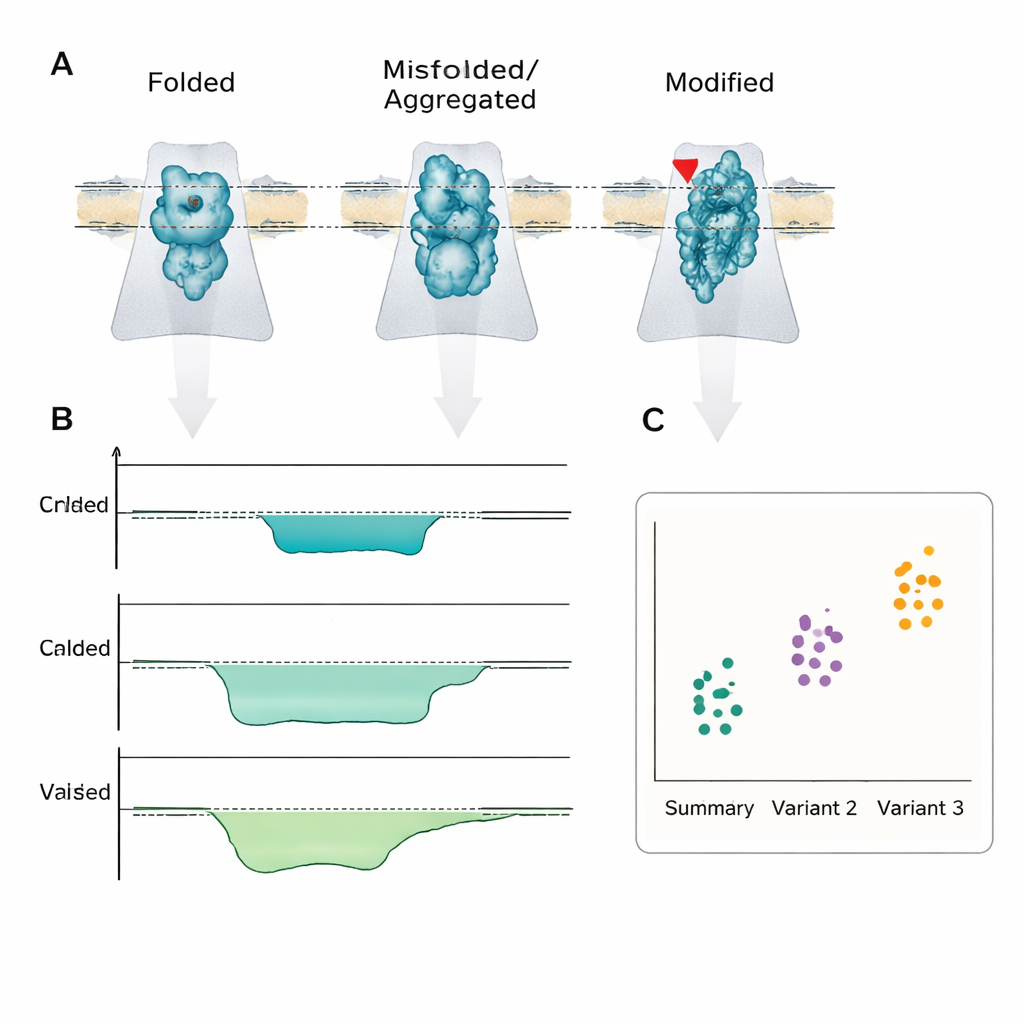
O que isso pode significar para os pacientes
A mensagem central é que a doença frequentemente é guiada menos pela quantidade de proteína existente e mais por qual forma ou versão química está presente. A detecção por nanoporos é uma das poucas tecnologias que pode ler diretamente essas diferenças no nível de molécula única, rápido e simples o suficiente para ser integrada em dispositivos portáteis. Embora desafios significativos de engenharia e padronização permaneçam, os autores argumentam que, da mesma forma que os sequenciadores de DNA por nanoporos avançaram para a clínica, sensores de proteínas e peptídeos por nanoporos poderiam eventualmente fornecer testes rápidos à beira do leito que não apenas indicam “algo está errado”, mas também revelam o enovelamento molecular incorreto ou a modificação exata por trás da condição de um paciente.
Citação: Ratinho, L., Meyer, N., Greive, S. et al. Nanopore sensing of protein and peptide conformation for point-of-care applications. Nat Commun 16, 3211 (2025). https://doi.org/10.1038/s41467-025-58509-8
Palavras-chave: detecção por nanoporos, biomarcadores proteicos, diagnósticos ponto de atendimento, modificações pós-traducionais, doenças conformacionais