Clear Sky Science · pt
Receptores opioides endógenos e o banquete ou a fome do comportamento alimentar mal-adaptativo
Por que nossos cérebros podem nos levar a comer em excesso ou quase não comer
A maioria das pessoas já sentiu tanto desejos intensos por alimentos ricos quanto, em outros momentos, perda de apetite sob estresse. Este artigo explica como o próprio sistema opioide do cérebro — a mesma família de substâncias envolvidas no alívio da dor e no vício em drogas — pode empurrar hábitos alimentares a extremos perigosos. Ao examinar tanto a obesidade quanto a anorexia nervosa, os autores mostram como circuitos cerebrais e sinais químicos semelhantes podem produzir resultados opostos: comer compulsivamente de forma crônica ou a autonegação severa de alimento.

Os químicos do prazer e da dor no cérebro
O corpo produz naturalmente moléculas semelhantes a opioides, como endorfinas, encefalinas e dinorfinas. Essas substâncias atuam em receptores opioides distribuídos pelo cérebro, especialmente em áreas que controlam recompensa, motivação, fome e dor. Quando comemos, sobretudo alimentos saborosos e calóricos, esses sistemas respondem com sinais que podem tornar a comida recompensadora e aliviar o desconforto. Em condições normais, isso nos ajuda a buscar alimento suficiente sem extremos. Mas quando esses receptores estão hiperativos, hipoativos ou conectados de forma diferente, podem distorcer quanto prazer sentimos com a comida, o quanto percebemos fome e quanto de dor ou estresse notamos.
Como os opioides naturais podem alimentar o comer em excesso e a obesidade
Na obesidade, os circuitos de recompensa do cérebro parecem ser remodelados de maneiras que lembram as alterações vistas com drogas aditivas. Receptores opioides em um centro chave de recompensa chamado núcleo accumbens ajudam a impulsionar o desejo de buscar e desfrutar alimentos palatáveis ricos em gordura e açúcar. Estudos genéticos sugerem que certas variantes do gene do receptor mu-opioide podem proteger algumas pessoas de ganhar peso, enquanto outros padrões de regulação gênica estão associados à obesidade. Experimentos em roedores mostram que bloquear os receptores opioides reduz o apelo de dietas doces e ricas em gordura, enquanto remover esses receptores pode tornar os animais resistentes à obesidade induzida por dieta. Ao mesmo tempo, pessoas com obesidade frequentemente apresentam menor disponibilidade de receptores mu-opioides no sistema de recompensa, mas níveis mais altos em regiões hipotalâmicas que detectam fome e saciedade, sugerindo uma mudança a longo prazo em como o cérebro valoriza e regula o alimento.
Quando o mesmo sistema sustenta a autonegação alimentar
A anorexia nervosa, embora externamente oposta à obesidade, também envolve sinalização opioide alterada. Estudos genéticos apontam repetidamente o gene do receptor delta-opioide como um fator de risco, e imagens cerebrais revelam disponibilidade global reduzida de receptores opioides em regiões que processam recompensa, medo e aversão. Uma teoria de longa data propõe que a privação alimentar em indivíduos suscetíveis desencadeia um “barato” auto-reforçador: opioides naturais liberados pela dieta e pelo exercício intenso atenuam o estresse e produzem alívio emocional, incentivando a perda de peso contínua em vez da realimentação normal. Modelos animais em que restrição alimentar é combinada com corrida voluntária mostram padrões semelhantes — hiperatividade, perda de peso e sinais de que o sistema opioide foi levado a um nível basal tão elevado que opioides externos perdem seu impacto. Importante, bloquear receptores opioides em alguns estudos parece ajudar pacientes com anorexia a ganhar peso e estimula roedores a aumentar a ingestão de gordura, sugerindo uma possível via terapêutica.
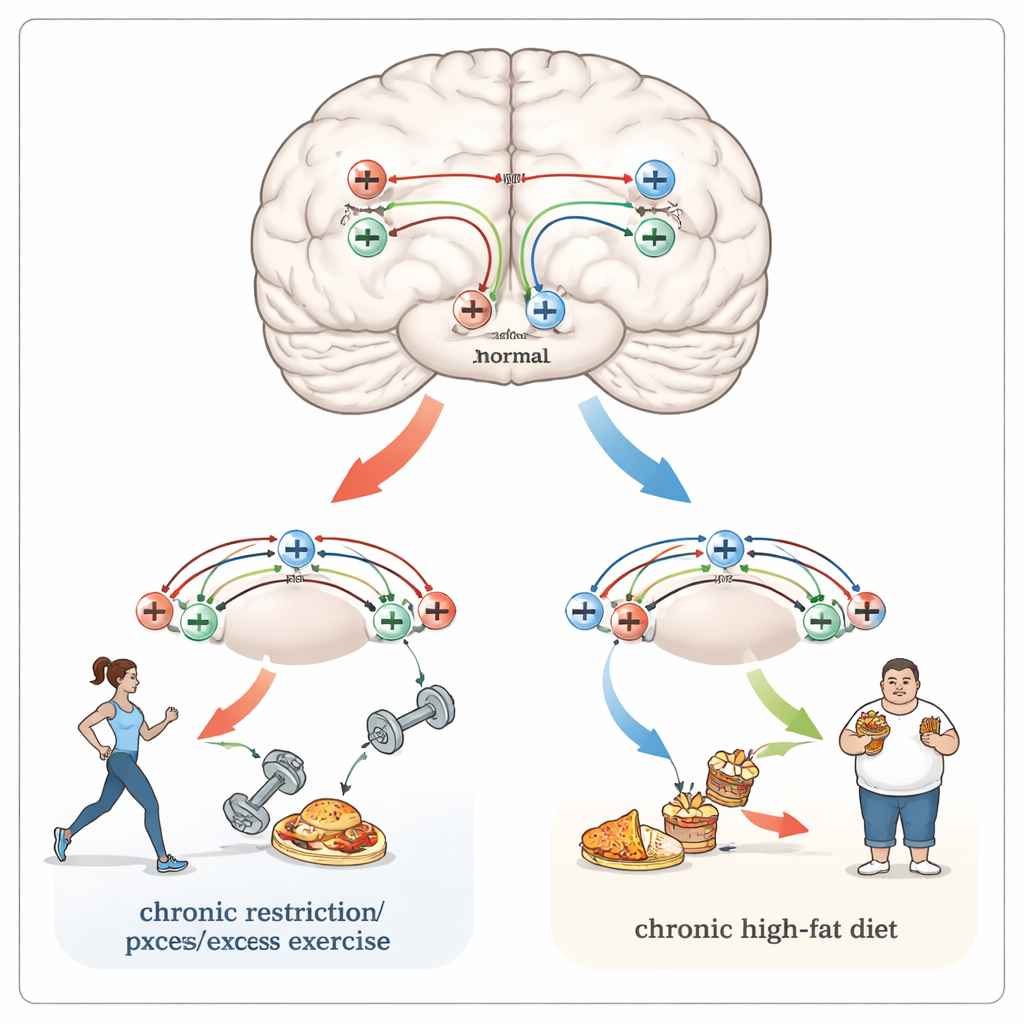
Vínculos compartilhados com dor, dependência e hábitos rígidos
As mesmas regiões e receptores cerebrais que moldam a alimentação também processam dor e recompensas de drogas. Pessoas com obesidade tendem a experimentar mais dor, incluindo enxaquecas, enquanto aquelas com anorexia de longa duração frequentemente apresentam uma resposta atenuada a estímulos dolorosos. Os opioides naturais, agindo em regiões como hipotálamo, tronco encefálico e núcleo accumbens, podem tanto suavizar a dor quanto deslocar a atenção para necessidades urgentes como a fome. Esses circuitos se sobrepõem a vias remodeladas por drogas aditivas, e a restrição alimentar crônica é conhecida por aumentar a sensibilidade a substâncias como opioides em estudos animais. Tanto a obesidade quanto a anorexia também estão associadas à flexibilidade cognitiva reduzida — a capacidade de adaptar hábitos a novas circunstâncias — o que pode refletir mudanças mais profundas e duradouras nas conexões entre neurônios, em parte conduzidas por receptores opioides.
O que isso significa para entender e tratar episódios extremos de alimentação
Em conjunto, as evidências sugerem que o sistema opioide do próprio cérebro ajuda a determinar se mudanças na alimentação — como exposição a alimentos ricos ou períodos de dieta — permanecem temporárias e adaptativas ou se transformam em padrões nocivos e de longa duração. Na obesidade, o comer repetido em excesso parece remodelar os circuitos de recompensa e fome de modo que alimentos hipercalóricos se tornem especialmente atraentes. Na anorexia, a privação e o exercício excessivo podem sequestrar os mesmos processos de aprendizagem dirigidos por opioides para fazer da autonegação e da hiperatividade algo recompensador, apesar da perda de peso perigosa. Ao identificar onde e como esses receptores mudam, argumentam os autores, pesquisas futuras podem orientar tratamentos mais precisos — como bloqueadores de receptores direcionados, estimulação cerebral ou fármacos que normalizem a plasticidade sináptica — para direcionar os circuitos de banquete-ou-fome do cérebro de volta ao equilíbrio.
Citação: Sutton Hickey, A.K., Matikainen-Ankney, B.A. Endogenous opioid receptors and the feast or famine of maladaptive feeding. Nat Commun 16, 2270 (2025). https://doi.org/10.1038/s41467-025-57515-0
Palavras-chave: opioides endógenos, transtornos alimentares, obesidade, anorexia nervosa, circuitos de recompensa do cérebro