Clear Sky Science · pt
Iluminando o impacto da acetilação N-terminal: da proteína à fisiologia
Como pequenas marcas químicas podem alterar o comportamento das proteínas
Cada célula do seu corpo está repleta de proteínas que precisam dobrar corretamente, ir ao lugar certo, montar máquinas moleculares e ser eliminadas quando danificadas. Este artigo de revisão explora uma mudança química sutil, porém extremamente comum, em uma extremidade de muitas proteínas — chamada acetilação N-terminal — e mostra como essa pequena “tampa” ajuda a controlar tudo, desde crescimento celular e respostas ao estresse até desenvolvimento cardíaco e função cerebral.
A tampa protéica que a maioria de nós nunca ouviu falar
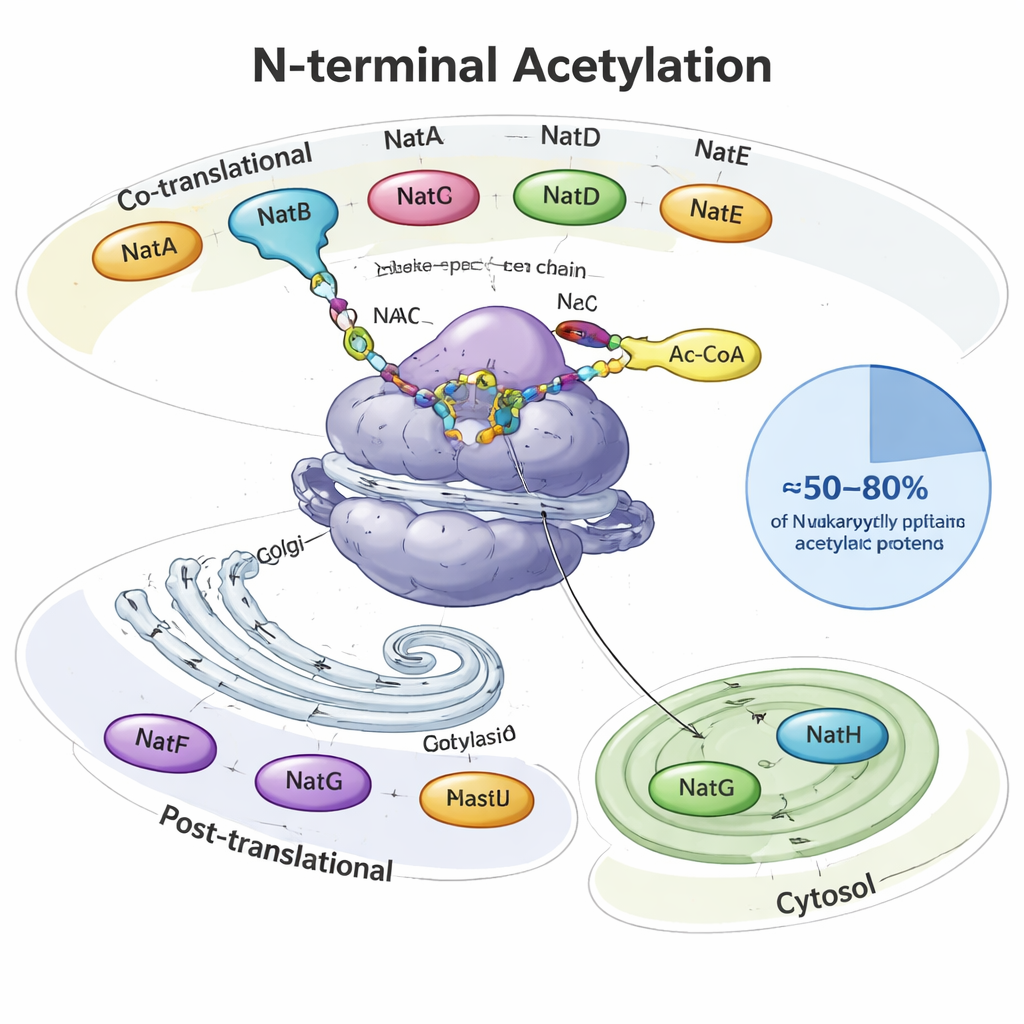
Quando uma proteína é sintetizada, ela sai da fábrica de proteínas da célula, o ribossomo, como um fio em crescimento. Em seu começo — o N-terminal — muitas proteínas eucariotas recebem um grupo acetil, uma pequena tampa de dois carbonos. Enzimas especializadas chamadas acetiltransferases N‑terminais (NATs) realizam esse trabalho, usando uma molécula metabólica comum (acetil‑CoA) como doadora. Em leveduras, plantas e animais, oito tipos principais de NAT (NatA–NatH) dividem essa função. Algumas atuam enquanto a proteína ainda está sendo feita, outras trabalham depois e ficam localizadas em locais específicos, como o aparelho de Golgi ou plastídios de plantas. Juntas, elas modificam cerca de metade a quatro quintos de todas as proteínas celulares, cada NAT reconhecendo sequências iniciais preferenciais de duas a quatro aminoácidos.
Muitas enzimas, cada uma com sua especialidade
NatA, NatB e NatC são as principais, atuando diretamente no ribossomo e cobrindo grandes porções do “acetiloma N‑terminal”. Só a NatA pode modificar cerca de 40% das proteínas humanas, normalmente aquelas cujo metionina inicial foi removida. NatB e NatC atuam em proteínas que mantêm a metionina inicial, mas diferem nos aminoácidos vizinhos que preferem. Outras NATs são mais seletivas: NatD foca em apenas algumas histonas que empacotam o DNA, NatF tem como alvo proteínas transmembranares no Golgi, NatG age dentro de plastídios vegetais, e NatH (NAA80) conclui um processo especial de maturação em duas etapas na actina, um componente principal do esqueleto celular. O artigo reúne estudos estruturais e bioquímicos que mostram como subunidades auxiliares ancoram essas enzimas a ribossomos ou membranas e afinam quais proteínas elas modificam.
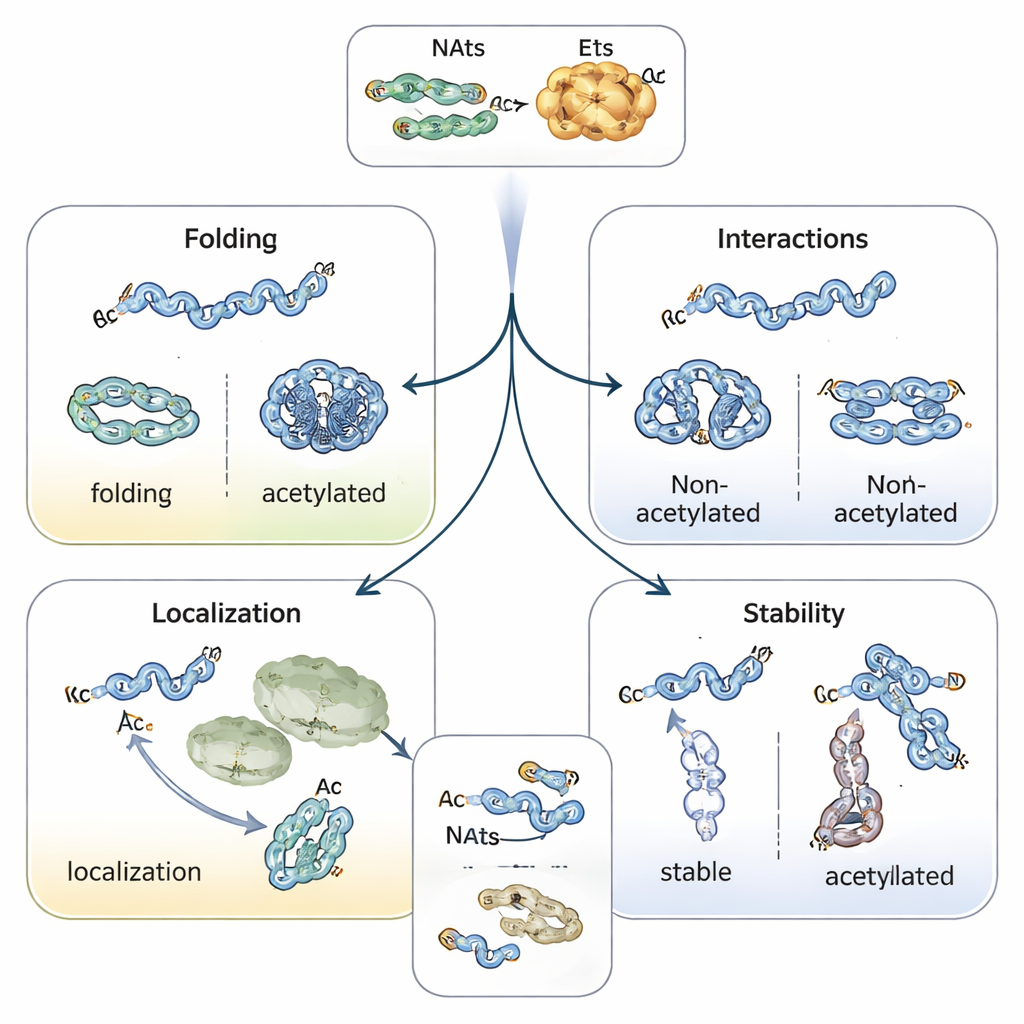
Direcionando o dobramento, localização e tempo de vida das proteínas
Adicionar uma tampa acetil altera a natureza química do início da proteína, frequentemente estabilizando estruturas helicoidais e influenciando como as proteínas se dobram. Por exemplo, a proteína associada ao Parkinson, alfa‑sinucleína, tende a agregar menos e adotar uma conformação mais segura quando seu N‑terminal está acetilado. Tropomiosina, uma parceira da actina, se liga e regula filamentos de actina muito melhor quando adequadamente acetilada. Em plantas e animais, a acetilação N‑terminal pode servir como uma espécie de etiqueta de endereço, ajudando proteínas a encontrar cloroplastos, lisossomos ou o Golgi. Talvez o mais marcante seja seu papel em determinar quanto tempo as proteínas sobrevivem: um N‑terminal desprotegido pode ser lido como um “sinal de degradação” por enzimas que marcam com ubiquitina, enquanto a acetilação pode mascarar esse sinal e estabilizar a proteína — ou, em alguns casos, criar uma etiqueta condicional que só é reconhecida quando a proteína está mal dobrada ou não faz parte do complexo correto.
Da fisiologia celular ao desenvolvimento e à doença
Porque a acetilação N-terminal afeta tantas proteínas, a perturbação das NATs tem consequências amplas para organismos inteiros. A remoção de NatA, NatB ou NatC em espécies-modelo frequentemente causa defeitos de desenvolvimento severos, respostas ao estresse alteradas ou até letalidade, enquanto enzimas mais especializadas, como NatF e NatH, produzem problemas mais restritos, como calcificações cerebrais ou perda auditiva. Em humanos, mutações hereditárias em vários genes de NATs estão na base de síndromes raras de neurodesenvolvimento com deficiência intelectual, defeitos cardíacos ou fraqueza muscular. A mesma maquinaria costuma estar hiperativa em cânceres, onde níveis elevados de NATs se correlacionam com pior prognóstico e podem impulsionar crescimento tumoral, metástase e resistência a terapias. Alterações na acetilação N‑terminal também influenciam proteínas propensas à agregação, como alfa‑sinucleína e huntingtina, ligando essa modificação a mecanismos de doenças neurodegenerativas.
Direções futuras e promessa médica
Os autores concluem que, embora hoje conheçamos a maioria das enzimas centrais que adicionam essas tampas N‑terminais, ainda entendemos apenas uma fração dos alvos proteicos específicos e das regras regulatórias. Um tema importante é que a acetilação no início da proteína frequentemente a protege da destruição prematura, ao mesmo tempo em que cria sinais contextuais para controle de qualidade. Identificar quais ligases de ubiquitina reconhecem quais padrões N‑terminais, e descobrir se existe alguma enzima capaz de remover essas tampas, são questões centrais em aberto. Como as NATs estão no cruzamento entre estabilidade proteica, regulação gênica e respostas ao estresse celular, inibidores seletivos de NAT — e talvez futuras ferramentas que ajustem a acetilação N‑terminal de proteínas específicas relacionadas a doenças — surgem como vias promissoras para novas terapias em câncer, doenças cardiovasculares e neurodegeneração.
Citação: McTiernan, N., Kjosås, I. & Arnesen, T. Illuminating the impact of N-terminal acetylation: from protein to physiology. Nat Commun 16, 703 (2025). https://doi.org/10.1038/s41467-025-55960-5
Palavras-chave: modificação de proteínas, acetilação N-terminal, controle de qualidade de proteínas, doença neurodegenerativa, biologia do câncer