Clear Sky Science · pt
metilação de RNA m6A modula a resposta antiviral na doença celíaca
Quando um Vírus e o Glúten se Aliam
A doença celíaca costuma ser vista como um problema alimentar simples: comer glúten e o intestino se prejudica. Este estudo revela uma história mais profunda, em que um tipo comum de vírus intestinal e uma pequena marca química em nossas moléculas de RNA atuam conjuntamente para levar o sistema imunológico a um dano duradouro. Entender essa camada oculta de controle pode ajudar a explicar por que apenas algumas pessoas desenvolvem doença celíaca e apontar para novos tratamentos que vão além da dieta sem glúten. 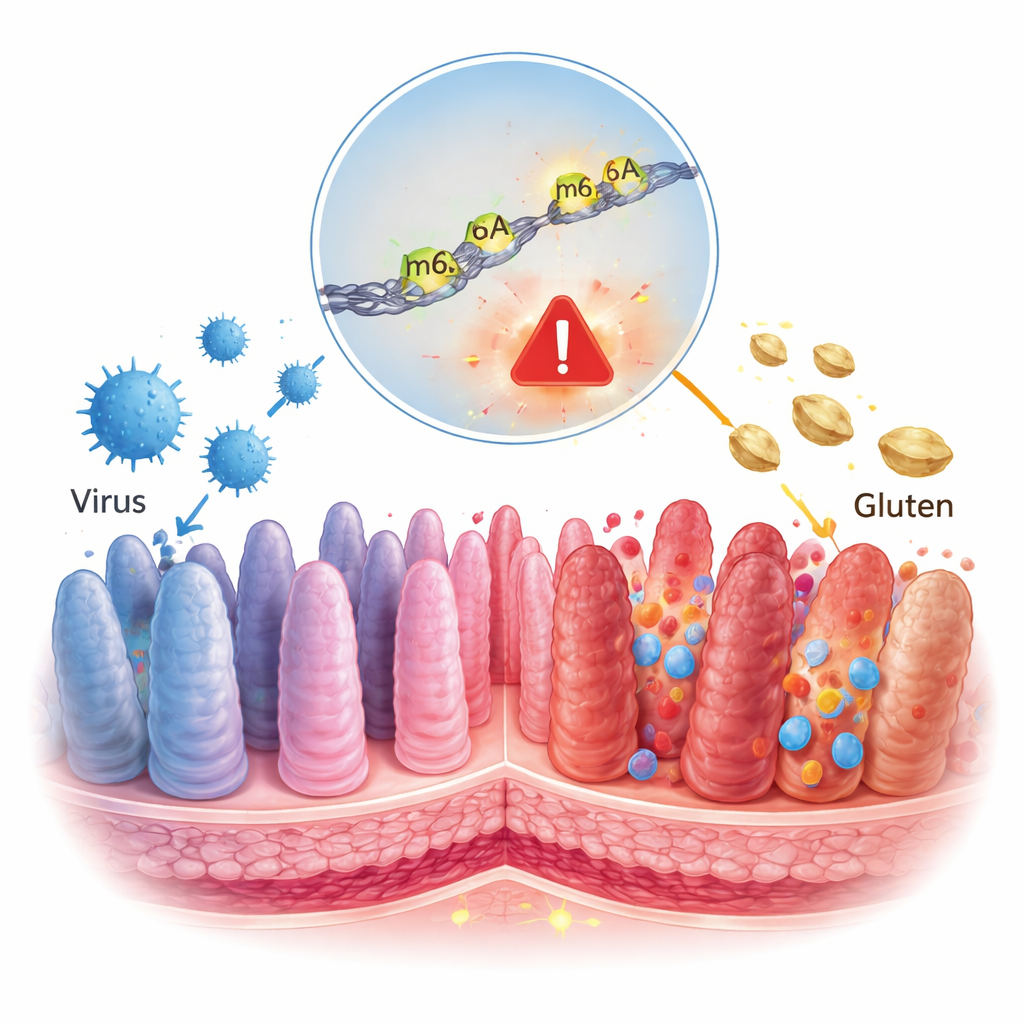
Uma Marca Oculta nas Nossas Mensagens Genéticas
Nossas células leem genes constantemente e os copiam em RNA, curtas “mensagens” que dizem à célula quais proteínas produzir. Essas mensagens não são fixas; elas podem ser decoradas com marcas químicas que agem como marcadores, mudando o grau de leitura da mensagem. Uma das marcas mais comuns chama‑se m6A, uma pequena alteração nas letras do RNA. Sabe‑se que vírus alteram essas marcas de RNA em células infectadas, e trabalhos anteriores já haviam ligado m6A à forma como o glúten desencadeia inflamação no intestino de celíacos. Os autores deste artigo perguntaram se uma mudança em m6A induzida por vírus poderia ajudar a virar o interruptor do sistema imune da tolerância alimentar para o ataque.
Evidências de Pacientes com Doença Celíaca
Os pesquisadores primeiro examinaram sangue e biópsias intestinais de pessoas com doença celíaca ativa e de controles sem doença. Eles descobriram que pacientes celíacos apresentavam níveis mais altos de anticorpos contra reovírus, um vírus de RNA fita dupla que infecta o intestino, sugerindo exposição mais frequente ou mais intensa. No tecido intestinal desses pacientes, genes-chave de alerta antiviral, especialmente um chamado IRF7, estavam ativados em níveis maiores, junto com moléculas inflamatórias como STAT1 e o atrativo para células imunes CXCL10. Ao mesmo tempo, a maquinaria que adiciona e lê marcas m6A estava mais ativa, e os níveis totais de m6A no RNA eram maiores. A expressão de genes antivirais subia e caía em conjunto com genes relacionados a m6A, sugerindo que o mesmo sistema de controle poderia estar impulsionando tanto a defesa viral quanto o dano autoimune.
Como o Glúten Amplifica o Alarme Viral
Para investigar causa e efeito, a equipe construiu um modelo semelhante ao da doença celíaca em células intestinais cultivadas em laboratório. Eles mimetizaram uma infecção viral usando um RNA sintético de fita dupla e então adicionaram fragmentos de glúten digerido semelhantes ao que apareceria no intestino após uma refeição. O mimético viral sozinho aumentou tanto IRF3 quanto IRF7, dois interruptores mestre das respostas antivirais. Mas quando o glúten foi adicionado, IRF7 mostrou um forte aumento adicional, enquanto IRF3 não. Os pesquisadores descobriram que, nessas condições, as marcas m6A aumentaram em uma região específica do RNA de IRF7, e que esse RNA interagia fisicamente com uma enzima que escreve m6A (METTL3) e uma que a remove (ALKBH5). Elevar m6A, seja adicionando mais METTL3 ou reduzindo ALKBH5, elevou ainda mais os níveis de IRF7, ligando diretamente a sinergia glúten‑mais‑vírus a essa modificação de RNA. 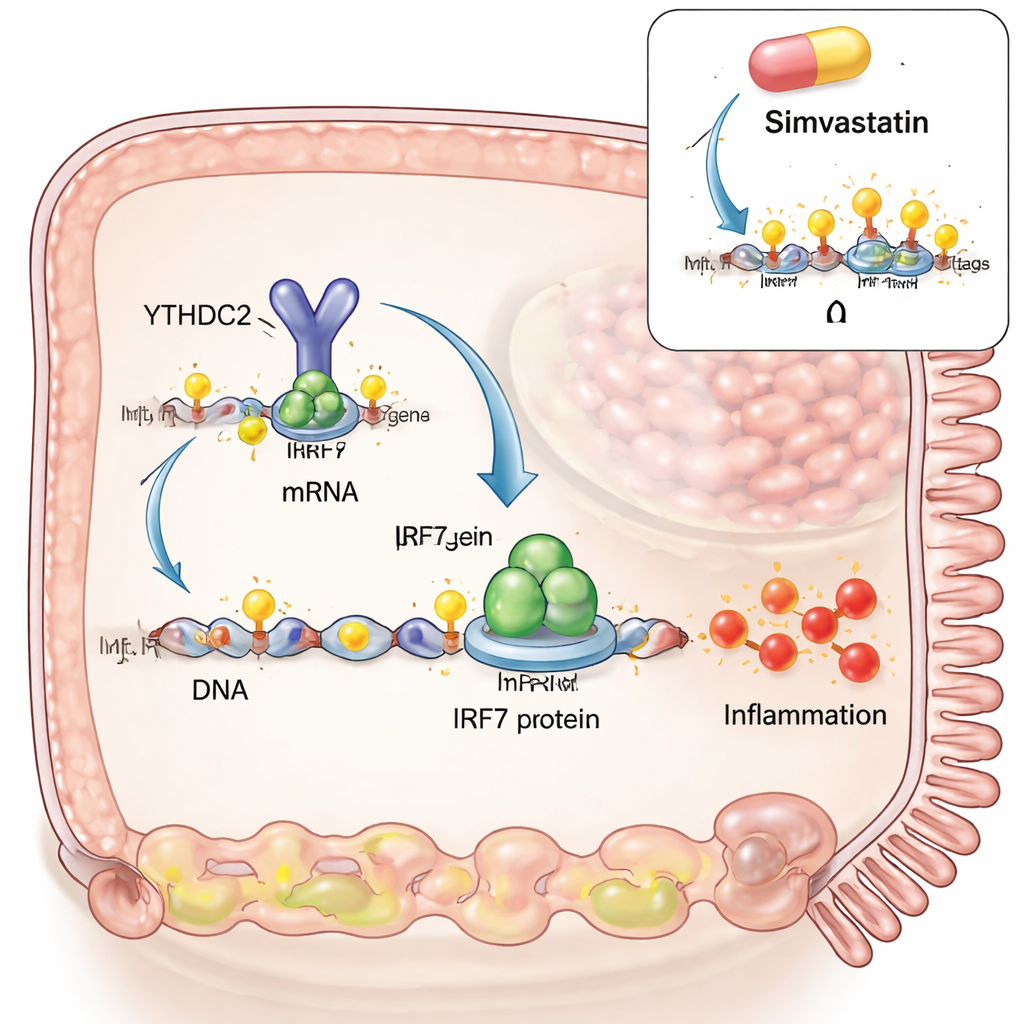
O Intermediário Molecular e um Medicamento Surpreendente
Em seguida, os autores investigaram como as marcas m6A no RNA de IRF7 realmente mudam o comportamento celular. Eles projetaram uma versão do RNA de IRF7 com o mesmo código proteico, mas sem os sítios de m6A. Esse RNA produziu quantidades semelhantes de transcrito, porém muito menos proteína IRF7, e não conseguiu desencadear genes inflamatórios downstream como STAT1 e CXCL10. O elo perdido foi uma proteína leitora chamada YTHDC2, que normalmente se liga ao m6A dentro da região que codifica a proteína e ajuda a promover a tradução eficiente em proteína. Sem os sítios m6A, YTHDC2 não conseguia mais se ligar ao RNA de IRF7. Bloquear a enzima escritora METTL3 no modelo celular reduziu a proteína IRF7 e CXCL10, diminuindo a saída inflamatória. Um medicamento redutor de colesterol, a sinvastatina, que recentemente foi demonstrado reduzir m6A em outros tecidos, também cortou m6A no RNA de IRF7, reduziu a proteína IRF7 nas células e atenuou genes relacionados a IRF7 em biópsias intestinais de celíacos obtidas recentemente e cultivadas ex vivo. Comparações em larga escala de expressão gênica sugeriram que a sinvastatina empurra o tecido celíaco para um perfil mais parecido com o de pacientes em dieta sem glúten.
O Que Isso Significa para Pessoas com Doença Celíaca
Este trabalho descreve um quadro em que um vírus intestinal e o glúten agem juntos sobre uma camada fina e afinada de controle do RNA. Em indivíduos suscetíveis, a infecção viral parece aumentar a marcação m6A do RNA de IRF7 em células intestinais. A exposição ao glúten então amplifica ainda mais esse sinal marcado, levando a mais proteína IRF7, alarmes antivirais mais fortes e níveis mais altos de mensageiros inflamatórios que ajudam a impulsionar o ataque autoimune ao revestimento intestinal. Ao reduzir as marcas m6A — seja geneticamente ou com um medicamento como a sinvastatina — a reação em cadeia pode ser suavizada, ao menos em modelos de laboratório e ex vivo. Para leitores leigos, a mensagem principal é que a doença celíaca não é somente sobre o que se come, mas também sobre como infecções e marcas químicas sutis no RNA moldam a decisão do sistema imune de tolerar ou atacar. Mirar essas marcas de RNA poderia, algum dia, complementar a dieta sem glúten e inspirar novos tratamentos para uma gama mais ampla de doenças autoimunes.
Citação: Sebastian-delaCruz, M., Olazagoitia-Garmendia, A., Pascual-Gonzalez, I. et al. m6A RNA methylation modulates antiviral response in celiac disease. Genes Immun 27, 130–139 (2026). https://doi.org/10.1038/s41435-025-00373-z
Palavras-chave: doença celíaca, metilação de RNA, imunidade antiviral, IRF7, sinvastatina