Clear Sky Science · pt
CRISPR-AuNP: otimização físico-química de uma plataforma de nanopartículas de ouro para edição gênica não viral modular e de baixo custo em HSPCs
Levando a edição gênica a mais pacientes
Ferramentas de edição gênica como o CRISPR já transformaram a vida de pessoas com doenças sanguíneas hereditárias, mas os tratamentos ainda são caros, tecnicamente exigentes e concentrados em poucos centros especializados. Este artigo descreve uma nova forma de entregar CRISPR em células-tronco formadoras de sangue usando partículas minúsculas à base de ouro que podem ser montadas em bancada em apenas algumas horas. O objetivo é tornar abordagens poderosas de edição gênica mais simples, mais baratas e mais fáceis de implementar em mais lugares do mundo.
Por que as células-tronco sanguíneas importam
Células-tronco e progenitoras formadoras de sangue vivem na medula óssea e reabastecem continuamente todos os tipos de células sanguíneas do corpo. Se os médicos conseguirem corrigir com segurança mutações causadoras de doenças nessas células, um tratamento único poderia proporcionar cura vitalícia para condições como anemia falciforme e algumas deficiências imunológicas. Hoje, a forma mais comum de introduzir CRISPR nessas células depende da eletroporação, um processo que usa pulsos elétricos para abrir poros nas membranas celulares. Embora potente, a eletroporação é agressiva para as células, exige equipamentos caros e reagentes especializados, e não é facilmente escalável ou exportável para ambientes com recursos limitados. Vetores virais mais seguros são excelentes para muitas terapias gênicas, mas são menos adequados para a entrega de CRISPR porque continuam produzindo as ferramentas de edição por tempo excessivo, aumentando o risco de alterações fora do alvo.
Construindo um minúsculo veículo de entrega de ouro
Os pesquisadores buscaram aprimorar um sistema de nanopartículas de ouro previamente relatado, que carregava componentes do CRISPR em sua superfície. Em projetos anteriores, o RNA guia que direciona a proteína de corte do CRISPR ao alvo era ancorado diretamente ao núcleo de ouro e então pareado com a proteína Cas9. Isso funcionou razoavelmente bem para um tipo de enzima CRISPR, mas teve desempenho ruim com a Cas9, central para muitas estratégias terapêuticas. Ao examinar de perto como a Cas9 e seu RNA guia se comportavam nas condições ácidas usadas durante a montagem das partículas, a equipe descobriu que o dímero de RNA guia se tornava instável na superfície de ouro, levando a pouco ou nenhum Cas9 ativo ligado à partícula. A microscopia confocal também sugeriu que a camada polimérica projetada para ajudar as partículas a escapar de compartimentos celulares se desprendia antes de cumprir sua função.
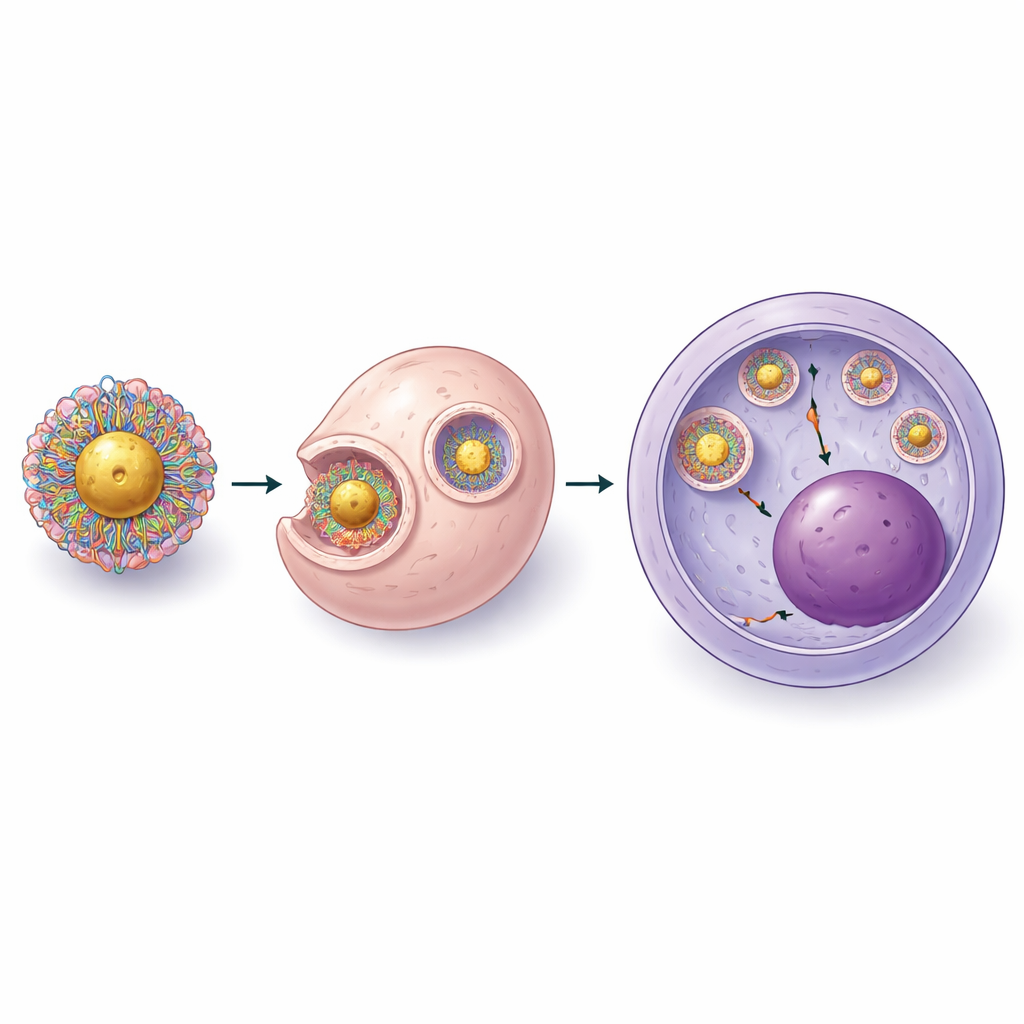
Redesign passo a passo da plataforma
Para contornar esses problemas, os cientistas reconstruíram o sistema do zero em três etapas. Primeiro, em vez de ancorar RNA nu ao ouro e depois adicionar a proteína, formaram complexos ribonucleoproteicos completos do CRISPR (proteína mais RNA guia) antes de colocá-los em contato com a superfície de ouro. Identificaram uma condição levemente ácida que permitia que esses complexos se ligassem às partículas mantendo a proteína de corte ativa. Em seguida, envolveram as partículas carregadas com polímeros especialmente projetados que combinavam cadeias carregadas positivamente — necessárias para escapar de compartimentos celulares — com segmentos flexíveis e hidrofílicos de polietilenoglicol que evitam a aglomeração. Medindo tamanho, carga superficial e conteúdo proteico, demonstraram ser possível carregar de forma reprodutível dezenas de complexos CRISPR por partícula, mantendo a estabilidade em solução.
Quebrando as defesas da célula
Mesmo com melhor carregamento, as partículas de segunda geração ainda enfrentavam um obstáculo chave: fazer o CRISPR escapar dos vesículas internas da célula e atingir a região onde o DNA reside. A equipe, portanto, afinou sistematicamente a química da camada polimérica e a razão entre grupos positivos no polímero e grupos negativos no complexo CRISPR. Descobriram que adicionar mais cadeias curtas de polietilenoglicol e um número controlado de âncoras contendo enxofre melhorava tanto a estabilidade das partículas quanto a capacidade de perturbar membranas endossômicas sem prejudicar as células. No desenho final, de terceira geração, criaram primeiro complexos compactos de CRISPR e polímero e depois os anexaram a núcleos de ouro concentrados. Microscopia eletrônica mostrou uma casca fina de CRISPR e polímero ao redor de cada esfera de ouro, e imagens em células-tronco vivas confirmaram que a carga podia escapar para o interior celular e alcançar o núcleo.
Resultados de edição com múltiplas ferramentas CRISPR
Para testar o desempenho das partículas otimizadas, os pesquisadores miraram em um gene chamado beta-2-microglobulina, que produz uma proteína encontrada na superfície de quase todas as células sanguíneas e pode ser facilmente quantificada por citometria de fluxo. Usando sua plataforma de ouro de terceira geração, alcançaram mais de 10% de interrupções precisas desse gene em células-tronco e progenitoras sanguíneas humanas primárias — níveis considerados significativos para muitas aplicações terapêuticas — enquanto mantinham alta sobrevivência celular. Embora essa eficiência seja menor do que a obtida por eletroporação, o sistema de ouro não exigiu equipamento especializado e causou estresse mínimo às células. Importante, a mesma plataforma pôde ser usada com diferentes proteínas CRISPR, incluindo Cas9, Cas12a e uma enzima mais nova chamada Cas12a-M29-1, com níveis de edição semelhantes e nenhuma toxicidade detectável, ressaltando a natureza modular do projeto.
O que isso pode significar para terapias futuras
Em termos simples, este trabalho mostra que é possível construir um pequeno transportador engenhosamente projetado à base de ouro que pode levar ferramentas CRISPR a células-tronco sanguíneas sensíveis sem eletricidade ou vírus, usando materiais comerciais por menos de setenta dólares por milhão de células. Embora melhorias adicionais sejam necessárias para igualar a eficiência dos melhores métodos clínicos atuais, especialmente para doenças que exigem níveis muito altos de células corrigidas, essa plataforma montada em bancada reduz barreiras práticas para realizar edição gênica sofisticada. Com refinamento contínuo e testes de segurança, tais nanopartículas poderiam ajudar a ampliar os benefícios das terapias baseadas em CRISPR além de centros especializados, tornando tratamentos curativos mais acessíveis a pacientes no mundo todo.
Citação: Gottimukkala, K.S.V., Lane, D.D., Cunningham, R. et al. CRISPR-AuNP: physicochemical optimization of a gold nanoparticle platform for cost-effective and modular non-viral gene editing in HSPCs. Gene Ther 33, 188–202 (2026). https://doi.org/10.1038/s41434-025-00591-0
Palavras-chave: edição gênica CRISPR, nanopartículas de ouro, células-tronco hematopoéticas, entrega não viral, nanomedicina