Clear Sky Science · pt
Repensando a genômica da distrofia muscular facioescapuloumeral na era telômero-a-telômero: armadilhas na paisagem oculta de repetições D4Z4
Por que esta história sobre uma doença muscular importa
A distrofia muscular facioescapuloumeral (FSHD) é uma das doenças hereditárias de desgaste muscular mais comuns, frequentemente enfraquecendo os músculos do rosto e dos ombros de jovens adultos aparentemente saudáveis. Durante anos, cientistas concentram-se em um único trecho de DNA próximo à ponta do cromossomo 4 como o culpado. Este novo estudo mostra que o quadro é muito mais complexo: repetições de DNA semelhantes estão espalhadas pelo genoma, e muitos testes laboratoriais padrão não conseguem distingui-las. Compreender essa paisagem oculta é essencial para um diagnóstico preciso, melhor pesquisa e, em última instância, terapias mais seguras.
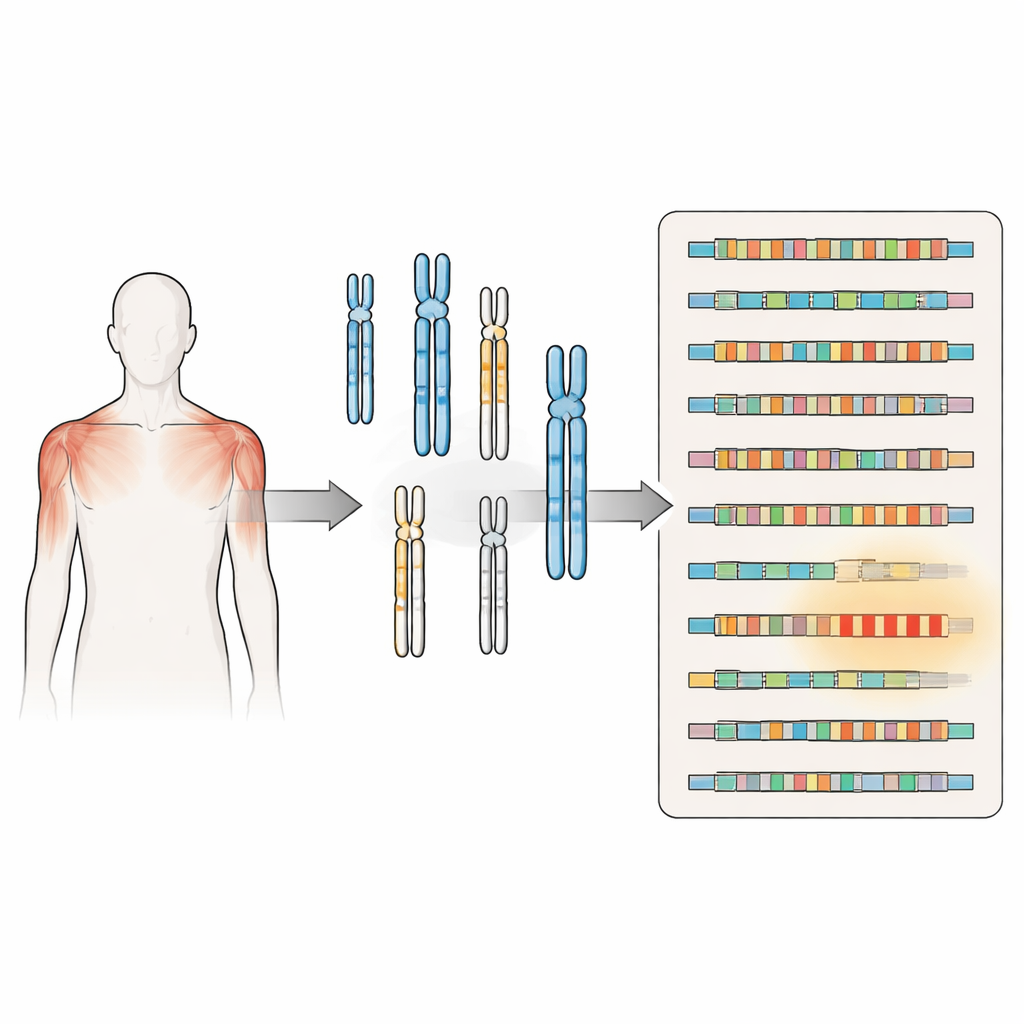
Um olhar mais atento sobre um distúrbio muscular intrigante
A FSHD há muito tempo é associada ao encurtamento de uma sequência de DNA repetida chamada D4Z4 perto da extremidade do cromossomo 4. Quando essa região repetida encolhe abaixo de um determinado tamanho e situa-se em um contexto genético particular, ela permite a produção de uma proteína chamada DUX4, que pode danificar células musculares. Uma segunda forma da doença surge quando genes que normalmente mantêm essa região fortemente compactada e silenciada estão mutados, novamente permitindo que o DUX4 apareça. Ambas as vias convergem para o mesmo problema: um gene que deveria estar majoritariamente desligado no músculo adulto torna-se esporadicamente ativo, contribuindo para fraqueza e atrofia muscular.
Repetições ocultas pelo genoma
Mapas anteriores do genoma humano eram incompletos, especialmente em regiões ricas em DNA repetitivo nas extremidades dos cromossomos e próximas aos centrômeros. Usando a nova montagem do genoma humano telômero-a-telômero, que preenche essas lacunas, os autores reexaminaram todo o genoma usando a sequência D4Z4 do cromossomo 4 como molde de busca. Eles descobriram aglomerados e cópias isoladas de repetições semelhantes a D4Z4 em pelo menos dez cromossomos adicionais. Algumas dessas repetições são estruturalmente completas e ficam próximas a sinais que poderiam estabilizar RNAs do tipo DUX4, sugerindo que elas podem produzir proteínas ou moléculas de RNA relacionadas sob condições apropriadas.
Quando os testes de laboratório veem mais de um lugar ao mesmo tempo
A pesquisa e o diagnóstico da FSHD frequentemente dependem de testes que amplificam fragmentos específicos de DNA ou RNA com sequências curtas de primers, uma estratégia conhecida como PCR. Esses primers foram originalmente projetados sob a suposição de que as repetições D4Z4 existiam apenas nos cromossomos 4 e 10. Combinando predições computacionais com experimentos em células que carregam cromossomos humanos individuais, os autores mostram que muitos conjuntos de primers amplamente usados se ligam não apenas à região ligada à doença no cromossomo 4, mas também a repetições semelhantes espalhadas pelo genoma. Primers direcionados ao exon principal do DUX4 ou a lncRNAs vizinhos frequentemente amplificam produtos de vários cromossomos ao mesmo tempo, tornando impossível saber onde um sinal específico realmente se originou.
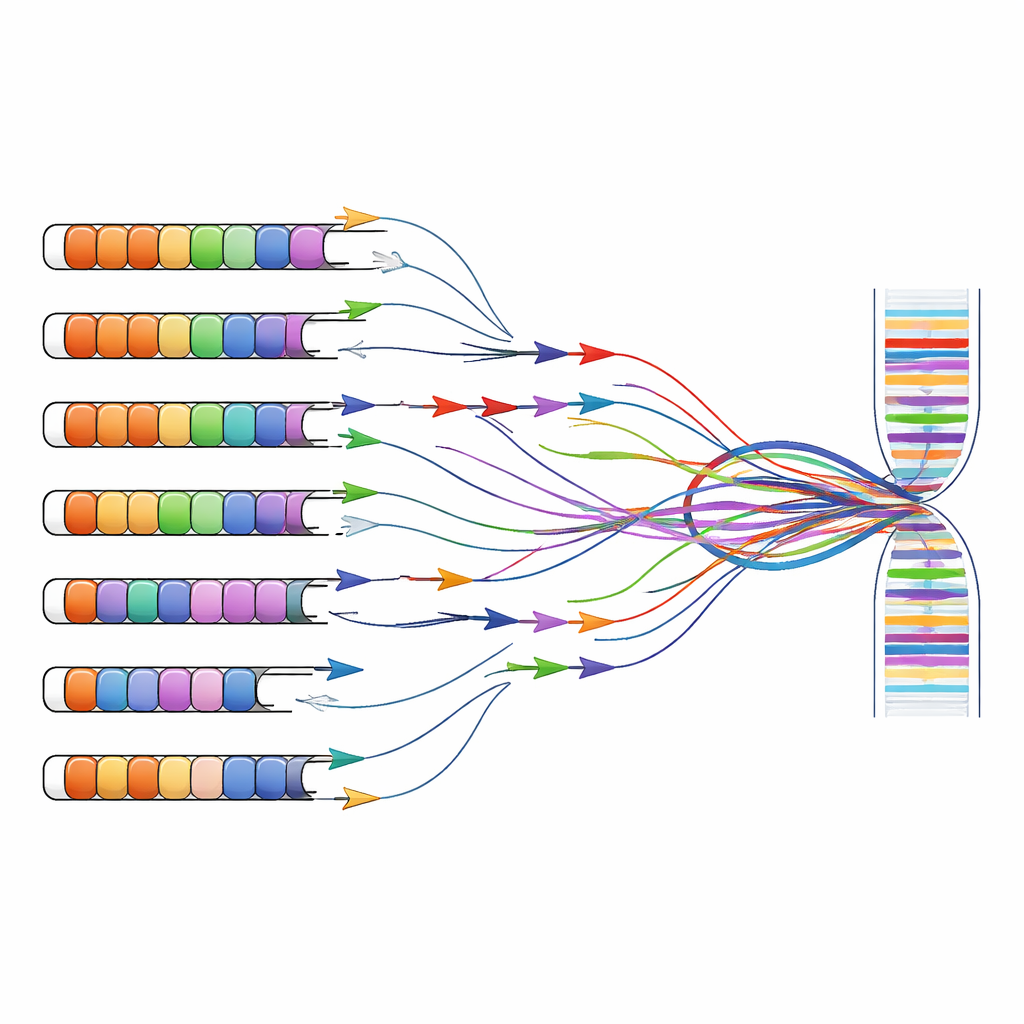
Repensando ferramentas de diagnóstico e pesquisa
Esse problema de múltiplas localizações vai além da pesquisa básica e alcança a clínica. Testes mais recentes que medem metilação do DNA (uma marca química associada ao silenciamento gênico) ou que usam sequenciamento de leituras curtas frequentemente agregam sinais de muitas repetições quase idênticas. Como resultado, medições de “metilação D4Z4” ou “transcritos DUX4” em conjuntos de dados públicos podem, na verdade, refletir uma mistura de contribuições do cromossomo 4, do cromossomo 10 e de outros sítios. Os autores argumentam que, para vincular corretamente alterações genéticas aos sintomas, os cientistas agora devem adotar métodos conscientes de repetições que diferenciem loci individuais — por exemplo, sequenciamento de leituras longas que possa abranger blocos repetidos inteiros e capturar seus padrões de metilação e produtos de RNA na íntegra.
O que isso significa para pacientes e terapias futuras
O estudo não derruba o papel central da região D4Z4 encurtada no cromossomo 4 na FSHD, mas mostra que essa região vive em um bairro saturado por sequências semelhantes. Sinais antes assumidos como prova de atividade no locus da doença podem, de fato, provir em parte de seus “primos” genômicos. Para os pacientes, isso significa que as ferramentas de diagnóstico mais confiáveis serão aquelas que resolvem fisicamente qual cromossomo e qual arranjo repetido está envolvido, em vez de depender apenas de leituras indiretas. Para pesquisadores e desenvolvedores de fármacos, destaca a necessidade de projetos altamente específicos que evitem atingir acidentalmente repetições inofensivas em outras partes do genoma. Na era telômero-a-telômero, compreender e tratar a FSHD dependerá de ver toda a paisagem de repetições, não apenas um único marco.
Citação: Salsi, V., Losi, F., Pini, S. et al. Rethinking genomics of facioscapulohumeral muscular dystrophy in the telomere-to-telomere era: pitfalls in the hidden landscape of D4Z4 repeats. Eur J Hum Genet 34, 357–367 (2026). https://doi.org/10.1038/s41431-025-02000-x
Palavras-chave: distrofia muscular facioescapuloumeral, repetições D4Z4, DUX4, genoma telômero-a-telômero, diagnóstico genético