Clear Sky Science · pt
Chaperonas artificiais: de designs convencionais a sistemas inteligentes
Ajudando Moléculas a Dobrarem do Jeito Certo
Dentro de cada célula viva, longas cadeias de proteínas e material genético precisam se dobrar e torcer até adquirirem formas exatas para funcionar corretamente. Quando se dobram mal, podem aglomerar‑se, perder suas funções e até desencadear doenças como as neurodegenerativas. A natureza conta com moléculas “chaperonas” para manter essa multidão microscópica em ordem, mas esses ajudantes naturais são caros, frágeis e difíceis de usar fora das células. Este artigo explora como cientistas estão construindo chaperonas artificiais — ajudantes projetados que podem reconduzir moléculas desnorteadas à forma correta e que podem até ser ligados e desligados como ferramentas inteligentes.
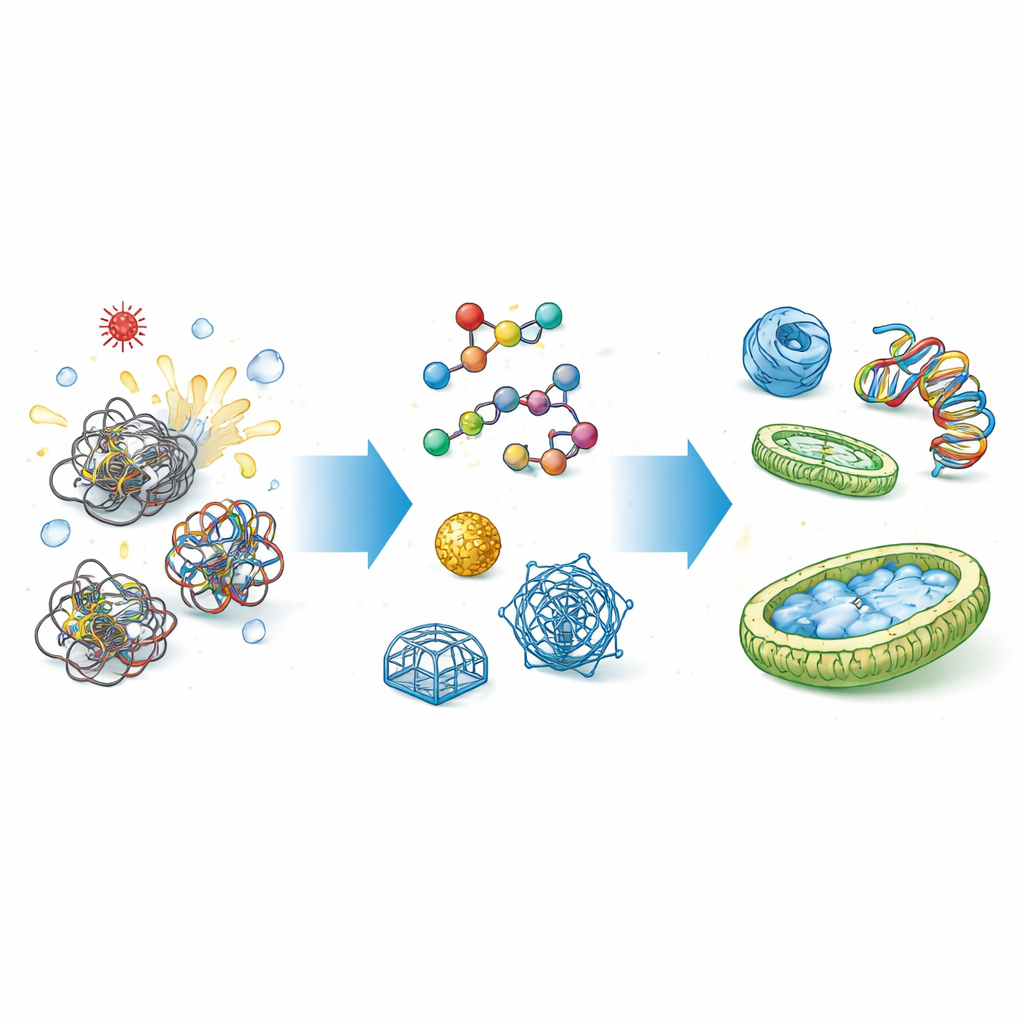
Por Que as Células Precisam de Ajudantes de Dobramento
Proteínas e ácidos nucleicos (como DNA e RNA) não nascem prontos; eles precisam dobrar em formas tridimensionais intrincadas. O caminho até essas formas está cheio de armadilhas, nas quais as cadeias podem ficar presas ou aderir umas às outras. Chaperonas naturais, como as proteínas de choque térmico, seguram essas cadeias flexíveis, isolam suas partes pegajosas e fornecem um espaço protegido para que dobrem corretamente. Papéis semelhantes ocorrem para ácidos nucleicos, onde chaperonas ajudam a deslizar nós e rearranjar pares de bases. Quando esse controle falha, o resultado pode ser perda de função, aglomerados tóxicos, doenças e falhas dispendiosas na produção industrial de proteínas.
De Produtos Químicos Simples a Polímeros Projetados
As primeiras chaperonas artificiais eram produtos químicos relativamente simples que alteravam a sensação do ambiente para as moléculas. Certos solventes e detergentes podem ocultar regiões pegajosas em proteínas, impedir aglomerações e dar uma segunda chance para que elas se refoldem. Alguns ácidos graxos pequenos, por exemplo, ajudam colágeno mutante a dobrar mais corretamente e aliviam o estresse dentro de células afetadas por doenças hereditárias. Mas esses ajudantes químicos normalmente precisam ser adicionados em altas doses, são difíceis de ajustar para alvos específicos e podem perturbar outros componentes em misturas complexas. Para obter mais controle, pesquisadores recorreram a polímeros maiores e sob medida — cadeias flexíveis que podem ser decoradas com ramos carregados ou hidrofílicos para acomodar DNA, RNA e proteínas de forma mais seletiva.
Kit de Ferramentas de Polímeros e Nanogéis
Polímeros projetados podem ligar‑se às costas carregadas do DNA ou a parches expostos em proteínas, suavizando o panorama energético para que essas moléculas encontrem suas formas preferidas mais rapidamente e com maior confiabilidade. Para ácidos nucleicos, polímeros catiônicos (carregados positivamente) podem neutralizar a repulsão entre fitas, acelerando o pareamento de bases, a troca de fitas e a formação de estruturas exóticas usadas em computação baseada em DNA e biossensores. Para proteínas, polímeros como laços de polietilenoglicol especialmente moldados ou polianions sintéticos podem superar algumas chaperonas naturais na prevenção de agregação induzida por calor. Outros sistemas emparelham polímeros chaperona flexíveis com peptídeos curtos para remodelar membranas semelhantes às celulares em nanosheets planos ou vesículas, criando plataformas bidimensionais reversíveis para entrega de carga e engenharia de tecidos.

Construindo Chaperonas Inteligentes e Comutáveis
Além de simplesmente segurar e liberar seus clientes, chaperonas artificiais modernas podem agora responder ao ambiente. Pesquisadores construíram nanogéis, nanopartículas e redes poliméricas cuja fixação em proteínas aperta ou afrouxa com mudanças de acidez, temperatura, luz ou químicos específicos como a glicose. Por exemplo, alguns micelos tornam‑se mais hidrofóbicos em pH levemente ácido, imitando chaperonas naturais ao capturar proteínas ameaçadas e depois liberá‑las quando o pH muda novamente. Polímeros responsivos à temperatura colapsam ou se expandem ao atravessarem um limiar, permitindo sequestrar proteínas danificadas em uma temperatura e liberar as refoldadas em outra. Grupos sensíveis à luz podem ser usados como interruptores moleculares, ligando ou desligando vias de montagem de DNA com um flash, enquanto partículas responsivas a açúcares podem proteger um hormônio terapêutico e então liberá‑lo de forma preferencial quando a glicemia está alta.
O Que Isso Significa para a Medicina e a Tecnologia
O artigo conclui que as chaperonas artificiais estão evoluindo de simples estabilizadores químicos para “ferramentas moleculares” altamente programáveis que podem reconhecer, proteger e remodelar diversos tipos de estruturas biológicas sob demanda. Ao equilibrar cuidadosamente forças atrativas e repulsivas e ao incorporar sensibilidade a sinais como pH, calor, luz ou estresse mecânico, esses sistemas podem dobrar moléculas‑alvo no lugar e no momento certos. A longo prazo, esses ajudantes inteligentes poderiam tornar a produção industrial de proteínas mais eficiente, aprimorar biossensores, alimentar computadores moleculares e oferecer novas maneiras de combater doenças ligadas a proteínas mal dobradas — potencialmente incluindo condições como a doença de Alzheimer — enquanto imitam de perto o controle sutil que as células vivas já alcançam.
Citação: Zhang, W., Maruyama, A. Artificial chaperones: from conventional designs to smart systems. NPG Asia Mater 18, 12 (2026). https://doi.org/10.1038/s41427-026-00640-z
Palavras-chave: chaperonas artificiais, dobramento de proteínas, polímeros inteligentes, nanomedicina, materiais responsivos a estímulos