Clear Sky Science · pt
Enfrentando a cuproptose: do reencaminhamento metabólico à exploração terapêutica no câncer
Quando um Metal Útil se Volta Contra o Câncer
O cobre é mais conhecido como componente de fios elétricos e encanamentos, mas também circula discretamente em nossas células, ajudando enzimas a produzir energia e a nos proteger contra danos. Este artigo de revisão explora uma reviravolta surpreendente: sob condições específicas, o excesso de cobre pode levar células cancerosas a um tipo particular de morte. Compreender esse processo — chamado “cuproptose” — pode abrir novas vias para tratar tumores que escaparam às terapias padrão.
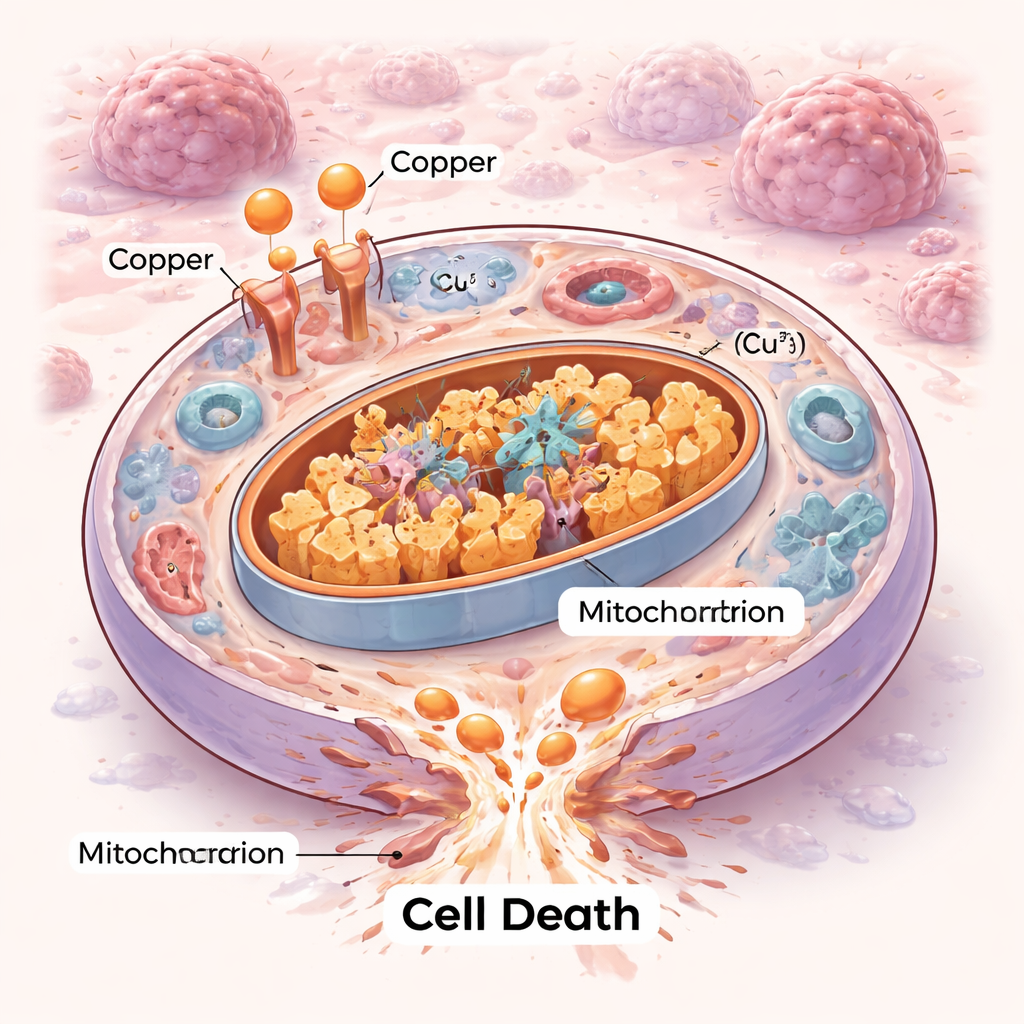
Uma Nova Forma de Morte Celular
As células não morrem todas da mesma maneira. Por décadas, os cientistas mapearam programas ordenados de autodestruição como a apoptose e formas mais recentes como a ferroptose. A cuproptose acrescenta um capítulo novo. Aqui, o excesso de cobre inunda as usinas da célula — as mitocôndrias — e se liga a enzimas metabólicas específicas que normalmente ajudam a queimar combustível. Essa ligação faz com que essas enzimas se agreguem e desestabiliza pequenos componentes ferro‑enxofre de que as mitocôndrias precisam para funcionar. O resultado é uma espécie de engarrafamento interno e colapso mecânico que a célula não consegue reparar, terminando em morte por estresse proteotóxico em vez das rotas clássicas de suicídio celular.
Como as Células Cancerosas Controlam o Cobre e a Energia
Porque o cobre é ao mesmo tempo essencial e perigoso, as células mantêm uma rede logística elaborada para movê‑lo com segurança. Transportadores dedicados trazem cobre para dentro da célula, proteínas carreadoras o escoltam até as mitocôndrias e outros destinos, e moléculas de armazenamento como metalotioneínas e glutationa neutralizam qualquer excesso. Os tumores frequentemente reconfiguram esse sistema. Alguns aumentam importadores ou chaperonas para suprir suas altas demandas energéticas; outros elevam exportadores ou proteínas de armazenamento para evitar sobrecarga de cobre. Ao mesmo tempo, muitos cânceres mudam seu metabolismo — alternando entre queima de açúcar na superfície celular e respiração mitocondrial mais profunda. A revisão explica que a cuproptose atinge com mais força células que ainda dependem amplamente das mitocôndrias, tornando tumores com esse perfil metabólico especialmente vulneráveis.
Chaves Mestres que Ajustam a Sensibilidade ao Cobre
“Tomadores de decisão” celulares importantes influenciam se a cuproptose pode ocorrer. O supressor tumoral p53, por exemplo, tende a deslocar as células da fermentação rápida de açúcar para um uso mais ordenado de combustível mitocondrial. Ao fazer isso, e ao alterar o manejo de enzimas que ligam cobre, o p53 pode tornar os cânceres mais suscetíveis à morte induzida por cobre — enquanto formas mutantes de p53 frequentemente fazem o oposto. Em contraste, o fator de hipóxia HIF‑1α, ativado em núcleos tumorais pouco oxigenados, ajuda as células a escapar da cuproptose ao reduzir enzimas mitocondriais-chave e aumentar escudos que se ligam ao cobre. Outras vias, como Wnt/β‑catenina e AKT, promovem resistência ao impulsionar a exportação de cobre ou modificar quimicamente proteínas cruciais para que elas não respondam mais à sobrecarga de cobre. Juntas, essas redes atuam como termostatos, elevando ou reduzindo a sensibilidade de um tumor a tratamentos baseados em cobre.
O Cobre, o Sistema Imune e Entregas de Fármacos Mais Inteligentes
O papel do cobre não se limita a matar células cancerosas diretamente; ele também molda a paisagem imune ao redor dos tumores. Um estresse controlado por cobre pode tornar células cancerosas moribundas mais “visíveis”, liberando sinais de perigo que recrutam e ativam células T, células dendríticas e macrófagos. O cobre também pode influenciar os níveis de pontos de verificação imune como PD‑L1, que os tumores usam para desligar células T antitumorais, sugerindo oportunidades de combinar drogas direcionadas ao cobre com imunoterapias modernas. Como o cobre livre pode prejudicar tecidos saudáveis, os pesquisadores estão desenvolvendo ferramentas de precisão — ionóforos de pequenas moléculas que levam cobre seletivamente para células cancerosas, e plataformas de nanomedicina que encapsulam cobre ou fármacos mediados por cobre em partículas ou hidrogéis direcionados. Essas tecnologias visam elevar o cobre a níveis letais dentro dos tumores mantendo o resto do corpo em uma faixa segura.
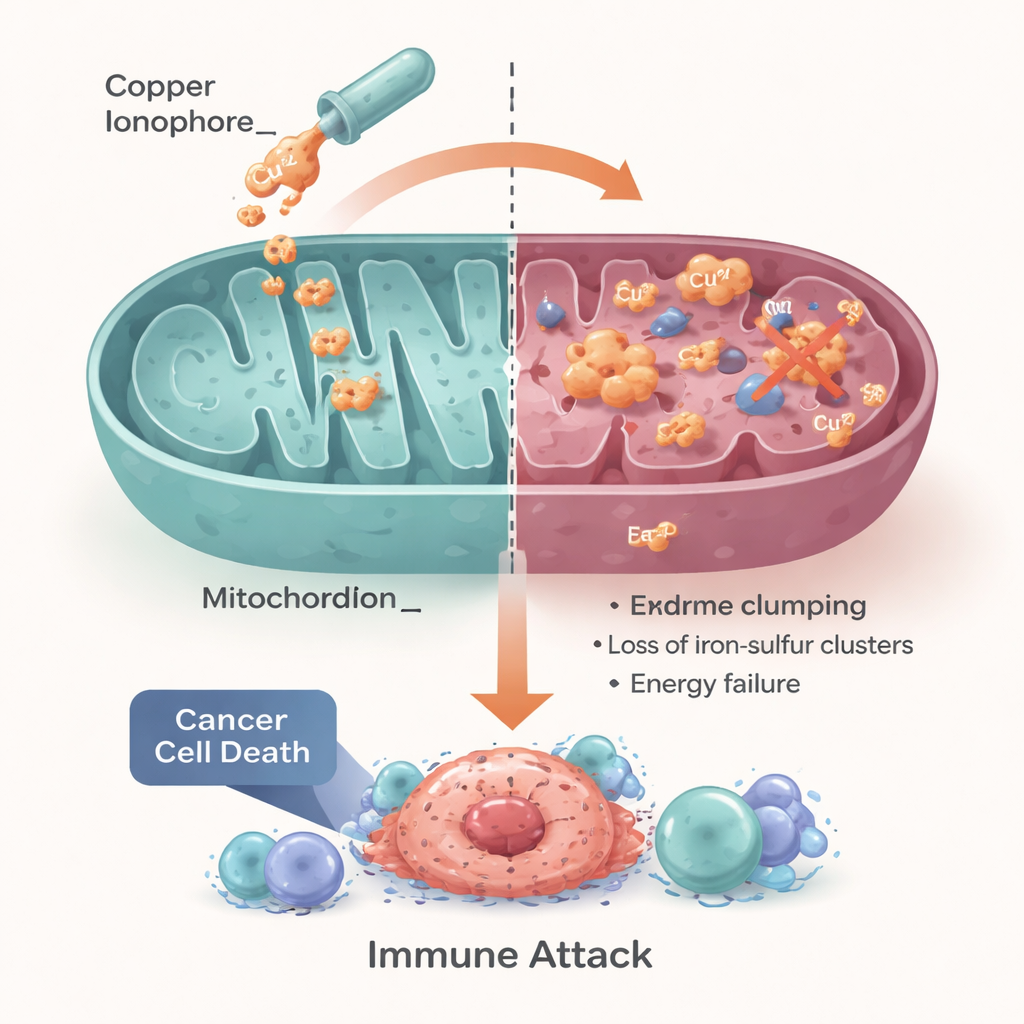
Transformando uma Fraqueza Celular em Tratamento
Os autores concluem que a cuproptose transforma uma necessidade celular básica — o manejo cuidadoso do cobre e da energia — em uma possível calcanhar de Aquiles do câncer. Cânceres com manejo de cobre perturbado ou uma dependência excessiva do metabolismo mitocondrial podem ser especialmente sensíveis a estratégias baseadas em cobre, incluindo drogas reposicionadas como dissulfiram e elesclomol, bem como nanopartículas de próxima geração. No entanto, eles enfatizam que o sucesso dependerá de combinar os pacientes certos com a abordagem adequada, usando biomarcadores que informem sobre transportadores de cobre, atividade mitocondrial e o estado imune e de oxigenação do tumor. Se esses obstáculos puderem ser superados, aproveitar a cuproptose pode dar aos oncologistas uma nova alavanca movida a metal para tratar tumores que atualmente têm poucas opções eficazes.
Citação: Hao, Q., Gan, Y. & Zhou, X. Tackling cuproptosis: from metabolic rewiring to therapeutic exploitation in cancer. Cell Mol Immunol 23, 239–260 (2026). https://doi.org/10.1038/s41423-026-01387-x
Palavras-chave: cuproptose, metabolismo do cobre, terapia contra o câncer, metabolismo tumoral, imunoterapia do câncer