Clear Sky Science · pt
Força magneto‑mecânica dinâmica em lisossomos induz repolarização duradoura de macrófagos para imunidade antitumoral
Usando Forças Suaves para Despertar o Sistema Imune
O câncer frequentemente sobrevive fazendo com que as defesas do corpo adormeçam. Este estudo explora uma maneira inesperada de despertá‑las novamente: puxando fisicamente compartimentos minúsculos dentro de células imunes com nanopartículas acionadas por campo magnético. Em vez de depender apenas de medicamentos, os pesquisadores usam forças mecânicas cuidadosamente ajustadas dentro das células para reprogramar macrófagos em combatentes tumorais de longa duração.
Por que Tumores Sólidos São Difíceis de Tratar
Imunoterapias modernas contra o câncer, como anticorpos bloqueadores de checkpoints e células imunes geneticamente modificadas, transformaram o tratamento de alguns cânceres sanguíneos. Ainda assim, para muitas pessoas com tumores sólidos, como o câncer de pulmão, essas abordagens ajudam apenas uma minoria. Uma razão principal é o microambiente tumoral. Tumores são cercados por um nicho protetor repleto de células e sinais que abafam a imunidade. Macrófagos, que podem atacar tumores (um estado semelhante a M1) ou apoiá‑los (um estado semelhante a M2), frequentemente são empurrados para o modo M2 que favorece o tumor. Inverter essa programação “ruim” de forma duradoura tem sido difícil usando apenas drogas bioquímicas convencionais.
Transformando Nanopartículas em Minúsculos Motores Mecânicos
A equipe projetou nanomotores magnéticos—partículas em escala nanométrica de óxido de ferro dopado com zinco revestidas por um polímero carregado positivamente—que são prontamente engolidos por macrófagos e acabam concentrados em lisossomos, os centros de reciclagem e sinalização da célula. Uma vez no interior, um campo magnético rotativo externo faz com que essas partículas se alinhem em cadeias semelhantes a hastes e girem, agitando o fluido viscoso dentro dos lisossomos e criando pequenos vórtices. Simulações por computador e experimentos em membranas modelo mostraram que, ao ajustar cuidadosamente a frequência de rotação, a tensão de cisalhamento na membrana lisossomal pode ser definida em um ponto ideal: forte o suficiente para tornar a membrana brevemente permeável, mas não tão forte a ponto de destruí‑la permanentemente.
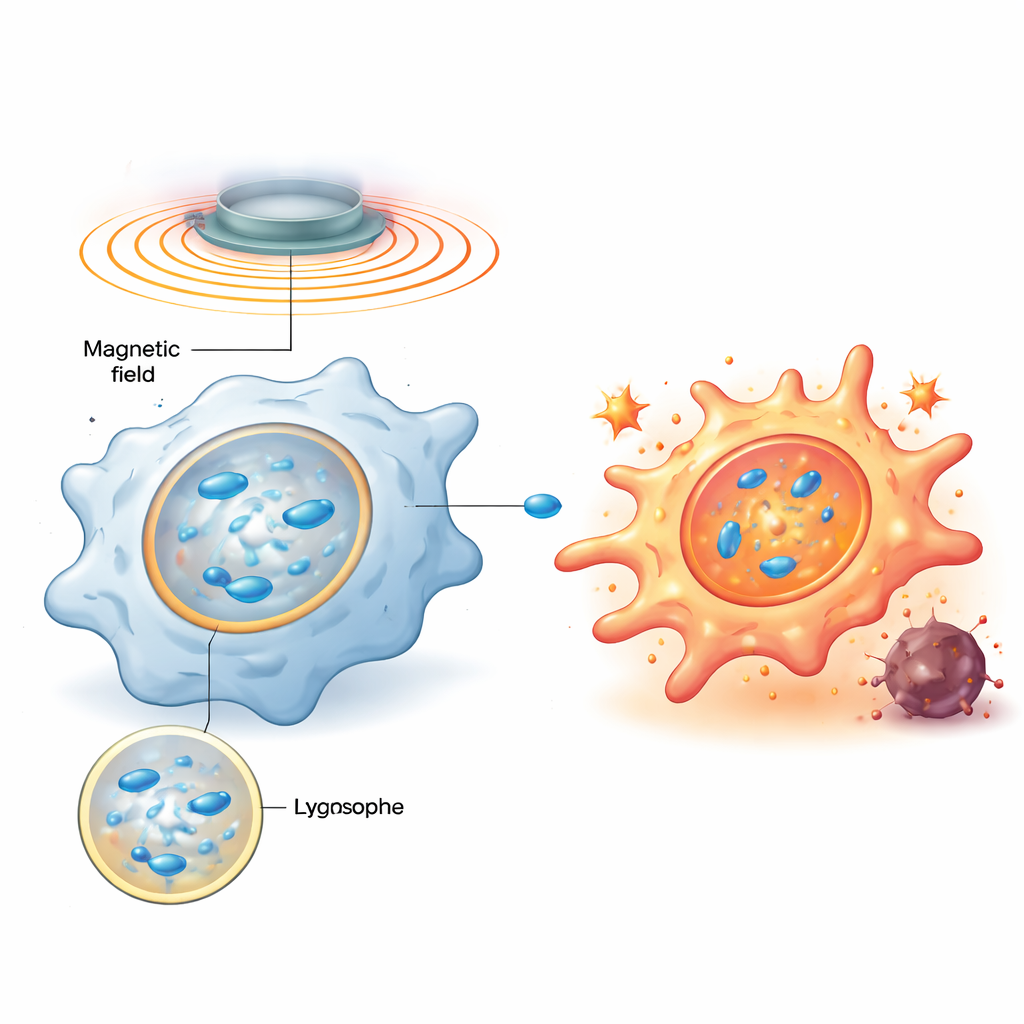
Um Empurrão Mecânico Dispara um Alarme Bioquímico
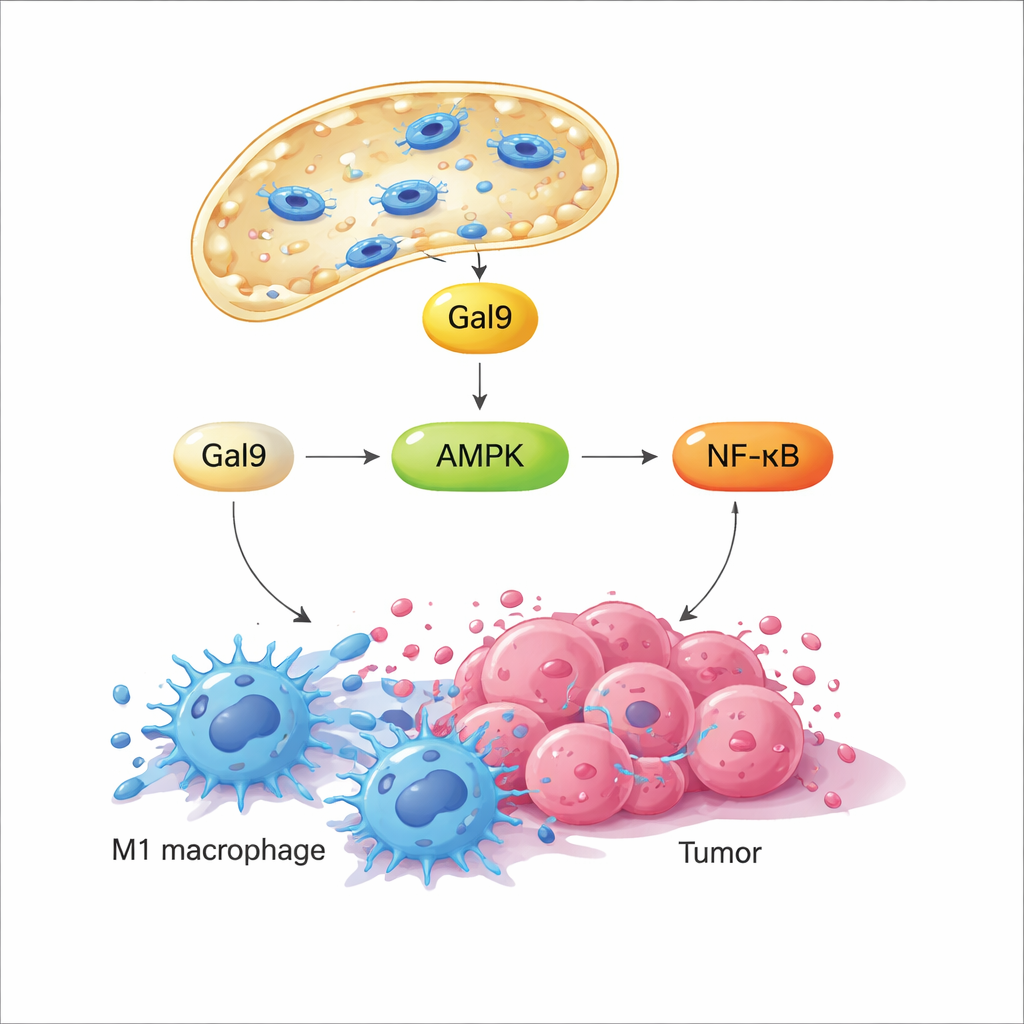
Quando a membrana lisossomal é brevemente perturbada, uma proteína ligadora de açúcares chamada galectina‑9 corre para os pontos danificados, atuando como sensor desse estresse mecânico. O estudo mostra que isso, por sua vez, ativa uma enzima chave sensora de energia, AMPK, que então impulsiona a via de sinalização NF‑κB—bem conhecida por dirigir respostas inflamatórias e antimicrobianas. Juntos, esses sinais reprogramam o metabolismo dos macrófagos, afastando‑o de um estado silencioso e eficiente em consumo de combustível para uma glicólise rápida, padrão associado a um comportamento hostil semelhante a M1. Importante, quando o campo magnético é desligado, o lisossomo se repara e a sinalização diminui; quando o campo é religado mais tarde, a mesma via é reativada. Esse ciclo programável de liga/desliga permite aos pesquisadores “acionar” repetidamente o mesmo interruptor mecânico sem matar as células.
Reeducando Macrófagos para Combater Tumores
Em cultivos celulares, essa permeabilização lisossomal induzida magneticamente—denominada MagLMP—converteu macrófagos empurrados para um estado semelhante a M2 que apoia tumores de volta para um estado pró‑inflamatório semelhante a M1. Essas células reprogramadas produziram mais citocinas inflamatórias e mantiveram seu perfil semelhante a M1 por dias, mesmo em meio de cultura derivado de tumor que normalmente as direciona para M2. Em modelos tumorais de camundongos, incorporar nanomotores magnéticos nos tumores e aplicar ciclos diários do campo rotativo retardou o crescimento de vários tipos de câncer. Quando os macrófagos foram experimentalmente depletados, o benefício desapareceu em grande parte, mostrando que essas células são centrais para o efeito do tratamento. Sequenciamento de RNA de célula única do tecido tumoral revelou ainda que a MagLMP aumentou a proporção de macrófagos semelhantes a M1, impulsionou neutrófilos antitumorais e células T CD8 efetoras, e regulou para cima genes relacionados ao NF‑κB e à glicólise dentro dos macrófagos.
Do Controle Local à Terapia Sistêmica
Os pesquisadores então perguntaram se essa abordagem poderia funcionar mais como um tratamento do mundo real, administrado pela corrente sanguínea. Eles injetaram os nanomotores por via intravenosa e usaram um imã externo simples para concentrá‑los nos tumores, demonstrando captação eficiente por macrófagos no leito tumoral. O tratamento subsequente com MagLMP novamente deslocou os macrófagos para o estado semelhante a M1 e conteve o crescimento tumoral. Em um modelo murino de câncer de pulmão em estágio inicial crescendo dentro do próprio pulmão, combinar orientação magnética com MagLMP cíclica levou a uma sobrevivência marcadamente prolongada: cerca de um terço dos camundongos tratados viveu mais de 300 dias, comparado com apenas semanas nos animais controle. Combinar MagLMP com um inibidor de checkpoint PD‑1 aumentou ainda mais o controle tumoral em modelos de difícil tratamento.
Uma Nova Maneira de Controlar a Imunidade de Dentro para Fora
Este trabalho mostra que forças mecânicas minúsculas e bem controladas dentro de um organelo específico podem ser aproveitadas para direcionar o comportamento imune em animais vivos. Ao “cutucar” repetida e reversivelmente os lisossomos, a MagLMP ativa um eixo galectina‑9–AMPK–NF‑κB que reprograma macrófagos em combatentes tumorais duradouros sem danificar amplamente as células. Para não especialistas, a ideia central é que sinais físicos—entregues por nanomotores acionados magneticamente—podem agir como um botão no sistema imune, oferecendo uma nova classe de ferramentas para complementar medicamentos em futuras imunoterapias do câncer.
Citação: Li, Y., Zheng, M., Zhu, Z. et al. Dynamic magneto-mechanical force in lysosomes induces durable macrophage repolarization for antitumor immunity. Cell Res 36, 197–218 (2026). https://doi.org/10.1038/s41422-025-01217-1
Palavras-chave: imunoterapia do câncer, reprogramação de macrófagos, nanopartículas magnéticas, mecanotransdução, sinalização lisossomal