Clear Sky Science · pt
Ativação mecânica transitória do canal Piezo1 facilita a expansão ex vivo de células-tronco hematopoéticas
Produzindo Mais Células-Tronco Sanguíneas que Salvam Vidas
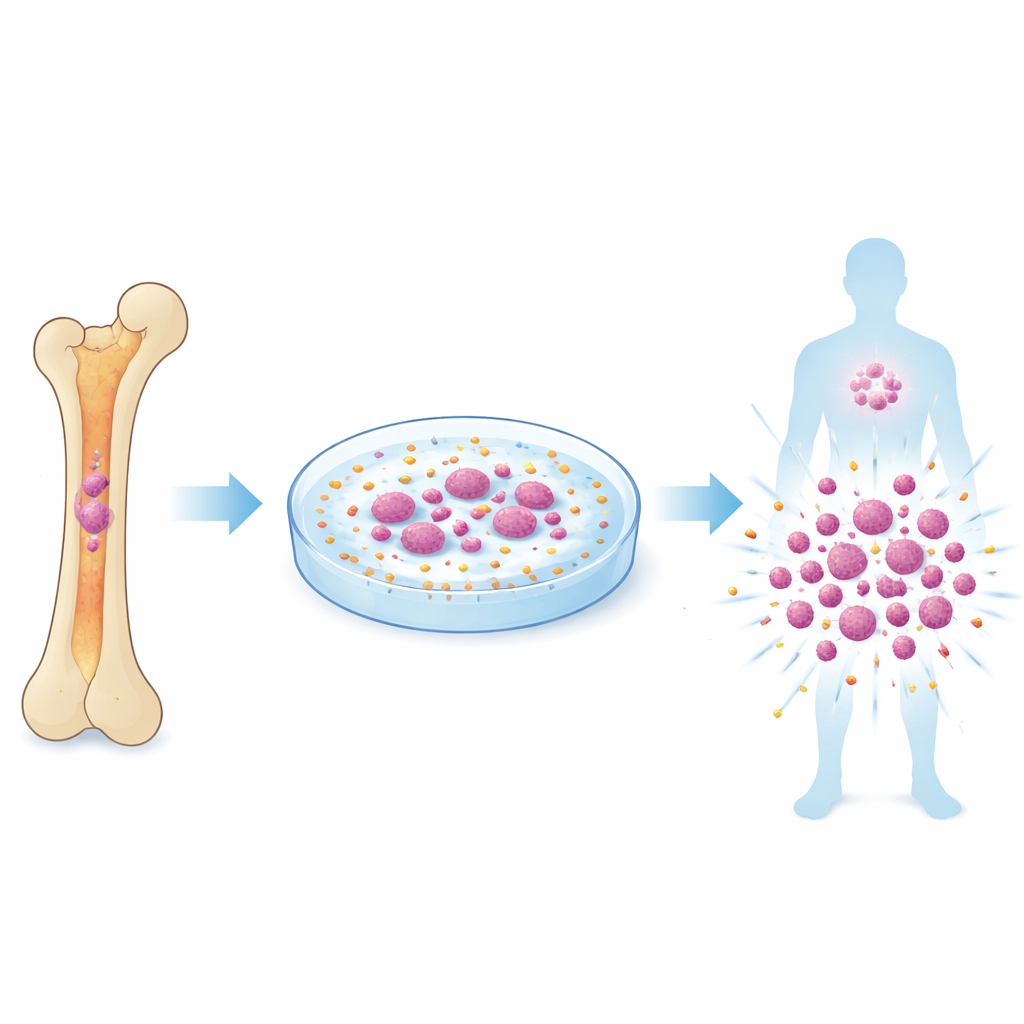
Transplantes de medula óssea podem curar certos cânceres sanguíneos e doenças hereditárias, mas os médicos frequentemente esbarram na escassez de verdadeiras células-tronco formadoras de sangue disponíveis por doador. Este estudo revela uma maneira surpreendente de cultivar essas células raras fora do corpo ao “tocar” suavemente nelas com pequenas esferas de plástico que acionam um sensor mecânico em sua superfície. O trabalho sugere uma rota nova e potencialmente mais segura para gerar células-tronco em quantidade suficiente para que mais pacientes se beneficiem do transplante.
Por que é Tão Difícil Fazer Células-Tronco Sanguíneas Crescerem
As células-tronco sanguíneas ficam no interior dos ossos e abastecem, discretamente, nossas hemácias, leucócitos e plaquetas durante toda a vida. Transplantar essas células pode redefinir um sistema sanguíneo danificado, como no tratamento da leucemia, mas só se houver células-tronco saudáveis em quantidade suficiente e se elas permanecerem totalmente funcionais. Esforços para expandi-las em placas de laboratório muitas vezes falham: as células tendem a perder a capacidade de se autorrenovar ou a perder a habilidade de reconstruir o sistema sanguíneo a longo prazo. A maioria dos métodos atuais depende de misturas de fatores de crescimento e ajustes genéticos, mas não recria totalmente o ambiente físico complexo da medula óssea, onde as células-tronco estão constantemente sujeitas a empurrões, tração e pressão.
Um Interruptor Mecânico Oculto nas Células-Tronco
Os pesquisadores focalizaram uma proteína chamada Piezo1, um canal minúsculo em forma de válvula na membrana celular que se abre quando a membrana é dobrada ou esticada, permitindo a entrada de íons cálcio e iniciando sinais internos. Ao examinar muitos tipos de células sanguíneas, encontraram que o Piezo1 é especialmente abundante nas verdadeiras células-tronco hematopoéticas. Quando eliminaram o Piezo1 geneticamente ou o bloquearam com um fármaco, as células-tronco cultivadas em placas deixaram de se expandir adequadamente e não repovoaram o sangue de camundongos após o transplante. Interessantemente, estimular continuamente o Piezo1 com ativadores químicos também foi prejudicial: as células acumulavam cálcio em excesso, produziam moléculas reativas danosas e tinham menor capacidade de enxertia. Esses resultados sugeriram que as células-tronco precisam de ativações mecânicas breves e bem temporizadas do Piezo1, e não de provocações químicas constantes.
Aproveitando Pequenas Esferas para Tocar o Sensor
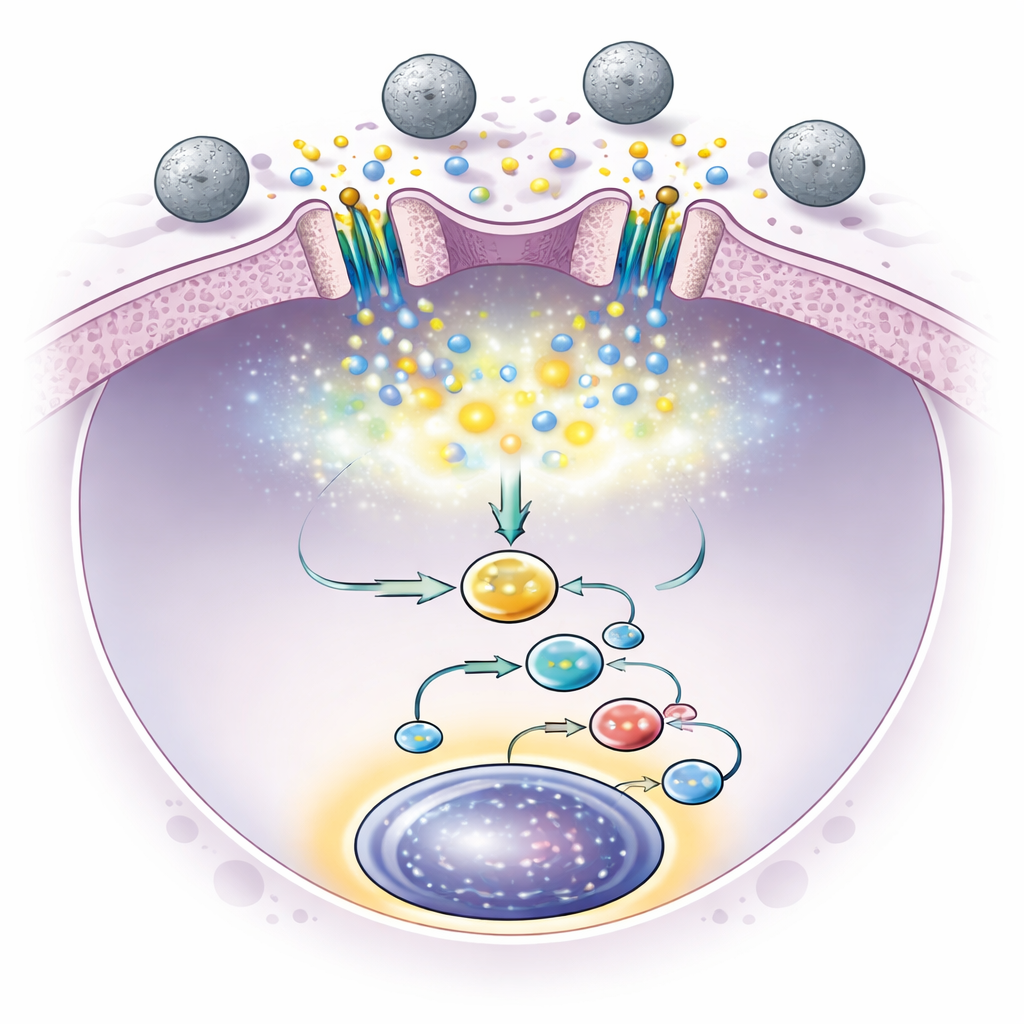
Para fornecer o impulso mecânico adequado, a equipe recorreu a esferas poliméricas microscópicas — essencialmente bolinhas de plástico lisas — que podiam colidir com as células-tronco em cultura. Testaram esferas de diferentes tamanhos e rigidez e descobriram que esferas de poliestireno de 500 nanômetros — chamadas PS500 — eram notavelmente eficazes. Quando células da medula óssea de camundongos foram cultivadas junto com essas esferas, o número de células-tronco aumentou dramaticamente, e essas células mantiveram forte capacidade de repovoamento a longo prazo em transplantes seriados através de várias gerações de camundongos. Imagens cuidadosas e medidas mecânicas mostraram que as esferas entalavam repetidamente a membrana das células com forças minúsculas, suficientes para abrir os canais Piezo1 em curtos pulsos sem sobrecarregar as células.
Do Toque Mecânico aos Sinais de Crescimento
A breve abertura dos canais Piezo1 desencadeou pequenos pulsos de entrada de cálcio nas células-tronco. Isso, por sua vez, ativou vias internas que levaram as células a produzir certas proteínas sinalizadoras, notadamente o fator de crescimento interleucina-6. A interleucina-6 então retroalimentou as próprias células-tronco e ativou uma proteína chamada Stat3 em seus núcleos, conhecida por promover a sobrevivência e a autorrenovação das células-tronco. Quando os pesquisadores bloquearam essa via do Stat3, o efeito benéfico das esferas desapareceu, confirmando que essa cadeia de eventos — toque mecânico, pulso de cálcio, liberação de interleucina-6 e ativação de Stat3 — era crucial para a expansão. Importante, após apenas um curto período de exposição às esferas, a sinalização permaneceu ativa e o número de células-tronco continuou a crescer, ressaltando que a estimulação constante não era necessária.
Promessa para Transplantes Humanos
A equipe aplicou em seguida a mesma abordagem a células-tronco sanguíneas humanas coletadas do sangue do cordão umbilical, uma fonte comum, porém muitas vezes limitada, para transplantes. Com as esferas PS500, essas células humanas se expandiram várias vezes mais do que com os melhores métodos baseados apenas em pequenas moléculas, mantendo, entretanto, sua capacidade de repovoar permanentemente o sangue de camundongos imunodeficientes. Estudos de segurança em camundongos sugeriram que as esferas não entram nas células-tronco, podem ser removidas de forma eficiente por centrifugação simples ou filtração, e não causam danos óbvios a órgãos nem anormalidades sanguíneas nas doses testadas. Isso posiciona o sistema baseado em esferas como uma tecnologia prática e potencialmente escalável para bancos de sangue e centros de transplante.
O Que Isso Pode Significar para Pacientes
Em essência, o estudo mostra que um sinal mecânico suave — entregue por esferas nanoscópicas em movimento — pode induzir as células-tronco sanguíneas a se multiplicarem preservando sua potência, ao ativar brevemente um sensor de pressão incorporado em vez de sobrecarregá-lo. Se traduzida para a clínica, essa abordagem poderia facilitar a geração de células-tronco de alta qualidade a partir de uma pequena unidade de sangue de cordão ou de um doador parcial, ampliando o acesso a transplantes curativos para muitas mais pessoas. Também destaca como prestar atenção não apenas à “sopa” química ao redor das células, mas também às sensações físicas que elas experienciam, pode desbloquear novas formas de controlar o destino celular.
Citação: Wang, Q., Zeng, X., Yang, H. et al. Transient mechanical activation of the Piezo1 channel facilitates ex vivo expansion of hematopoietic stem cells. Cell Res 36, 272–285 (2026). https://doi.org/10.1038/s41422-025-01209-1
Palavras-chave: células-tronco hematopoéticas, canais iônicos mecanossensíveis, Piezo1, microesferas de poliestireno, transplante de células-tronco