Clear Sky Science · pt
Inosina promove reprogramação metabólica de eritrócitos e restaura liberação de oxigênio para rejuvenescimento via eixo 2,3‑BPG‑PNP
Por que isso importa para o envelhecimento saudável
À medida que as pessoas envelhecem, os órgãos frequentemente não recebem oxigênio suficiente — um estresse silencioso que contribui para doenças cardíacas, perda de memória, fraqueza muscular e outros problemas ligados à idade. Este estudo faz uma pergunta simples, mas poderosa: e se parte do problema comece dentro dos glóbulos vermelhos que transportam o oxigênio, e se uma molécula natural comum chamada inosina pudesse ajudar a restaurar sua vitalidade?
Como os glóbulos vermelhos mudam com a idade
Os pesquisadores acompanharam mais de 300 adultos com idades entre 20 e 85 anos e mediram cuidadosamente quão bem seus glóbulos vermelhos liberavam oxigênio. Eles observaram um declínio constante ao longo da vida: as hemácias de pessoas mais velhas retinham o oxigênio com mais afinco e o liberavam menos para os tecidos. Essa mudança ocorreu junto com sinais de alerta em outros órgãos, incluindo pressão arterial mais alta e declínios sutis na função renal e hepática. Em camundongos, o mesmo padrão apareceu: animais mais velhos tinham glóbulos vermelhos que liberavam menos oxigênio e mostravam mais estresse oxidativo, um desgaste químico associado ao envelhecimento.
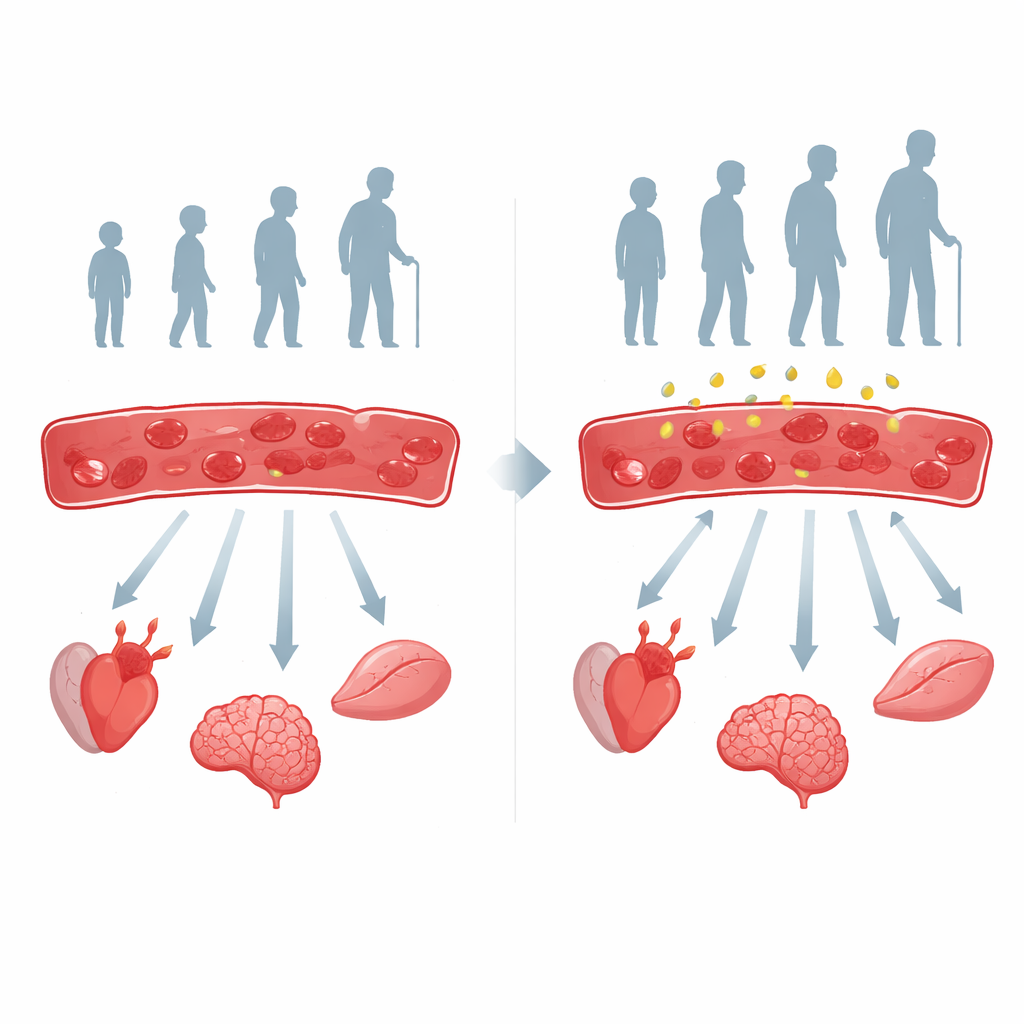
O interruptor de combustível oculto dentro das células sanguíneas
Os glóbulos vermelhos não têm núcleo nem mitocôndrias, por isso dependem de uma química interna simplificada para produzir energia e ajustar a liberação de oxigênio. Uma pequena molécula chamada 2,3‑BPG normalmente ajuda a hemoglobina a liberar oxigênio onde é necessário. A equipe descobriu que os níveis de 2,3‑BPG caem com a idade porque uma enzima que o produz, a BPGM, fica menos ativa. Em humanos e camundongos, níveis mais baixos de 2,3‑BPG acompanharam de perto a piora na liberação de oxigênio. Quando os cientistas geraram camundongos cujos glóbulos vermelhos não podiam produzir 2,3‑BPG, os animais desenvolveram hipóxia tecidual precoce, mais estresse oxidativo, músculos mais fracos, pior memória e pior controle da glicose — essencialmente um quadro de envelhecimento acelerado impulsionado apenas por mudanças nos glóbulos vermelhos.
Inosina como fonte de energia alternativa
O perfil metabólico revelou que os glóbulos vermelhos envelhecidos não apenas desaceleram; eles se reconfiguram. À medida que o manejo da glicose enfraquece, passam a queimar cada vez mais inosina, um composto natural derivado de nucleotídeos. Em pessoas e camundongos mais velhos, a enzima PNP, que quebra a inosina em um fragmento de açúcar chamado ribose‑1‑fosfato, tornou‑se mais ativa. Usando inosina marcada, os pesquisadores mostraram que esse fragmento de ribose flui para vias internas-chave que sustentam a produção de energia e, importantemente, ajudam a reconstruir 2,3‑BPG. Em experimentos in vitro, expor glóbulos vermelhos humanos ou de camundongo à inosina rapidamente aumentou sua capacidade de liberar oxigênio e reduziu espécies reativas de oxigênio danosas — desde que as células pudessem captar inosina por meio de um transportador chamado ENT1 e digeri‑la com PNP.
Testes genéticos e ensaios em animais
Para confirmar a importância desse sistema de combustível de reserva, a equipe criou camundongos cujos glóbulos vermelhos não possuíam ENT1, a porta de entrada para a inosina. Esses animais não puderam se beneficiar da inosina, apresentaram pior liberação de oxigênio, maior estresse oxidativo e mostraram declínios mais rápidos na cognição, força muscular e controle da glicose à medida que envelheciam. Os cientistas então passaram a um teste pré‑clínico: administraram injeções diárias de inosina a camundongos de meia‑idade durante um mês. Os animais tratados apresentaram glóbulos vermelhos que liberavam mais oxigênio e produziam menos oxidantes nocivos. Os camundongos correram melhor em um cilindro rotatório, tiveram pegada mais forte, desempenho superior em testes de memória e tiveram menos evidências de dano por baixo teor de oxigênio no coração, rins, músculos e em regiões cerebrais-chave envolvidas na aprendizagem e memória.
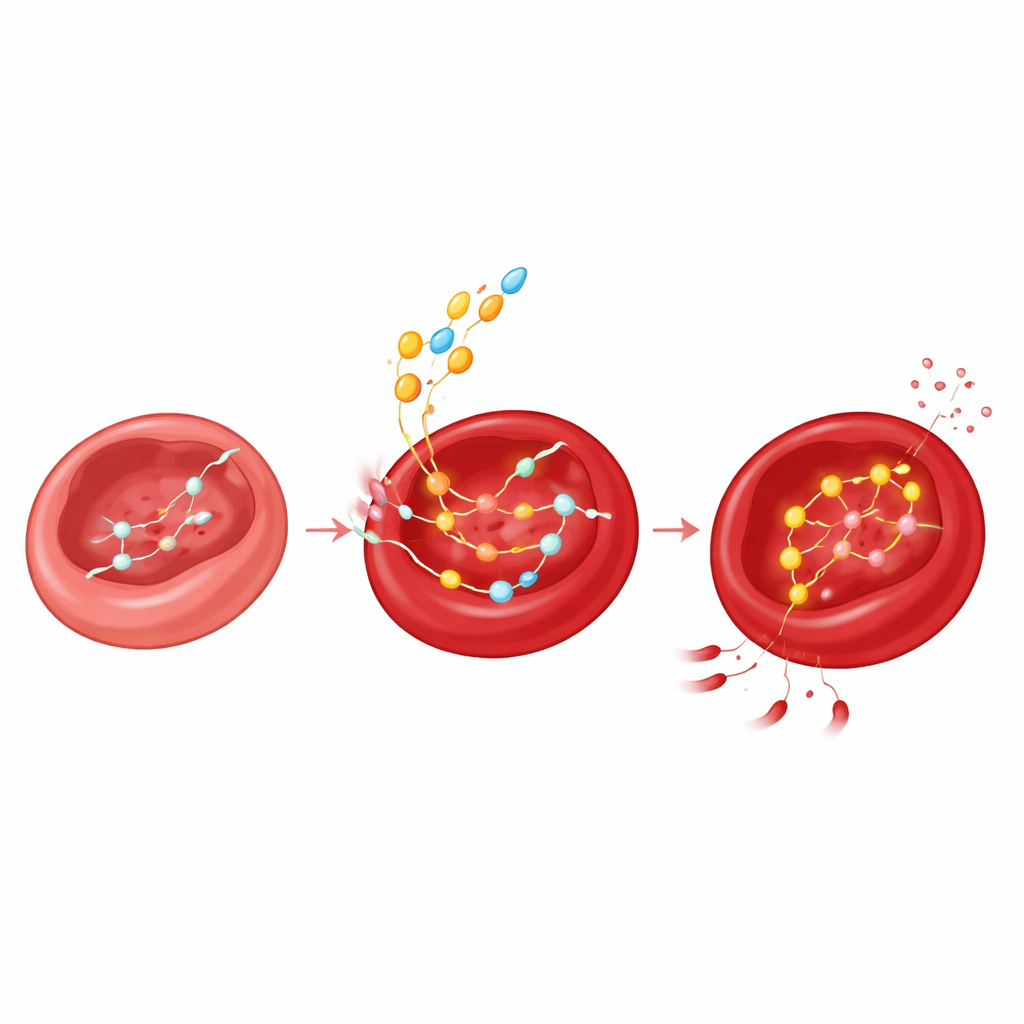
Um freio molecular que afrouxa com a idade
O estudo também revela um elegante circuito de retroalimentação. Usando modelagem molecular, ensaios enzimáticos e mutações direcionadas, os autores mostram que o próprio 2,3‑BPG se liga à PNP e bloqueia sua atividade ao competir com o fosfato em pontos de contato específicos na enzima. Na juventude, o abundante 2,3‑BPG, portanto, mantém a degradação da inosina sob controle. À medida que os níveis de 2,3‑BPG caem com a idade, esse freio se solta: a PNP torna‑se mais ativa, a inosina é consumida mais rapidamente e seu fragmento de ribose é desviado para vias produtoras de energia para compensar o metabolismo da glicose mais lento. Em outras palavras, a mesma molécula que ajuda a hemoglobina a liberar oxigênio também regula discretamente como os glóbulos vermelhos acessam uma reserva de combustível de emergência.
O que isso significa para envelhecimento e rejuvenescimento
Em conjunto, o trabalho propõe que o envelhecimento não é apenas sobre órgãos que falham, mas também sobre glóbulos vermelhos envelhecidos que entregam menos oxigênio. Uma queda na atividade da BPGM e nos níveis de 2,3‑BPG marca um novo “característico do envelhecimento”, enquanto o eixo inosina–PNP–ENT1 funciona como um sistema de resgate embutido que restaura parcialmente o fluxo de energia e a liberação de oxigênio. Ao fornecer inosina adicional externamente, pelo menos em camundongos, os pesquisadores conseguiram fortalecer esse sistema de resgate, melhorar o desempenho dos glóbulos vermelhos, aliviar a hipóxia tecidual e atenuar declínios na força e na memória. Embora muito ainda precise ser testado em humanos, o estudo levanta a possibilidade intrigante de que ajustar o metabolismo dos glóbulos vermelhos — talvez com inosina ou estratégias relacionadas — possa se tornar uma nova via para um envelhecimento mais saudável.
Citação: Liu, W., Yang, Z., Chen, C. et al. Inosine promotes erythrocyte metabolic reprogramming and restores oxygen release for rejuvenation via 2,3-BPG-PNP axis. Cell Discov 12, 19 (2026). https://doi.org/10.1038/s41421-026-00877-6
Palavras-chave: glóbulos vermelhos, envelhecimento, transporte de oxigênio, inosina, metabolismo