Clear Sky Science · pt
Bilirrubina ativa diretamente RIPK3 para induzir necroptose não clássica
Quando uma molécula útil se torna prejudicial
A bilirrubina é mais conhecida como o pigmento amarelo por trás da icterícia neonatal e da cor familiar dos hematomas. Em níveis baixos, ela contribui para proteger nossas células contra danos. Mas quando a bilirrubina se acumula no organismo e penetra no cérebro, pode provocar lesões duradouras, especialmente em recém‑nascidos e em pessoas com doença hepática grave. Este estudo revela uma surpresa: o excesso de bilirrubina pode ativar diretamente um “interruptor de morte” molecular dentro das células cerebrais, desencadeando uma forma destrutiva de morte celular e oferecendo um novo alvo para terapias futuras.
Do pigmento sanguíneo à ameaça cerebral
A bilirrubina é produzida quando o corpo recicla glóbulos vermelhos. Normalmente, o fígado a modifica e elimina, mantendo os níveis baixos e relativamente seguros. Em certas condições — como icterícia neonatal, infecções graves ou insuficiência hepática — a bilirrubina não processada pode se acumular. Por se dissolver facilmente em gorduras, essa forma “livre” pode atravessar a barreira hematoencefálica, sobretudo quando essa barreira está comprometida por doença ou inflamação. Uma vez no cérebro, a bilirrubina é conhecida por ser tóxica, mas os passos exatos de como ela danifica os neurônios permaneceram pouco claros.
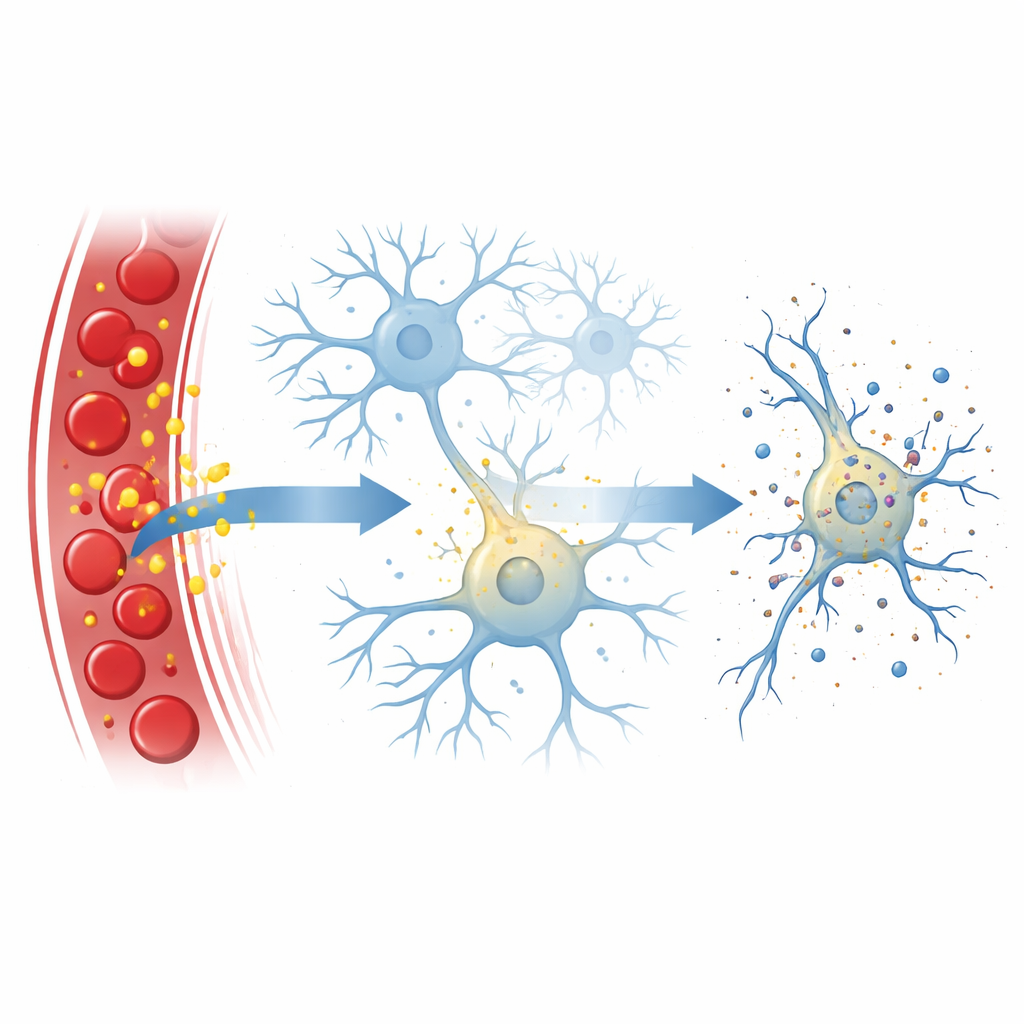
Uma explosão celular controlada
Os pesquisadores concentraram‑se na necroptose, uma forma regulada de morte celular que se assemelha a uma pequena explosão: a célula incha, sua membrana externa se rompe e seu conteúdo vaza, frequentemente desencadeando inflamação. Esse processo é normalmente conduzido por uma cadeia de proteínas, com uma chamada RIPK3 atuando como um nó central e outra, MLKL, perfurando a membrana celular. Nos modelos clássicos, a ativação de RIPK3 depende de proteínas parceiras que reconhecem sinais de perigo, como moléculas inflamatórias ou material genético viral. Aqui, a equipe descobriu que a bilirrubina pode contornar esses parceiros habituais e ainda assim induzir necroptose em células nervosas.
A bilirrubina agarra o interruptor de morte da célula
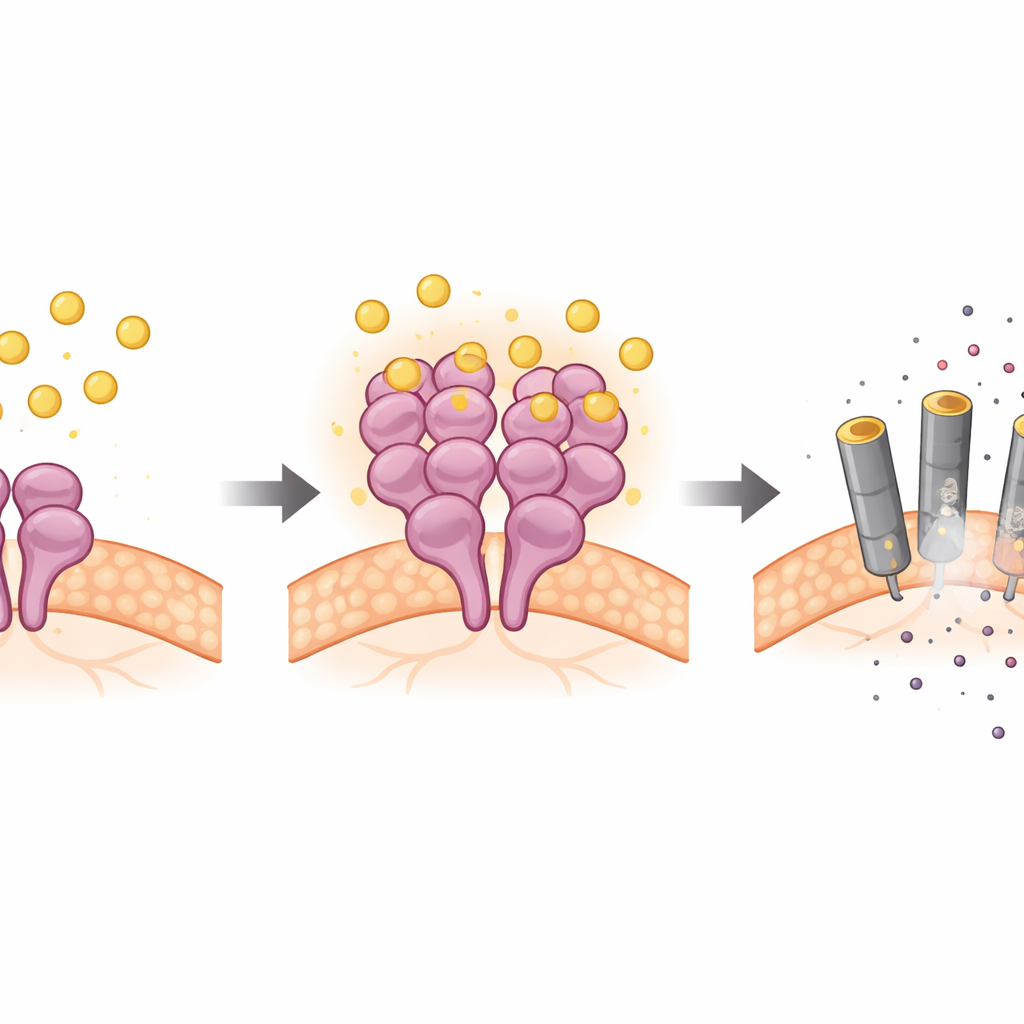
Usando neurônios em cultura, fatias cerebrais e modelos murinos, os cientistas mostraram que a bilirrubina ativa seletivamente RIPK3 e seu parceiro a jusante MLKL nos neurônios, enquanto deixa as proteínas upstream habituais em grande parte inalteradas. Experimentos genéticos revelaram que, quando RIPK3 ou MLKL foram removidos, a bilirrubina já não conseguia matar os neurônios de modo eficiente. Testes bioquímicos foram além: a bilirrubina ligou‑se fisicamente ao RIPK3 em dois pontos específicos de seu núcleo ativo, incentivou a agregação das moléculas de RIPK3 e aumentou sua atividade quinase — a função química que liga a via de morte. Essa interação direta com RIPK3 não dependia da superfície típica de interação da proteína (o domínio RHIM) nem de outros adaptadores, destacando uma via não clássica para a necroptose.
Evidências vindas do cérebro vivo
Para avaliar se esse mecanismo tem relevância em animais inteiros, a equipe elevou os níveis de bilirrubina em camundongos, seja injetando‑a no cérebro, seja induzindo lesão hepática e inflamação para que a bilirrubina naturalmente chegasse ao cérebro. Em camundongos normais, isso levou a forte ativação de RIPK3 e MLKL em regiões cerebrais vulneráveis, aumento de marcadores de morte celular e perda visível de neurônios saudáveis. Camundongos geneticamente desprovidos de RIPK3 foram protegidos: seus neurônios mostraram muito menos dano, menos sinais de morte e respostas inflamatórias reduzidas, apesar dos mesmos níveis elevados de bilirrubina. Importante, uma forma processada e solúvel em água da bilirrubina — geralmente considerada inofensiva — não ativou RIPK3 nem causou lesão cerebral semelhante, reforçando que a forma lipossolúvel não modificada é a verdadeira culpada.
O que isso significa para os pacientes
Este trabalho revela que o excesso de bilirrubina não conjugada pode ativar diretamente RIPK3, desencadeando uma ruptura controlada, porém destrutiva, das células cerebrais por necroptose. Em vez de agir apenas como um veneno geral ou fonte de estresse oxidativo, a bilirrubina funciona como um ativador de pequena molécula de um programa de morte específico em neurônios e células imunes cerebrais. Para pacientes com icterícia severa ou insuficiência hepática, isso sugere que bloquear RIPK3 ou MLKL — especialmente com fármacos capazes de penetrar no cérebro — pode algum dia ajudar a limitar o dano neurológico. Em termos simples, o estudo mostra como um pigmento normalmente útil pode se tornar um assassino molecular preciso e aponta novas formas de neutralizá‑lo sem comprometer suas funções protetoras cotidianas.
Citação: Xue, Q., Ma, X., Chen, Z. et al. Bilirubin directly activates RIPK3 to induce non-classical necroptosis. Cell Discov 12, 21 (2026). https://doi.org/10.1038/s41421-026-00876-7
Palavras-chave: neurotoxicidade da bilirrubina, necroptose, RIPK3, insuficiência hepática e lesão cerebral, vias de morte celular