Clear Sky Science · pt
Pipeline integrativa de perfilamento espacial para determinar arquiteturas do TME em amostras clínicas arquivadas usando a tecnologia superplex CmTSA
Por que a paisagem oculta ao redor dos tumores importa
Os cânceres não crescem isoladamente. Eles estão rodeados por um vizinhança movimentada de células imunes, células de suporte, vasos sanguíneos e tecido fibrótico que, juntos, formam o “microambiente” tumoral. Este trabalho apresenta uma maneira prática de mapear essa paisagem oculta em detalhe usando amostras de tecido padrão de hospitais. Ao revelar que tipos de células ficam próximas umas das outras e como se organizam em vizinhanças úteis ou prejudiciais, o método pode ajudar médicos a prever melhor como o câncer de um paciente vai se comportar e quais tratamentos têm maior probabilidade de funcionar.
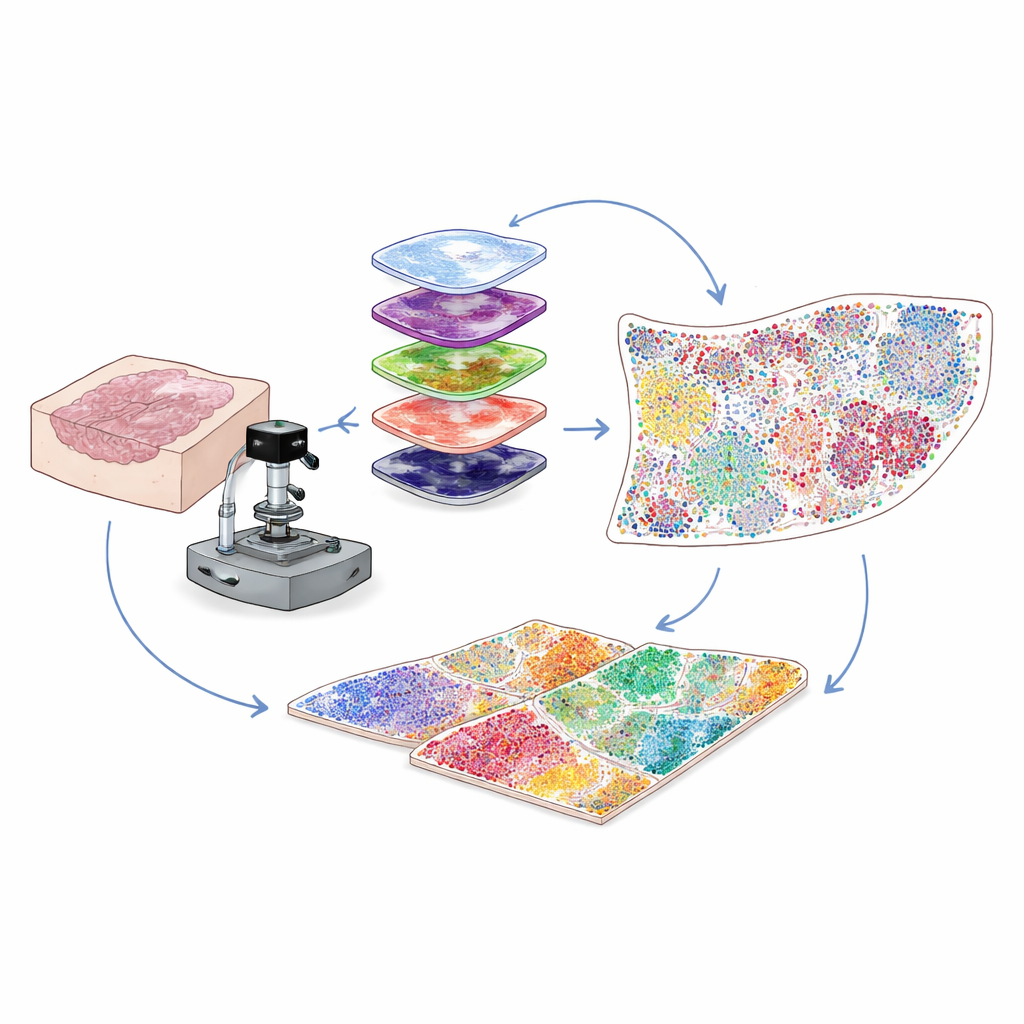
Ver mais em amostras hospitalares corriqueiras
A maioria das amostras clínicas de câncer é preservada como fatias finas de tecido embebido em parafina, conhecidas como blocos FFPE, que podem ser armazenadas por anos. Elas são uma mina de ouro para pesquisa, mas um problema técnico tem limitado os cientistas: essas amostras emitem fluorescência de fundo natural que afoga os sinais fracos de muitas proteínas importantes. Os autores resolveram isso combinando luz intensa, cuidadosamente ajustada, com um tratamento químico suave para apagar seletivamente esse brilho de fundo sem danificar o tecido ou os alvos proteicos. Esse passo híbrido de “clareamento” óptico e químico aumenta de forma nítida a clareza da imagem, permitindo detectar sinais proteicos fracos que, de outra forma, seriam perdidos.
Pintando dezenas de marcadores proteicos na mesma lâmina
Para entender quais células estão presentes e o que elas estão fazendo, cientistas coram tecidos com anticorpos que se ligam a proteínas específicas. Métodos multiplex tradicionais ou têm dificuldade com sinais fracos de proteínas raras ou só conseguem rastrear um número limitado de marcadores por vez. Aqui, a equipe usa uma abordagem chamada amplificação cíclica do sinal por tyramida. Em cada rodada, um pequeno conjunto de marcadores é corado e “desenvolvido” enzimaticamente em pontos fluorescentes brilhantes e permanentemente ligados. Os anticorpos são então removidos suavemente enquanto o sinal permanece, o fundo é novamente clareado, e o próximo conjunto de marcadores é aplicado. Repetindo esse ciclo muitas vezes e alinhando as imagens usando o sinal constante dos núcleos celulares, eles conseguem visualizar de forma confiável de 30 a 60 proteínas diferentes em uma única fatia de tecido, em toda uma lâmina, com resolução de célula única.
Convertendo imagens coloridas em um atlas célula a célula
Imagens de alto plex contêm milhões de pixels, muito mais do que um humano poderia analisar a olho nu. Os autores, portanto, constroem um pipeline de visão computacional que primeiro encontra e contorna cada núcleo celular usando ferramentas de deep learning originalmente desenvolvidas para segmentação celular geral. Em seguida, com base em onde a fluorescência de cada proteína aparece — na membrana, no citoplasma ou no núcleo — e em conjuntos de regras lógicas, cada célula é atribuída a um tipo ou subtipo, como célula tumoral, célula T helper, célula T citotóxica, célula B, fibroblasto ou outras. A saída é uma tabela digital que lista, para cada célula na lâmina, sua identidade e suas coordenadas exatas. Isso transforma uma imagem complexa em um mapa quantitativo de quem está onde dentro do microambiente tumoral.
Revelando vizinhanças celulares que influenciam o desfecho
Células raramente atuam isoladas; o que importa é quem são seus vizinhos. Para capturar isso, os pesquisadores testam diferentes maneiras de definir vizinhanças locais ao redor de cada célula e adotam uma abordagem de rede baseada em raio. Imagine desenhar um pequeno círculo — cerca da espessura de um fio de cabelo humano — ao redor de cada célula e listar quem vive dentro dele. Agrupando células cujos círculos ao redor têm misturas semelhantes de vizinhos, o método identifica “nichos funcionais” recorrentes, como zonas ricas em células imunes, barreiras ricas em fibroblastos ou regiões dominadas por tumor. Aplicando essa estratégia a tecido de cólon mostra que vizinhanças baseadas em raio se alinham melhor com estruturas anatômicas conhecidas do que métodos alternativos. Em amostras de câncer cervical de pacientes com desfechos bons versus ruins, a equipe observa que nichos ricos em células imunes se agrupam perto da borda tumoral em pacientes com bom prognóstico, enquanto pacientes com desfecho pior exibem zonas espessas e densas em fibroblastos que cercam as células tumorais e parecem isolar as células imunes atacantes.
De mapas espaciais a tratamentos personalizados
Ao combinar coloração de alta qualidade e acessível para muitas proteínas com análise de imagem robusta, este trabalho entrega um pipeline completo que pode ser aplicado a grande número de amostras hospitalares padrão. O método transforma tecido preservado em mapas detalhados de como células tumorais, imunes e estromais se arranjam e interagem. Para leitores leigos, a conclusão é que não apenas os tipos de células, mas seus padrões precisos de vizinhança importam para como um câncer se comporta. Esta plataforma pode ajudar pesquisadores a localizar pontos quentes imunes protetores, identificar barreiras celulares supressoras e, em última instância, apoiar prognósticos mais precisos e estratégias de imunoterapia mais afinadas.
Citação: Xiao, C., Zhou, R., Chen, Q. et al. Integrative spatial profiling pipeline for determining TME architectures in archival clinical specimens using CmTSA superplex technology. Cell Discov 12, 16 (2026). https://doi.org/10.1038/s41421-026-00874-9
Palavras-chave: microambiente tumoral, proteômica espacial, imagem multiplex, imunologia do câncer, análise de célula única