Clear Sky Science · pt
O contexto epigenético define a atividade transcricional dos sinais canônicos e não canônicos de NF-κB no câncer de pâncreas
Por que este estudo importa para pacientes
O câncer de pâncreas é um dos mais letais, em parte porque suas células são hábeis em perceber e responder a sinais de perigo no entorno. Este estudo investiga dois desses sinais, chamados TNFα e TWEAK, e mostra como eles ativam diferentes “modos de leitura” no DNA das células cancerosas. Entender esses modos pode abrir caminhos para desacelerar o crescimento tumoral, limitar a disseminação e tornar os tratamentos mais eficazes.
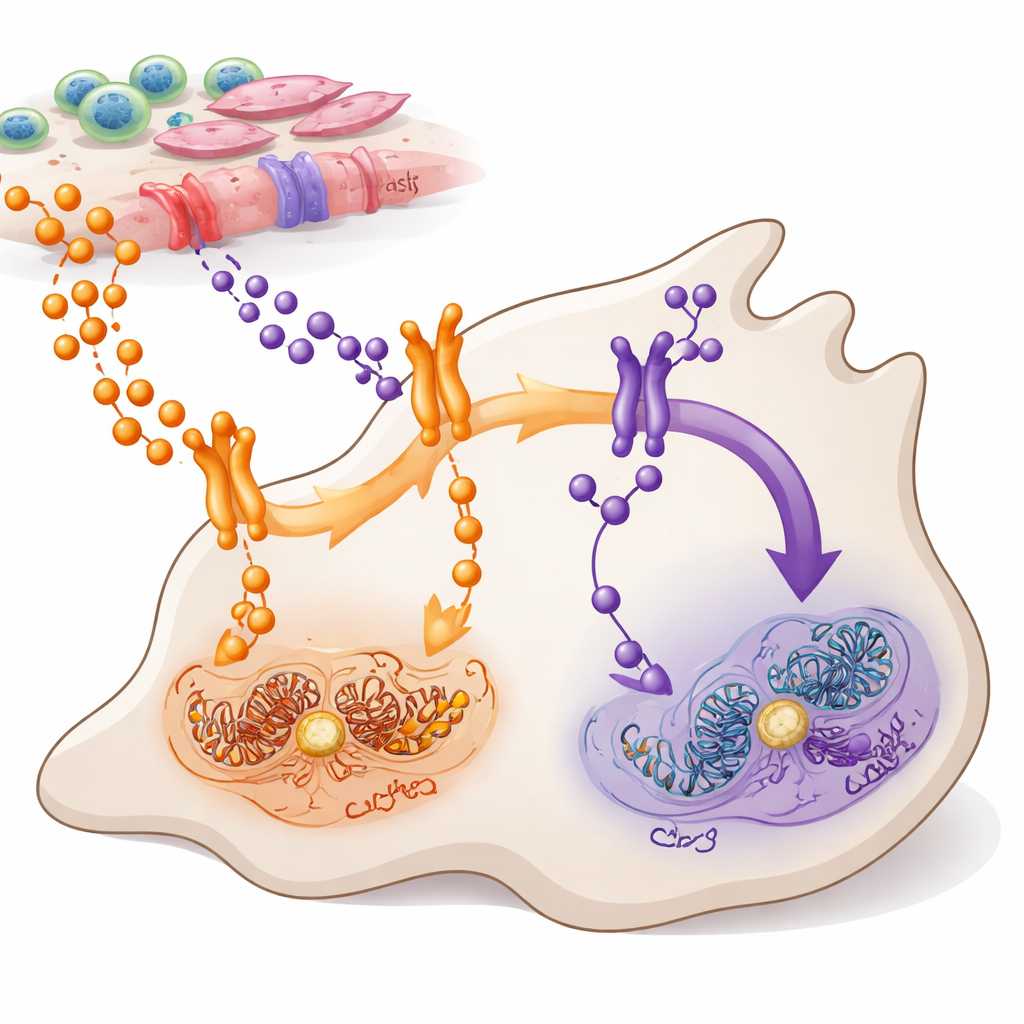
Duvas rotas de mensagem para dentro das células tumorais
TNFα e TWEAK são pequenas proteínas mensageiras liberadas por células dentro e ao redor de um tumor. Ambas se comunicam com um sistema de controle importante dentro das células conhecido como NF-κB, que ajuda a decidir se as células crescem, migram ou morrem. Os autores focaram no adenocarcinoma ductal pancreático, a forma mais comum e agressiva do câncer de pâncreas, em que o NF-κB está anormalmente ativo na maioria dos tumores. Eles mapearam quais células produzem TNFα e TWEAK, quais células carregam seus receptores e como esses sinais fluem por dois ramos relacionados do NF-κB — frequentemente chamados de via canônica (via RELA) e não canônica (via RELB).
Quem envia os sinais na vizinhança do tumor
Ao combinar sequenciamento de RNA de célula única de milhares de células de tumores de pacientes com microscopia avançada, a equipe descobriu que TNFα vem principalmente de células imunes, especialmente macrófagos e certos linfócitos T e B. TWEAK, em contraste, é produzido por um elenco mais amplo: macrófagos, fibroblastos, células endoteliais e células estreladas. Seus receptores também diferem. Células tumorais e fibroblastos próximos expressam fortemente o principal receptor de TNFα e o receptor chave de TWEAK. Análises de rede sugeriram que a sinalização baseada em TWEAK forma uma teia de comunicação mais ampla e complexa entre células tumorais e de suporte, enquanto a sinalização por TNFα é mais focada em áreas ricas em células imunes.
Profundidades diferentes de resposta dentro das células tumorais
Em linhagens de câncer de pâncreas, os pesquisadores trataram as células com TNFα ou TWEAK e mediram quais genes eram ativados ao longo do tempo. TNFα desencadeou uma onda rápida e ampla de atividade gênica ligada à inflamação, movimento celular, remodelamento tecidual e sobrevivência. TWEAK induziu um conjunto menor e mais lento de alterações que em grande parte se sobrepunham aos alvos de TNFα em vez de iniciar um programa único. Ambos os sinais puderam promover migração celular e, em certas condições, morte celular, mas TNFα teve efeito mais forte sobre a mobilidade. Ao examinar dados de tumores de pacientes do The Cancer Genome Atlas, a equipe observou que tumores com níveis altos de TNFα ou TWEAK compartilhavam muitos genes ativados, confirmando esses padrões em cânceres humanos reais.
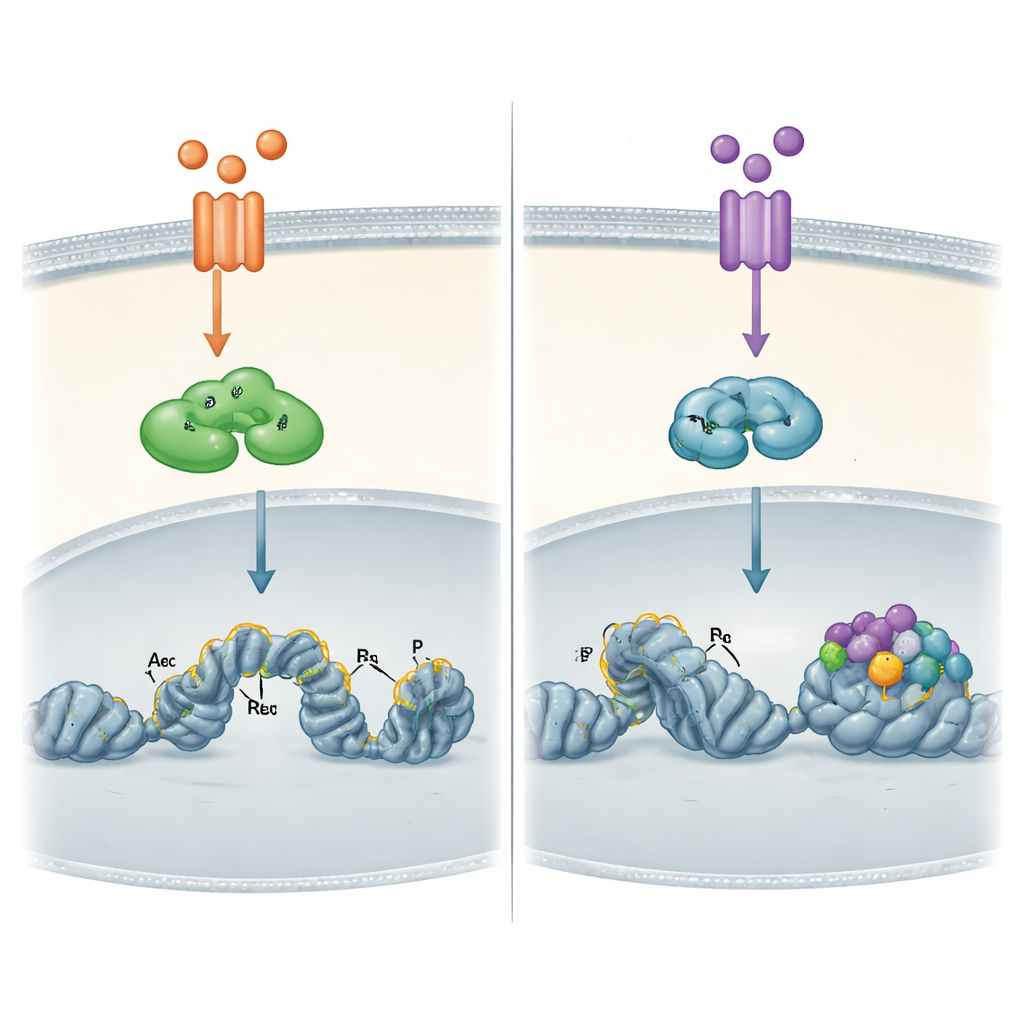
Como o panorama do DNA molda cada via
As diferenças mais marcantes surgiram quando os autores olharam diretamente para a cromatina das células cancerosas — a forma compacta do DNA e suas proteínas associadas. Usando mapas de ligação em todo o genoma, mostraram que RELA ativado por TNFα pode ligar-se não apenas a regiões de DNA já abertas, mas também a regiões mais compactas e então ajudar a “abrí‑las” adicionando marcas químicas associadas a interruptores ativos. RELB, ativado mais tardiamente por TWEAK, ligou‑se quase exclusivamente a sítios que já eram acessíveis e decorados com essas marcas ativas. Esses sítios de RELB eram especialmente ricos em motivos de ancoragem para outra família de fatores, AP‑1, sugerindo que o RELB depende de outras proteínas para preparar o terreno antes de poder agir.
O que isso significa para tratamentos futuros
Para um público não especializado, a conclusão principal é que TNFα e TWEAK usam a mesma caixa de ferramentas do NF‑κB de maneiras muito diferentes. TNFα, por meio de RELA, se comporta como um interruptor mestre que pode forçar a abertura de trechos fechados do DNA da célula cancerosa e ativar uma ampla gama de genes envolvidos em crescimento, sobrevivência e disseminação. TWEAK, por meio de RELB, é mais como um especialista que só pode atuar onde o DNA já está aberto e onde co‑fatores como AP‑1 estão presentes. Essa divisão de tarefas sugere que fármacos que visem remodelamento da cromatina, AP‑1 ou ramos específicos do NF‑κB poderiam reduzir seletivamente programas gênicos prejudiciais no câncer de pâncreas, preservando outras funções.
Citação: Aggrey-Fynn, J.E., Busch, J., Saul, D. et al. Epigenetic context defines the transcriptional activity of canonical and noncanonical NF-κB signaling in pancreatic cancer. Cell Death Discov. 12, 152 (2026). https://doi.org/10.1038/s41420-026-03019-9
Palavras-chave: câncer de pâncreas, sinalização NF-kappaB, microambiente tumoral, regulação epigenética, TNF e TWEAK