Clear Sky Science · pt
Aproveitando a piroptose na terapia do câncer de mama: mecanismos imunológicos e estratégias emergentes de biomateriais
Transformando a morte celular em uma nova arma contra o câncer de mama
O câncer de mama continua sendo um dos tipos mais comuns e difíceis de tratar no mundo. Muitos tumores acabam escapando à cirurgia, quimioterapia e até às imunoterapias modernas. Esta revisão explora uma ideia emergente: desencadear deliberadamente uma forma inflamável de morte celular chamada piroptose dentro dos tumores mamários. Ao fazer as células cancerosas se romperem de maneira controlada e inflamatória, os cientistas esperam tanto matar o tumor diretamente quanto estimular o sistema imunológico a participar do ataque.
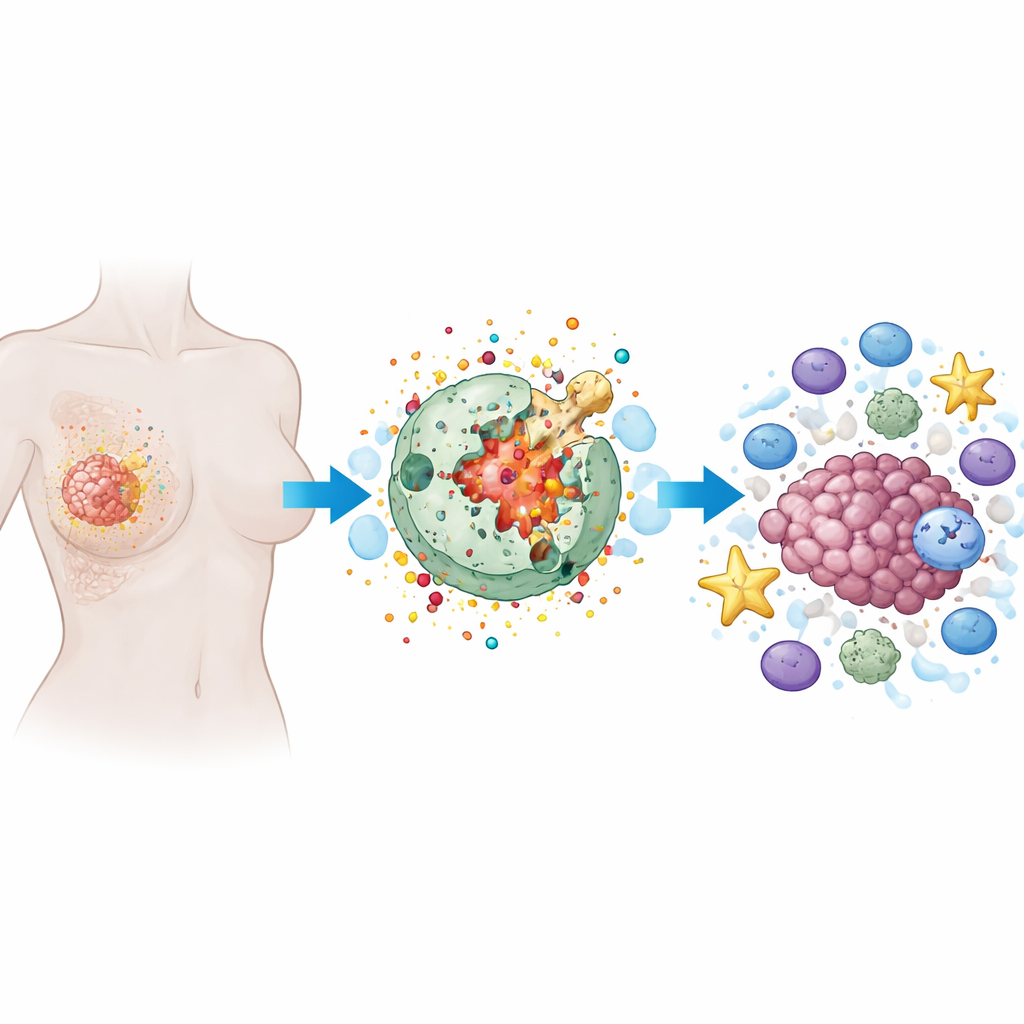
Como funciona uma forma inflamável de morte celular
A piroptose é uma forma programada de morte celular na qual a célula incha, sua membrana externa fica cheia de poros e ela finalmente se rompe, derramando seu conteúdo. Ao contrário da morte celular silenciosa e organizada observada em muitas terapias, a piroptose é barulhenta e inflamatória. Proteínas especializadas, especialmente uma família chamada gasderminas, agem como pequenos cargas de demolição. Uma vez cortadas por enzimas internas, as gasderminas perfuram a membrana celular. Isso não apenas destrói a célula cancerosa, mas também libera sinais de alarme e moléculas inflamatórias que podem convocar e ativar células do sistema imune.
Por que os tumores mamários são um desafio especial
O câncer de mama não é uma única doença, mas uma coleção de subtipos com comportamentos distintos. Alguns, como o câncer de mama triple‑negative, carecem de alvos farmacológicos comuns e frequentemente resistem ao tratamento. Muitos tumores mamários são considerados “imunologicamente frios”, ou seja, têm poucas células imunes ativas no interior. A revisão explica como características do microambiente tumoral mamário — incluindo células do estroma, células imunossupressoras e faltas locais de oxigênio — podem tanto preparar o terreno para a piroptose quanto, se mal controladas, transformar sua inflamação em combustível para o crescimento e a disseminação do tumor. Essa natureza de dois gumes torna a precisão especialmente importante.
Os interruptores de gasdermina dentro das células tumorais
Um tema central do artigo é como diferentes proteínas gasdermina atuam como interruptores moleculares dentro das células do câncer de mama. Versões como GSDMD e GSDME podem converter sinais vindos de quimioterapia, radiação ou células imunes atacantes em uma piroptose completa. Outras, como GSDMC e algumas formas de GSDMB, estão frequentemente elevadas em tumores agressivos e podem tanto promover quanto restringir a doença, dependendo de como são ativadas. Muitos cânceres de mama silenciam quimicamente a GSDME, atenuando a piroptose e a ativação imune. Restaurar ou ativar seletivamente as gasderminas corretas pode determinar se uma terapia apenas mata algumas células ou transforma todo o tumor em uma vacina in situ que alerta o sistema imune.
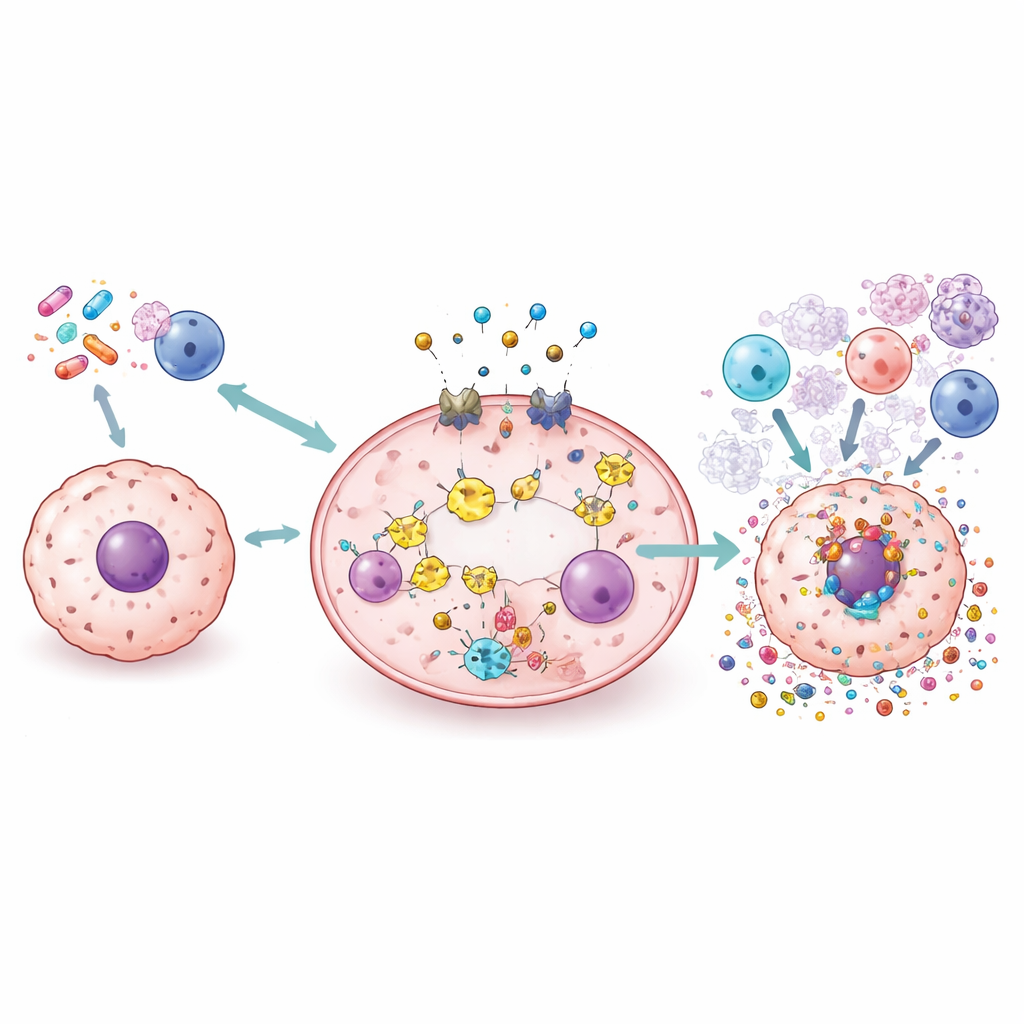
Novas ferramentas: drogas, nanopartículas, vírus e radiação
A revisão percorre uma ampla gama de estratégias em estudo para aproveitar a piroptose com segurança. Medicamentos convencionais como cisplatina e doxorrubicina podem ser reaproveitados ou reformulados para empurrar as células cancerosas em direção ao rompimento mediado por gasdermina em vez da morte silenciosa. Pequenas moléculas podem amplificar ou bloquear partes da via para ajustar finamente a inflamação. Nanopartículas e transportadores biomiméticos estão sendo projetados para entregar quimioterápicos, íons de cobre ou moléculas ativadas por luz diretamente nos tumores, onde desencadeiam piroptose poupando os tecidos saudáveis. Vírus oncolíticos e a radioterapia também podem ser projetados ou combinados com outros agentes para provocar piroptose e remodelar a paisagem imune do tumor, potencialmente tornando os inibidores de checkpoint imune mais eficazes.
Equilibrando benefícios potentes com riscos reais
Como a piroptose é altamente inflamatória, as mesmas respostas que ajudam o sistema imunológico a combater o câncer também podem danificar tecidos normais ou até promover o crescimento tumoral se se tornarem crônicas. Os autores destacam biomarcadores iniciais — como assinaturas gênicas, padrões de metilação, fragmentos de proteínas gasdermina no sangue e perfis de citocinas — que podem ajudar a identificar quais pacientes têm maior probabilidade de se beneficiar e quem está em risco maior de perigosas “tempestades de citocinas”. Projetos avançados de nanomedicina, combinações de drogas cuidadosamente escolhidas e monitoramento em tempo real de marcadores inflamatórios estão sendo explorados para manter a resposta eficaz, porém controlada.
O que isso pode significar para pacientes futuros
Em termos simples, esta revisão argumenta que fazer as células cancerosas “morrerem alto” pode transformar o cuidado do câncer de mama. Ao desencadear a piroptose em um subgrupo preciso de células tumorais, os médicos podem tanto reduzir o tumor quanto despertar uma resposta imune poderosa e duradoura, tornando tumores frios mais quentes e mais responsivos às imunoterapias modernas. Ainda assim, a piroptose é uma aliada volátil: se liberada de forma muito ampla ou prolongada, pode agravar a inflamação ou favorecer células resistentes. Pesquisas futuras se concentrarão em mapear quem se beneficiará, aperfeiçoar sistemas de entrega direcionada e realizar ensaios clínicos que combinem abordagens indutoras de piroptose com drogas imunes. Se esses desafios forem superados, aproveitar a piroptose poderá adicionar uma nova e potente dimensão ao tratamento do câncer de mama.
Citação: Asiedu, R.K.F., Souley Abdou, M., Wei, R. et al. Harnessing pyroptosis in breast cancer therapy: immunological mechanisms and emerging biomaterial strategies. Cell Death Discov. 12, 157 (2026). https://doi.org/10.1038/s41420-026-02996-1
Palavras-chave: piroptose, câncer de mama, gasdermina, microambiente tumoral, nanomedicina