Clear Sky Science · pt
Dinâmica absoluta e estática relativa: a relação entre glicólise e OXPHOS no desenvolvimento do câncer
Por que as escolhas energéticas do câncer importam
As células cancerosas são como atletas de resistência extremos: precisam constantemente se abastecer para crescer, se espalhar e escapar do tratamento. Esta revisão explica como as células tumorais acessam dois sistemas energéticos principais — um rápido e outro eficiente — e, mais importante, como elas combinam e alternam entre eles. Compreender essas estratégias energéticas em mutação oferece uma nova forma de pensar sobre o diagnóstico e o tratamento do câncer ao longo de todo o curso da doença.
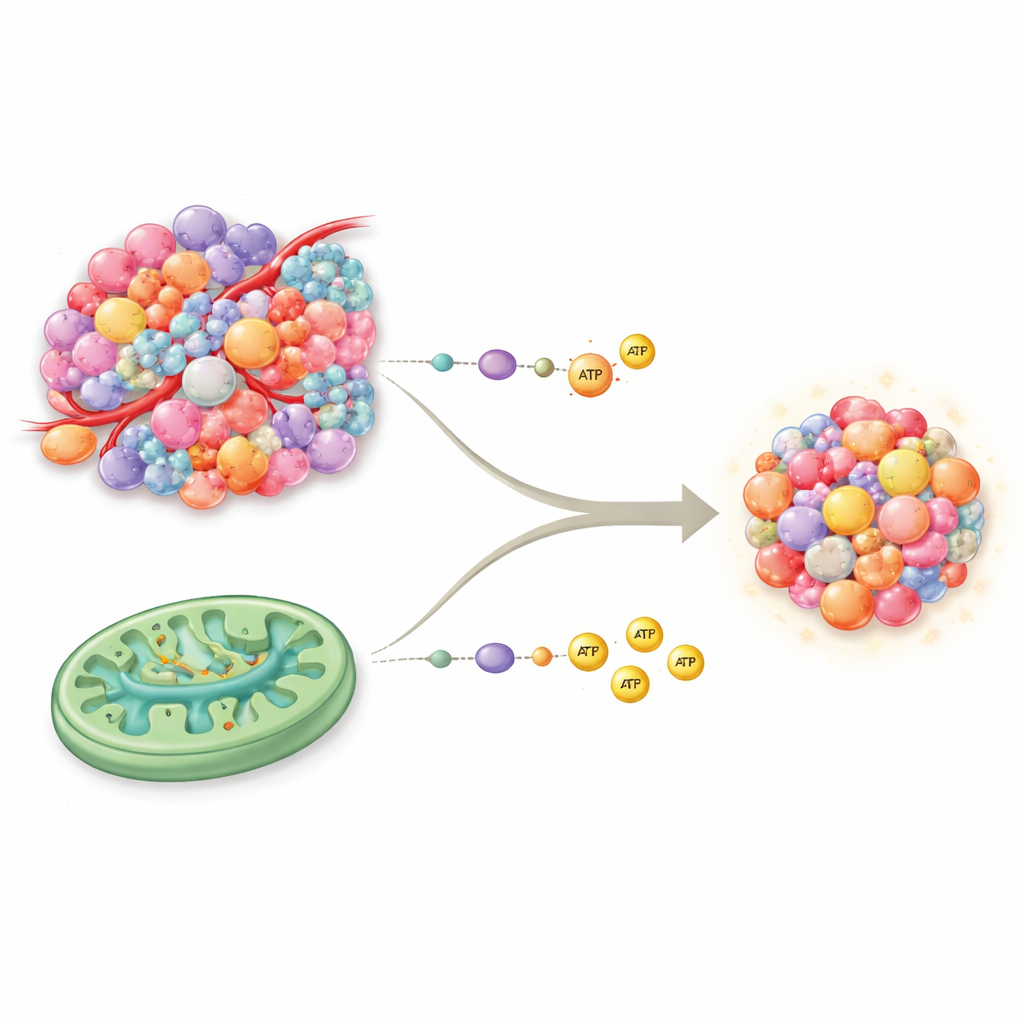
As duas principais vias de produção de energia celular
Normalmente, nossas células geram energia por duas rotas centrais. A glicólise é o sistema rápido, “dinheiro no bolso”, que quebra açúcar rapidamente, mas produz relativamente pouca energia por unidade. A fosforilação oxidativa, ou OXPHOS, ocorre nas mitocôndrias e funciona mais como uma usina de alta eficiência, gerando muito mais energia, mas exigindo bom fornecimento de oxigênio e nutrientes. Durante décadas pensou‑se que o câncer dependia quase exclusivamente da glicólise, mesmo na presença de oxigênio — um padrão conhecido como efeito Warburg. Evidências recentes derrubam essa visão simples: muitos tumores têm mitocôndrias plenamente funcionais e podem usar OXPHOS e o ciclo do ácido tricarboxílico (TCA) ao lado da glicólise, conferindo-lhes um conjunto energético mais amplo e flexível do que se supunha.
Muitos tipos celulares, muitas escolhas de combustível
Um tumor não é uma massa uniforme. É um pequeno ecossistema contendo células cancerosas, células de suporte, vasos sanguíneos e células imunes, cada um com necessidades energéticas distintas. Algumas células cancerosas vivem próximas aos vasos sanguíneos e desfrutam de oxigênio e nutrientes abundantes; outras estão enterradas em regiões mal supridas. Como resultado, células dentro do mesmo tumor podem favorecer a glicólise, depender principalmente de OXPHOS ou usar ambos simultaneamente. Essa variedade metabólica — chamada heterogeneidade — surge de diferenças no fluxo sanguíneo, níveis de nutrientes, tipo celular e sinais do ambiente circundante. Além disso, tumores frequentemente exibem simbiose metabólica: células glicolíticas exportam lactato como um subproduto, que células vizinhas dependentes de OXPHOS importam e queimam como combustível valioso. Compartilhamento semelhante de lactato ocorre entre células cancerosas e células de suporte, como fibroblastos, células endoteliais e células com função imuno‑suppressora, ajudando coletivamente o tumor a prosperar e resistir à terapia.
Em constante mudança: como a energia tumoral oscila ao longo do tempo
O metabolismo tumoral não é apenas diversificado em um dado momento; é também altamente dinâmico. À medida que os tumores crescem, enfrentam condições mutáveis como hipóxia, acúmulo de ácido, falta de nutrientes e variações na rigidez do tecido. Em condições adversas e com pouco oxigênio, muitas células cancerosas migram para a glicólise. Sob acúmulo de ácido ou privação de açúcar, podem voltar a aumentar o uso de OXPHOS. A mesma flexibilidade aparece em marcos biológicos importantes. Células que se dividem rapidamente apoiam‑se na glicólise para gerar blocos de construção para novo DNA, lipídios e membranas. Células em repouso ou circulantes no sangue frequentemente dependem mais de OXPHOS. Durante a invasão e a metástase, as células cancerosas ajustam repetidamente sua escolha de combustível: alguns passos favorecem a glicólise, outros favorecem OXPHOS, e células metastáticas que colonizam novos órgãos ajustam seu metabolismo para combinar com o “solo” do tecido de destino.
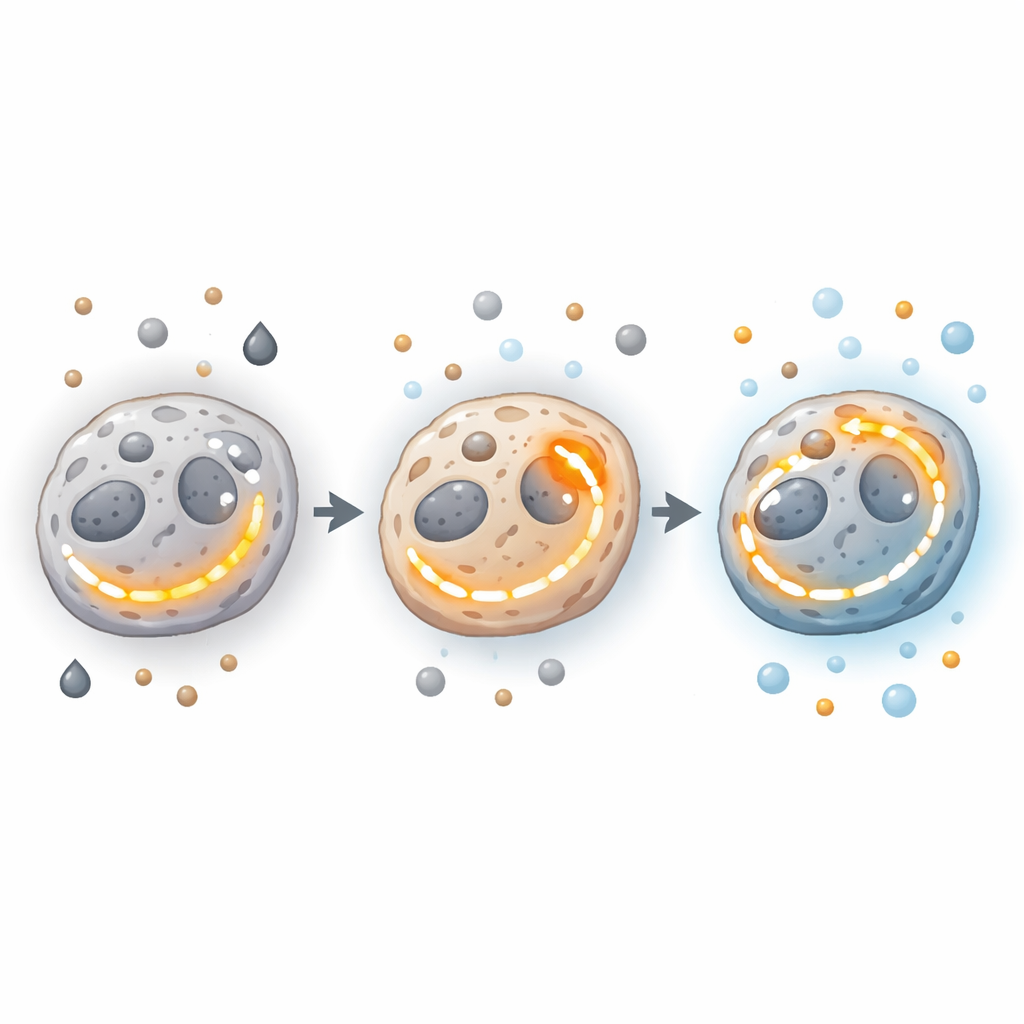
Genes, enzimas e “usinas” por trás da troca
No interior da maquinaria celular, genes e enzimas orientam essas decisões energéticas. Oncogenes e supressores tumorais podem empurrar células em direção à glicólise ou ao OXPHOS, ou permitir que aumentem ambos. Mutações ou alterações em enzimas-chave do TCA, como aquelas que manipulam citrato, succinato ou isocitrato, podem inclinar o equilíbrio, às vezes promovendo sinais pró‑tumorais como formação de vasos e invasão. Enzimas posicionadas em cruzamentos cruciais — como a piruvato quinase M2, que ajuda a decidir se o carbono derivado do açúcar vira energia ou material de construção — conectam a glicólise e a função mitocondrial. Ao mesmo tempo, diferenças no número, estrutura e desempenho mitocondrial entre regiões tumorais ampliam ainda mais o espectro de estados energéticos possíveis.
Repensando o tratamento por meio de um alvo energético em movimento
Como as células tumorais podem alternar entre glicólise e OXPHOS, bloquear apenas uma via muitas vezes não é suficiente; o câncer pode redirecionar seu uso de combustível e sobreviver. Os autores defendem que o metabolismo energético no câncer é brevemente estável e é fundamentalmente, e constantemente, mutável. Propõem ver os tumores por meio de um “espectro do metabolismo energético” que deve ser medido ao longo do tempo, não apenas uma vez. Na prática, isso poderia significar acompanhar as preferências de combustível de um tumor em diferentes estágios da doença e combinar inibidores de glicólise e OXPHOS em combinações sob medida. Estratégias de tratamento dinâmicas e guiadas pelo metabolismo assim poderiam cortar melhor o suprimento de energia do tumor, limitar sua capacidade de adaptação e melhorar o controle de longo prazo da doença.
Citação: Bao, X., Hou, B., Guo, Z. et al. Absolute dynamic and relative static: the relationship of glycolysis and OXPHOS in cancer development. Cell Death Discov. 12, 136 (2026). https://doi.org/10.1038/s41420-026-02992-5
Palavras-chave: metabolismo do câncer, glicólise, fosforilação oxidativa, microambiente tumoral, plasticidade metabólica