Clear Sky Science · pt
Exossomal S100A9 promove metástase pulmonar de carcinoma adenoide cístico ao ativar fibroblastos associados ao câncer
Como um câncer silencioso das salivares encontra o caminho para os pulmões
O carcinoma adenoide cístico é um câncer de crescimento lento, porém persistente, que frequentemente começa nas glândulas salivares e depois surge nos pulmões, às vezes anos após a remoção do tumor primário. Para pacientes e familiares, essa disseminação tardia é assustadora e difícil de prever ou prevenir. Este estudo esclarece como as células desses tumores preparam secretamente o tecido pulmonar distante para a invasão cancerígena, revelando uma conversa oculta entre as células tumorais e as células de suporte ao redor que pode finalmente oferecer novos pontos de intervenção terapêutica.
O câncer que persiste e retorna
O carcinoma adenoide cístico (CAC) é um câncer das glândulas da região da cabeça e pescoço, especialmente das glândulas salivares. Cirurgia e radioterapia frequentemente controlam o tumor primário, mas muitos pacientes acabam desenvolvendo metástases pulmonares, que são a principal causa de morte. Os medicamentos atuais para CAC disseminado são limitados, em parte porque os cientistas ainda não compreendem totalmente como as células do tumor original conseguem se estabelecer e crescer nos pulmões. Os autores deste artigo se propuseram a identificar os sinais-chave que permitem às células do CAC remodelar seu entorno e criar um “solo” favorável para futuros tumores pulmonares.
Pacotes minúsculos com grande impacto
Os pesquisadores focaram nos exossomos, pequenas bolhas membranosas que as células cancerosas liberam na corrente sanguínea. Essas vesículas carregam proteínas e material genético que podem reprogramar outras células à distância. Ao comparar uma linha celular padrão de CAC com uma versão selecionada por sua forte capacidade de se espalhar para os pulmões, a equipe descobriu que tanto as células agressivas quanto seus exossomos eram enriquecidos em uma proteína chamada S100A9, associada à inflamação. Pacientes cujos tumores e exossomos sanguíneos continham mais S100A9 tinham maior probabilidade de apresentar metástases pulmonares e períodos mais curtos sem recidiva, sugerindo que essa proteína contribui para a disseminação do câncer.
Reconfigurando a equipe de suporte do tumor
Usando sequenciamento de RNA de célula única, os autores construíram um mapa detalhado de todos os tipos celulares dentro dos tumores de CAC e das glândulas normais adjacentes. Eles descobriram uma comunicação intensa entre as células epiteliais do tumor e os fibroblastos vizinhos, as células estruturais responsáveis pela produção de tecido conjuntivo. No câncer, esses fibroblastos podem ser “recrutados” e transformados em fibroblastos associados ao câncer (CAF), que endurecem o tecido, alimentam a inflamação e ajudam as células tumorais a se mover. O estudo mostrou que exossomos ricos em S100A9, vindos de células de CAC agressivas, podiam converter fibroblastos normais em CAFs ativados: eles ficaram mais contráteis, mais móveis e passaram a produzir enzimas e moléculas inflamatórias que remodelam o tecido e promovem o crescimento tumoral.
De sinais locais a colônias pulmonares
A equipe então perguntou se esses fibroblastos ativados por exossomos realmente facilitavam a colonização pulmonar pelo CAC. Em modelos murinos, a injeção de exossomos carregados com S100A9 na corrente sanguínea preparou os pulmões: os fibroblastos locais passaram a expressar marcadores de ativação e o tecido pulmonar começou a expressar fatores associados à formação de novos vasos e à degradação da matriz. Quando células de CAC foram introduzidas posteriormente, camundongos pré-tratados com exossomos de S100A9 desenvolveram mais e maiores metástases pulmonares. Análises adicionais mostraram que esse processo dependia de uma cadeia de sinais inflamatórios centrada na molécula mensageira IL-17, juntamente com TNF e NF-κB, que em conjunto amplificaram a ativação dos fibroblastos e remodelaram o microambiente pulmonar.
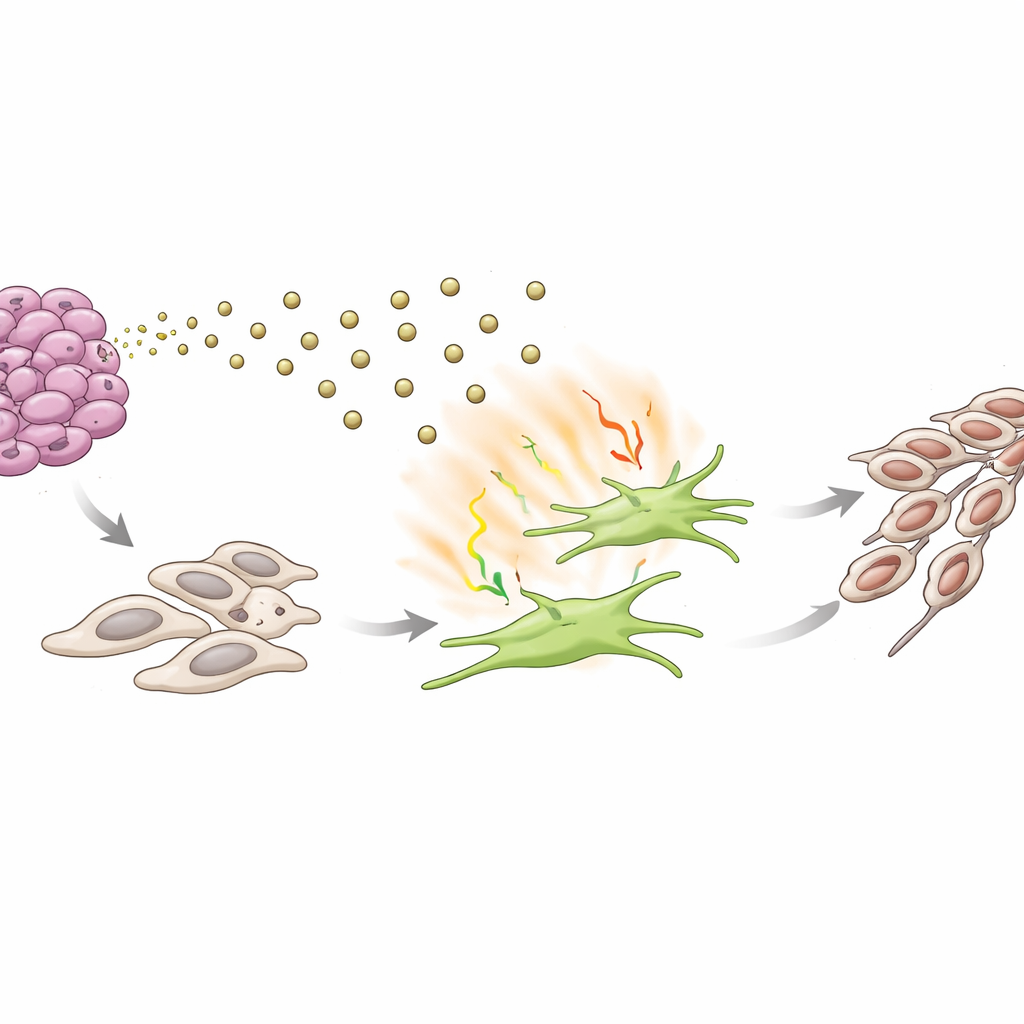
Um círculo vicioso que impulsiona a transformação do câncer
Em sistemas de co-cultura em laboratório, fibroblastos que haviam sido “educados” por exossomos ricos em S100A9, ou por essa via de sinalização dirigida por IL-17, tornaram as células de CAC vizinhas mais agressivas. As células tumorais mostraram maior capacidade de migração, invasão através de barreiras, crescimento em colônias e adoção de uma forma mais móvel e alongada, associada à transição epitélio–mesênquima, um passo-chave rumo à metástase. Bloquear IL-17 com um anticorpo neutralizante reverteu muitas dessas mudanças, enquanto adicionar IL-17 purificada isoladamente empurrou as células de CAC para esse estado mais invasivo. Em conjunto, esses achados descrevem um ciclo autorreforçador: as células tumorais enviam S100A9 em exossomos para ativar fibroblastos; fibroblastos ativados liberam IL-17 e outros sinais que, por sua vez, tornam as células tumorais mais propensas a se disseminar.
Quebrando o circuito de comunicação oculto
Para um leigo, a mensagem é que o CAC não se espalha para os pulmões por acaso. Em vez disso, o tumor original treina secretamente células de suporte e tecidos distantes para ajudá-lo a crescer em outro lugar, usando pequenos pacotes cheios de proteína como mensageiros. Este trabalho identifica S100A9 e a via de sinalização IL-17 a jusante como pontos centrais nesse processo. Ao direcionar esse eixo de comunicação — seja bloqueando S100A9, atenuando a sinalização de IL-17 ou interrompendo a ativação dos fibroblastos — terapias futuras podem ser capazes de interromper a “fase de preparação” da metástase pulmonar, oferecendo aos clínicos novas formas de evitar que esse câncer discreto, porém perigoso, volte longe de seu ponto de origem.
Citação: Chen, Cw., Zhang, Sr., Yan, Ym. et al. Exosomal S100A9 promotes lung metastasis of adenoid cystic carcinoma via activating cancer-associated fibroblasts. Cell Death Discov. 12, 120 (2026). https://doi.org/10.1038/s41420-026-02991-6
Palavras-chave: carcinoma adenoide cístico, exossomos, fibroblastos associados ao câncer, metástase pulmonar, eixo S100A9 IL-17