Clear Sky Science · pt
Navegando nas complexidades da ferroptose no adenocarcinoma ductal pancreático: papéis, mecanismos e aplicações potenciais
Por que este câncer mortal e uma nova forma de morte celular importam
O adenocarcinoma ductal pancreático (PDAC) está entre os cânceres mais letais; a maioria dos pacientes é diagnosticada tardiamente, os tratamentos raramente funcionam por muito tempo e a sobrevida é medida em meses, não anos. Este artigo de revisão explora uma descoberta relativamente recente — a ferroptose, um tipo de morte celular impulsionada por ferro e dano lipídico — e investiga se podemos transformá‑la numa arma contra o PDAC. Para o leitor, oferece uma janela sobre como os pesquisadores tentam superar um tumor resistente explorando suas próprias vulnerabilidades metabólicas.
Ferro, gorduras e o 'enferrujamento' das células cancerígenas
A ferroptose é diferente das formas mais conhecidas de morte celular, como a apoptose. Em vez de desmontar a célula de maneira ordenada, a ferroptose faz com que a célula “enferruje por dentro”. O ferro intracelular alimenta moléculas altamente reativas que atacam certos lipídios nas membranas celulares, fazendo‑as se degradarem. As células de PDAC, que exigem ferro e energia extras para sustentar seu rápido crescimento, são particularmente vulneráveis a esse tipo de dano. Para sobreviver, elas dependem de vários sistemas de defesa incorporados que eliminam esses subprodutos perigosos. A revisão descreve quatro circuitos protetores principais: um sistema glutatião–GPX4 que desintoxica lipídios danificados; um sistema FSP1–CoQ e vitamina K na membrana celular; um sistema DHODH–CoQ nas mitocôndrias; e uma via baseada em BH4 que preserva lipídios sensíveis. Juntos, esses mecanismos atuam como camadas de segurança projetadas para manter a ferroptose sob controle.
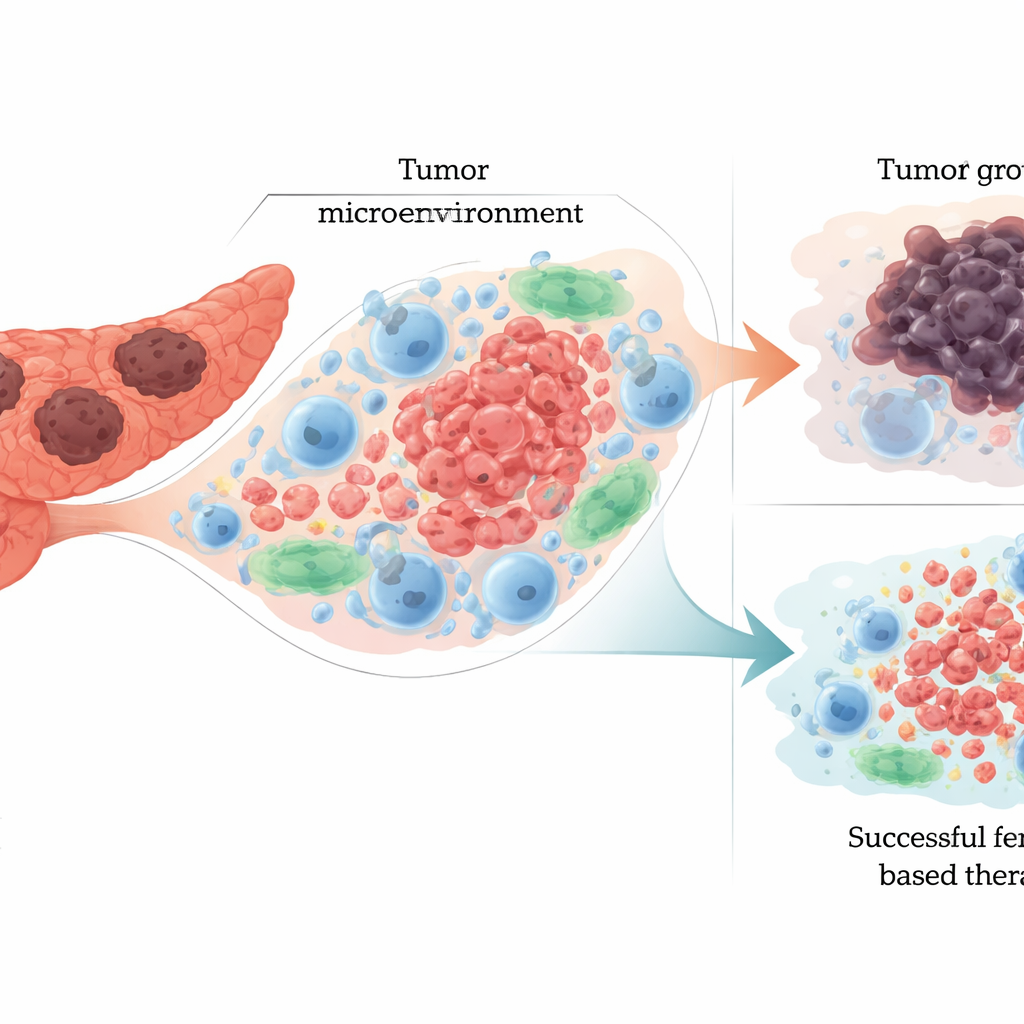
Como os tumores pancreáticos inclinham o equilíbrio
O PDAC reprograma o metabolismo básico — manejo do ferro, uso de lipídios e respostas ao estresse oxidativo — para favorecer o crescimento e resistir ao tratamento. As células tumorais frequentemente importam mais ferro, armazenam‑no de forma distinta e o liberam por processos como a degradação da ferritina, o que pode tanto alimentar o crescimento quanto predispor as células à ferroptose. Elas também alteram sua composição lipídica: aumentam certos ácidos graxos poli‑insaturados que são fáceis de oxidar, enquanto simultaneamente elevam enzimas e sistemas antioxidantes que reparam ou protegem as membranas. Genes-chave do câncer, como KRAS e p53, junto com vias como Keap1–Nrf2 e Hippo, ajudam a ajustar esse equilíbrio, às vezes tornando as células mais sensíveis à ferroptose e outras vezes reforçando suas defesas. O artigo explica que essas mesmas vias impulsionam a agressividade e a resistência a drogas do PDAC, sugerindo que empurrá‑las rumo à ferroptose pode prejudicar seletivamente as células tumorais.
Amiga e inimiga: a ferroptose no entorno tumoral
A ferroptose não ocorre isoladamente; desenrola‑se dentro de um microambiente tumoral lotado de células imunes, células do tecido conjuntivo e vasos sanguíneos. Quando as células cancerígenas passam por ferroptose, liberam ferro, lipídios oxidados e sinais de alerta que podem ter efeitos ambíguos. No lado benéfico, esses sinais podem ativar certas células imunes, levando‑as a atacar o tumor. No lado prejudicial, podem empurrar outras células imunes para um estado supressor e protetor do tumor ou matar diretamente defensores importantes, como células NK, células B e linfócitos T citotóxicos. A revisão enfatiza esse papel duplo: a ferroptose pode reduzir tumores ao matar células cancerígenas, mas também remodelar o ecossistema ao redor de forma a enfraquecer a imunidade e favorecer a progressão se não for controlada cuidadosamente.

Do insight biológico ao diagnóstico e à terapia
Como a ferroptose envolve ferro, lipídios e respostas ao estresse, ela deixa pegadas moleculares mensuráveis. Pesquisadores começaram a identificar genes, proteínas e moléculas de RNA relacionados à ferroptose no sangue e no tecido tumoral que se correlacionam com a presença, o estágio e os desfechos do PDAC. Ferritina elevada, hormônios reguladores de ferro alterados e assinaturas gênicas específicas podem ajudar a refinar diagnóstico e prognóstico. No lado do tratamento, múltiplas drogas experimentais e combinações visam empurrar as células de PDAC para a ferroptose — seja bloqueando suas defesas (como GPX4 ou o transportador de cistina sistema Xc−), seja sobrecarregando‑as com ferro e moléculas reativas. Algumas estratégias combinam indutores de ferroptose com quimioterapia padrão, como a gemcitabina, para superar resistência, enquanto outras encapsulam esses agentes em nanopartículas e vesículas biomiméticas para entregá‑los com mais precisão e reduzir danos colaterais.
Promessa, riscos e o caminho à frente
Os autores concluem que direcionar a ferroptose pode abrir uma nova frente contra o PDAC ao explorar exatamente os traços que tornam esse câncer tão difícil de tratar. Contudo, alertam que a ferroptose é uma espada de dois gumes. Os mesmos mecanismos que matam células tumorais podem lesar células-tronco saudáveis, fígado e rins, e células imunes cruciais, potencialmente causando efeitos colaterais graves e até piorando desfechos se aplicados de forma inadequada. O progresso futuro dependerá de mapear exatamente como a ferroptose interage com a genética, o metabolismo e o microambiente imune do PDAC; desenvolver sistemas de entrega que concentrem seus efeitos nos tumores; e validar biomarcadores e combinações de drogas baseadas em ferroptose em ensaios clínicos bem desenhados. Se esses desafios forem superados, a ferroptose pode se tornar um componente chave de terapias mais precisas, eficazes e personalizadas para o câncer pancreático.
Citação: Xiao, Y., Wang, W., Wang, G. et al. Navigating the complexities of ferroptosis in pancreatic ductal adenocarcinoma: roles, mechanisms and potential applications. Cell Death Discov. 12, 117 (2026). https://doi.org/10.1038/s41420-026-02987-2
Palavras-chave: câncer de pâncreas, ferroptose, microambiente tumoral, metabolismo do câncer, terapia por nanopartículas