Clear Sky Science · pt
Transição endotelial–mesenquimal mediada por APOA2 e reprogramação do metabolismo lipídico tumoral conferem resistência a drogas antiangiogênicas via TGF-β
Por que essa descoberta importa para os pacientes
Médicos usam cada vez mais drogas que sufocam tumores hepáticos ao cortar seu suprimento sanguíneo, mas muitos pacientes veem seus cânceres deixarem de responder após um benefício inicial. Este estudo aborda uma questão urgente: por que alguns cânceres de fígado se tornam resistentes a esses tratamentos que bloqueiam vasos sanguíneos, e como podemos contorná‑los? Os pesquisadores revelam uma parceria oculta entre uma proteína de transporte de gordura no sangue e um potente sinal de crescimento que permite aos tumores reconfigurar tanto seus vasos quanto seu uso de energia, apontando para uma estratégia alternativa para tratar um câncer de difícil cura.
Um tumor que aprende a viver sem seu suporte habitual
O carcinoma hepatocelular, a forma mais comum de câncer de fígado, depende fortemente de novos vasos sanguíneos para crescer. Drogas padrão para doença avançada foram concebidas para bloquear uma via-chave de crescimento vascular centrada no VEGF e seu receptor VEGFR2. Ainda assim, em muitos pacientes, os tumores continuam a prosperar apesar dessas medicações. Ao comparar amostras de tumores de pacientes que responderam ou não ao fármaco antiangiogênico apatinibe, os autores encontraram um gene em destaque: APOA2. Tumores de pacientes resistentes apresentaram níveis marcadamente mais altos de APOA2, uma proteína mais conhecida por seu papel no transporte de gorduras no sangue. Isso levantou a possibilidade de que a APOA2 possa ajudar os tumores a escapar de drogas que têm como alvo os vasos.
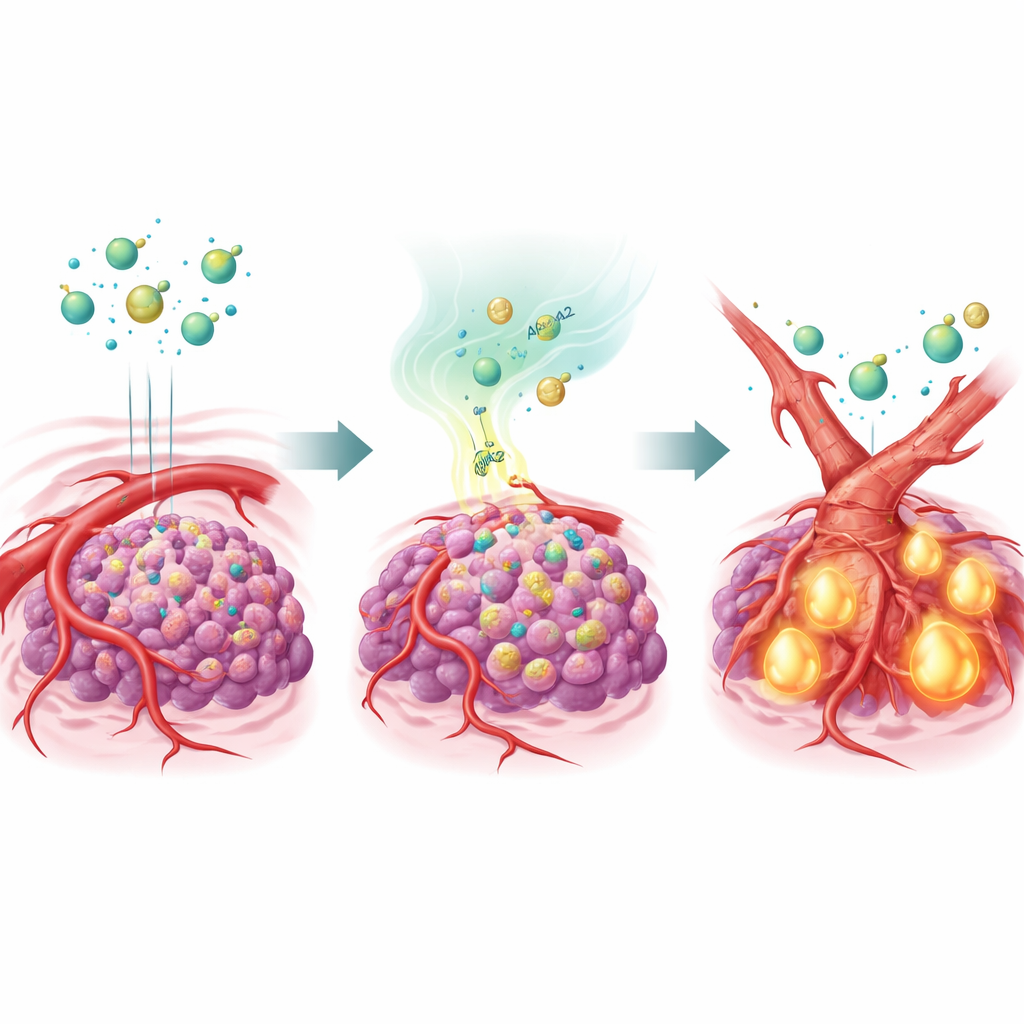
Uma proteína transportadora de gordura que remodela vasos
Para testar essa hipótese, a equipe modificou células de câncer de fígado para superproduzir APOA2 e as implantou em camundongos. Quando tratadas com vários fármacos antiangiogênicos, esses tumores ricos em APOA2 em grande parte ignoraram a terapia: seus vasos sanguíneos persistiram e os cânceres continuaram a crescer. Análises detalhadas mostraram que um sinal mestre chamado TGF-β estava fortemente ativado nesses tumores, e seus níveis estavam elevados tanto no microambiente tumoral quanto no sangue dos animais. O TGF-β atuou nas células que revestem os vasos sanguíneos, empurrando‑as a mudar de identidade num processo chamado transição endotelial‑para‑mesenquimal. Ao assumirem um estado mais parecido com tecido cicatricial, mesenquimal, essas células perderam grande parte de seu VEGFR2, o próprio alvo que as drogas antiangiogênicas foram projetadas para atingir. Em efeito, os vasos se remodelaram em uma forma que os fármacos já não conseguem reconhecer.
Um desvio metabólico que mantém as células cancerosas abastecidas
A história não terminou na parede do vaso. O mesmo sinal de TGF-β induzido pela APOA2 também reprogramou como as células tumorais obtêm energia. Em vez de dependerem principalmente da quebra de açúcar, células com altos níveis de APOA2 começaram a captar mais ácidos graxos livres do ambiente e a queimá‑los em suas mitocôndrias por oxidação de ácidos graxos. Experimentos que mediram o uso de nutrientes e o consumo de oxigênio mostraram que essas células ficaram mais dependentes de gordura como fonte de energia e produziram mais combustível celular (ATP). Essa mudança permitiu que as células tumorais continuassem a se dividir rapidamente e evitassem a morte celular, mesmo quando o suprimento sanguíneo estava sendo pressionado pelo tratamento antiangiogênico.
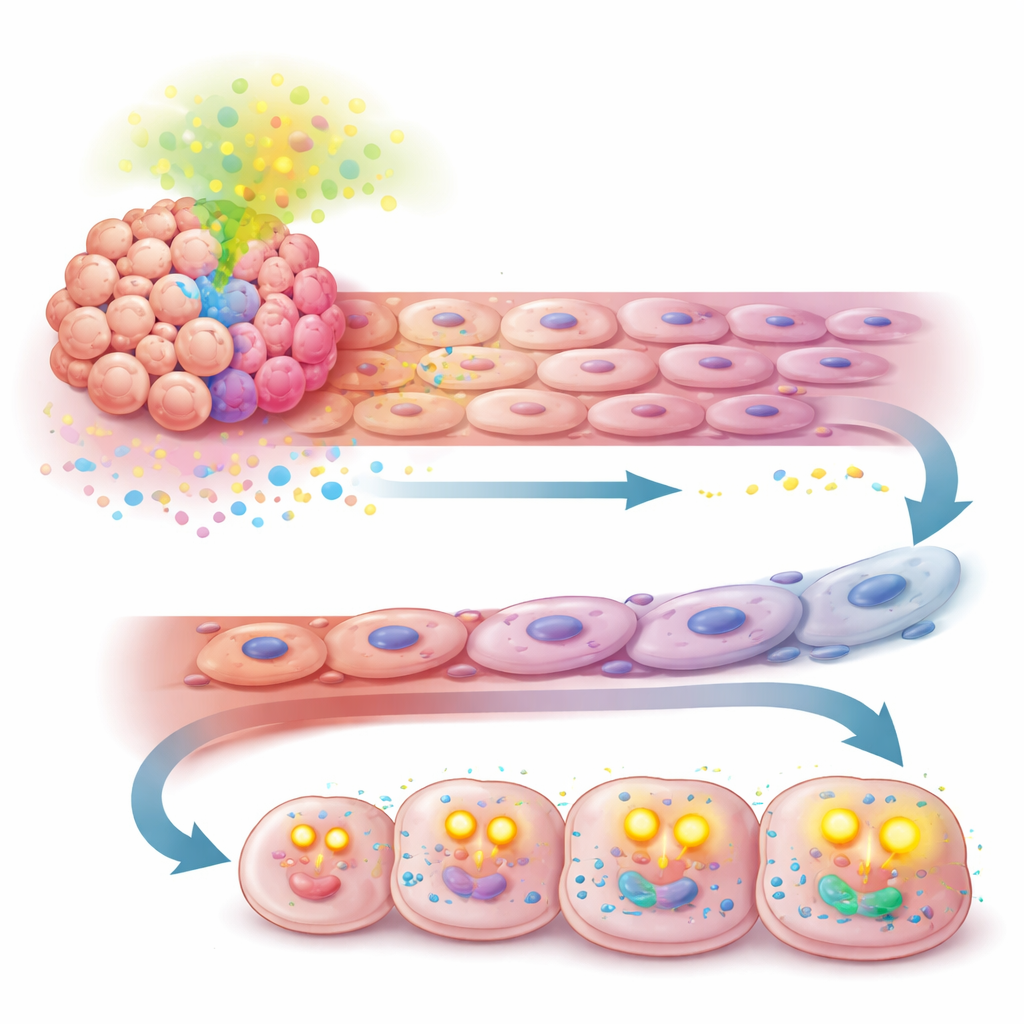
Virando uma vulnerabilidade em novo alvo terapêutico
De maneira crucial, quando os pesquisadores bloquearam o TGF-β, as vantagens conferidas pela APOA2 se desfizeram. Inibir esse sinal em modelos murinos reduziu as alterações vasculares anormais, restaurou a sensibilidade à terapia e retardou o crescimento tumoral. Ainda mais promissor, um anticorpo duplo que bloqueia simultaneamente TGF-β e o ponto de verificação imune PD-1 funcionou melhor do que cada abordagem isoladamente em tumores com altos níveis de APOA2. Esses resultados sugerem que, em um subconjunto de cânceres de fígado marcado por alta APOA2, a doença silenciosamente trocou sua dependência da via usual do VEGF por uma rota centrada no TGF-β que sustenta tanto os vasos quanto o metabolismo tumoral.
O que isso significa para o futuro do cuidado do câncer de fígado
Para leigos, a mensagem-chave é que alguns tumores hepáticos escapam às drogas atuais que atacam vasos sanguíneos ao reorganizar tanto sua tubulação quanto sua fonte de energia. Uma proteína associada a gorduras, a APOA2, amplifica o sinal de TGF-β, que por sua vez disfarça os vasos para que os medicamentos existentes não os reconheçam e ensina as células tumorais a viver de gorduras em vez de açúcar. O estudo sugere que testar tumores quanto à APOA2 poderia identificar pacientes que provavelmente não se beneficiariam dos antiangiogênicos padrão, mas que poderiam responder a fármacos que bloqueiam o TGF-β, especialmente quando combinados com imunoterapia moderna. Em resumo, ao expor como os tumores se adaptam, este trabalho aponta para uma estratégia mais personalizada que ataca tanto os vasos quanto a fonte de energia desses cânceres resilientes.
Citação: Zhang, S., Fu, Z., Zhu, F. et al. APOA2-mediated endothelial mesenchymal transition and cancer lipid metabolism reprogramming confers antiangiogenic drug resistance through TGF-β. Cell Death Discov. 12, 119 (2026). https://doi.org/10.1038/s41420-026-02984-5
Palavras-chave: carcinoma hepatocelular, resistência antiangiogênica, APOA2, sinalização TGF-beta, metabolismo lipídico do câncer