Clear Sky Science · pt
Multiômica revela heterogeneidade e populações funcionais de células progenitoras de oligodendrócitos induzidas por células-tronco neurais humanas
Por que proteger o isolamento do cérebro importa
O cabeamento do nosso cérebro depende de uma cobertura gordurosa chamada mielina, que envolve as fibras nervosas como o isolamento de cabos elétricos. Quando a mielina é danificada, como na esclerose múltipla e em outras doenças, os sinais desaceleram ou falham, causando problemas de movimento, visão e cognição. Este estudo explora um grupo especial de células humanas que podem reconstruir a mielina e faz uma pergunta prática: quais células são mais adequadas para futuras terapias celulares para reparar esse isolamento crucial?
De células-tronco iniciais a formadoras de mielina
Os pesquisadores começaram com células-tronco neurais humanas — células iniciais versáteis obtidas de tecido cerebral fetal que já estão comprometidas a se tornar células do sistema nervoso. Eles induziram essas células em laboratório a se diferenciarem em células progenitoras de oligodendrócitos, ou hOPCs, que são os precursores diretos das células formadoras de mielina. Ao microscópio, as células mudaram de formas simples e arredondadas para morfologias mais complexas com múltiplos ramos, e ativaram proteínas características que marcam passos ao longo do caminho rumo a células maduras produtoras de mielina. Isso forneceu uma fonte confiável e relativamente segura de precursores humanos construtores de mielina para análise detalhada.
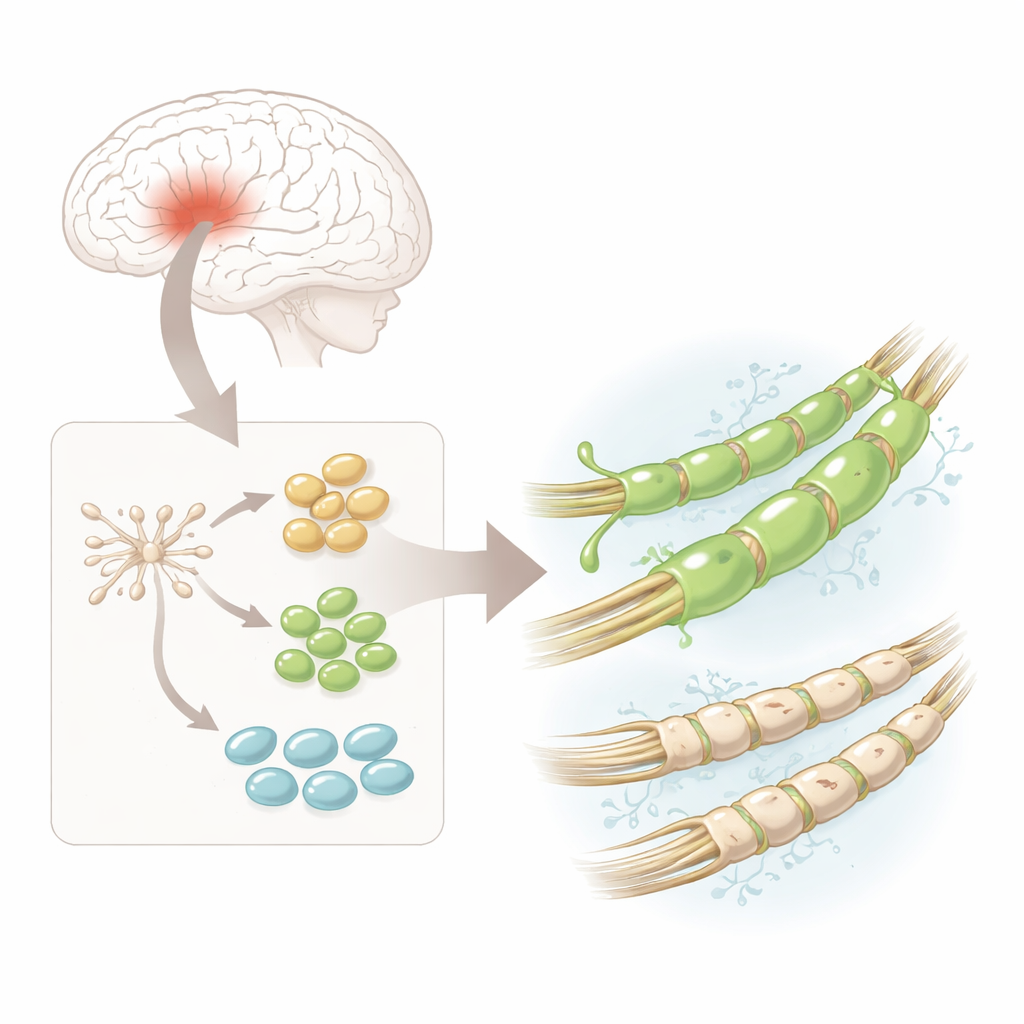
Um tipo celular, muitas variedades ocultas
Usando sequenciamento de RNA de célula única — uma abordagem que lê quais genes estão ativos em milhares de células individuais — a equipe descobriu que as hOPCs não eram todas iguais. Em vez disso, agruparam-se em três estágios principais: “pré-progenitores” iniciais, progenitores mais comprometidos e células se aproximando da identidade oligodendrocitária completa. Em todos esses estágios, um gene se destacou: PDGFRA, que codifica um receptor de superfície celular. Um método de imagem altamente sensível chamado RNA-Scope confirmou que a mensagem de PDGFRA e a proteína estavam mais abundantes que outros marcadores-chave em cada estágio, sugerindo que esse receptor poderia definir células particularmente capazes de construir mielina.
Separando as células de reparo mais poderosas
Para testar essa ideia, os cientistas separaram as hOPCs em dois grupos com base em a presença do receptor PDGFR-α em sua superfície. Em seguida, compararam células PDGFR-α–positivas, PDGFR-α–negativas e células não selecionadas em uma série de testes funcionais. Quando transplantadas em camundongos “shiverer” — que não conseguem formar mielina normal —, as células PDGFR-α–positivas produziram mielina mais densa e compacta em torno das fibras nervosas do que os outros grupos. Essas células também migraram mais longe e se multiplicaram mais rapidamente em ensaios de laboratório. Em outras palavras, a população PDGFR-α–positiva foi a mais vigorosa em deslocar-se para onde era necessária, expandir-se em número e reconstruir o isolamento.
Sinais internos que impulsionam crescimento e reparo
Aprofundando-se, a equipe comparou a atividade gênica entre células PDGFR-α–positivas e –negativas. Eles descobriram que as positivas ativaram redes de genes envolvidas no crescimento de células gliais e na formação de mielina, bem como várias rotas de sinalização intracelular chave. Duas vias, em particular, se destacaram: PI3K–AKT–mTOR, há muito associada ao crescimento celular e à produção de mielina, e a sinalização TGF-β, que influencia como células cerebrais jovens escolhem seus destinos. Os dados sugeriram que a ativação de PDGFR-α alimenta a via PI3K–AKT–mTOR, que por sua vez potencializa sinais relacionados ao TGF-β, juntos empurrando as células na direção de se tornarem formadoras eficazes de mielina.
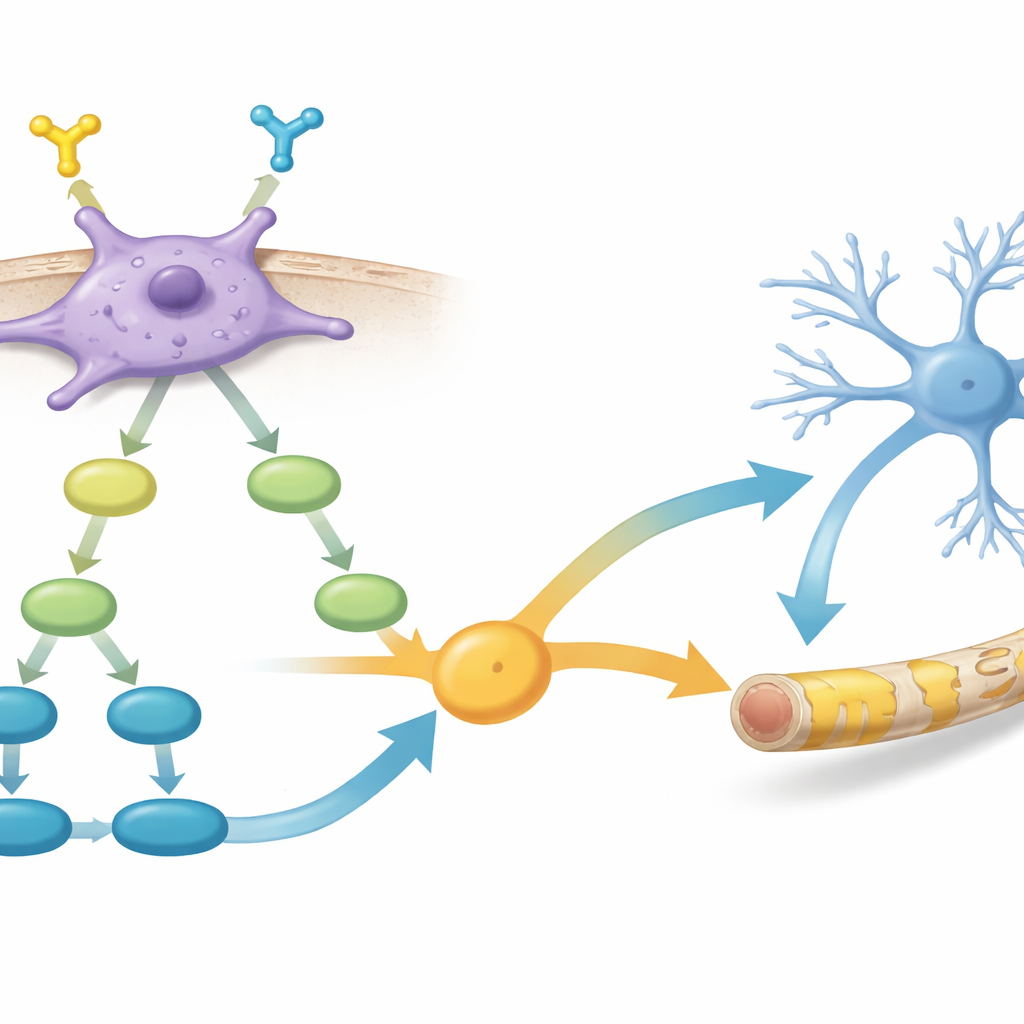
Potencializando o reparo da mielina com um ajudante químico
Os pesquisadores então investigaram se poderiam aprimorar ainda mais essas células promissoras. Eles trataram hOPCs PDGFR-α–positivas com uma pequena molécula que ativa a via TGF-β e examinaram tanto a atividade gênica quanto o comportamento celular. Após o tratamento, essas células apresentaram níveis mais altos de múltiplos genes relacionados à mielina e produziram bainhas de mielina mais espessas e completas quando transplantadas em camundongos shiverer, em comparação com células PDGFR-α–positivas não tratadas. Isso apoia a ideia de que ajustar cuidadosamente a sinalização interna em progenitores já bem selecionados pode melhorar ainda mais seu desempenho como ferramentas vivas de reparo da mielina.
O que isso significa para tratamentos futuros
Para não especialistas, a mensagem central é que nem todos os precursores formadores de mielina são iguais. Ao combinar poderosas ferramentas de leitura gênica e imagem, este estudo identifica um subgrupo de destaque — as hOPCs PDGFR-α–positivas — que migram melhor, se dividem mais e reconstróem a mielina de forma mais eficaz do que seus pares. Também destaca rotas de sinalização internas que podem ser quimicamente moduladas para tornar essas células ainda mais potentes. Em conjunto, essas informações traçam um roteiro para projetar terapias celulares mais seguras e eficientes para restaurar o isolamento do cérebro em doenças nas quais a mielina é perdida.
Citação: Ye, D., Zhou, H., Qu, S. et al. Multi-omics reveals heterogeneity and functional populations of oligodendrocyte progenitor cells induced by human neural stem cells. Cell Death Discov. 12, 112 (2026). https://doi.org/10.1038/s41420-026-02971-w
Palavras-chave: reparo da mielina, células progenitoras de oligodendrócitos, células-tronco neurais, terapia celular, sequenciamento de RNA de célula única