Clear Sky Science · pt
Crosstalk entre bioenergética mitocondrial e SASP determina a eficácia senolítica na senescência induzida por terapia
Por que eliminar células “zumbis” do câncer é tão complicado
Muitos medicamentos modernos contra o câncer não matam todas as células tumorais de imediato. Em vez disso, algumas células entram em um estado limbo chamado senescência: param de se dividir, mas permanecem vivas, algo como células “zumbis”. Essas células senescentes induzidas por terapia podem ser úteis inicialmente, mas se persistirem podem alimentar recidivas, resistência e efeitos colaterais. Por isso, os cientistas testam drogas senolíticas projetadas para matar seletivamente células senescentes. Este artigo faz uma pergunta aparentemente simples: por que algumas células cancerosas senescentes morrem quando expostas a senolíticos, enquanto outras teimosamente sobrevivem?
Usinas de energia que lembram seu passado
No cerne do estudo estão as mitocôndrias, as pequenas usinas dentro das células. Os autores investigaram se a forma como as mitocôndrias queimam combustíveis diferentes — como açúcares, gorduras e aminoácidos — afeta a sensibilidade das células cancerosas senescentes a senolíticos que têm como alvo uma proteína de sobrevivência chamada BCL‑xL. Usando um ensaio de alto rendimento (MitoPlate S‑1), eles “imprimiram digitalmente” funcionalmente a atividade mitocondrial em várias linhagens de câncer antes e depois de a senescência ser desencadeada por tratamentos distintos (drogas que danificam o DNA, bloqueadores da mitose, estresse oxidativo ou inibidores do ciclo celular). Eles descobriram que a senescência induzida por terapia não produz um único estado mitocondrial uniforme. Em vez disso, cada fármaco deixou uma “impressão bioenergética” distinta, alterando quão amplamente e intensamente as mitocôndrias podiam acessar várias fontes de energia. Crucialmente, essa flexibilidade se sobrepunha a uma linha de base pré-existente: a configuração mitocondrial original das células parentais definiu um limite superior — o “teto” — sobre quão forte qualquer resposta senolítica posterior poderia ser.
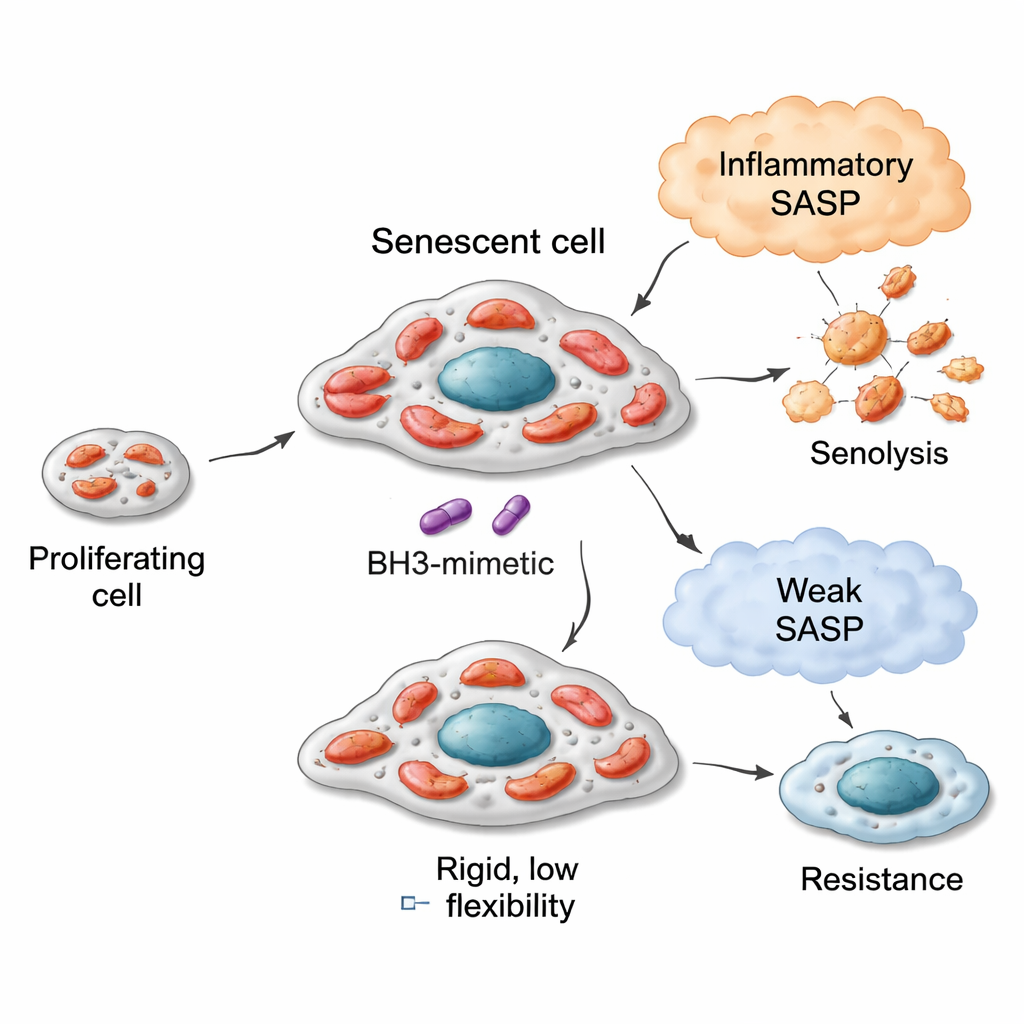
Motores flexíveis, combustíveis diferentes e sensibilidade senolítica
Em modelos de câncer de pulmão, mama e cólon, células senescentes com mitocôndrias mais flexíveis — capazes de oxidar uma gama maior de combustíveis — tendiam a ser mais vulneráveis a senolíticos que miram BCL‑xL, como navitoclax (ABT‑263) e A1331852. Por exemplo, células de câncer de pulmão levadas à senescência pelo fármaco bleomicina desenvolveram mitocôndrias que utilizavam vigorosamente muitos substratos, especialmente os ligados à quebra de ácidos graxos e a certas vias de aminoácidos. Essas células foram altamente sensíveis aos senolíticos. Em contraste, células empurradas à senescência por um inibidor de CDK4/6 (palbociclib) mostraram um repertório metabólico mais restrito e responderam mal aos mesmos agentes senolíticos. Ainda assim, essa relação tinha limites: células de câncer de mama também podiam tornar-se metabolicamente flexíveis após a senescência, mas, porque suas mitocôndrias iniciais eram menos “pré-configuradas” para apoptose, sua resposta senolítica máxima foi modesta. Células de câncer de cólon com maquinário apoptótico defeituoso permaneceram resistentes independentemente de como seu metabolismo mudou. Uma única medida — quão bem as células oxidavam o combustível succinato na linha de base — serviu como um indicador simples dessa capacidade mitocondrial herdada.
Quando o metabolismo conversa com a inflamação
Células senescentes são notórias pelo SASP, um coquetel de fatores secretados inflamatórios e de crescimento que podem influenciar os tecidos circundantes. A equipe investigou como o metabolismo mitocondrial se conecta a esse comportamento secretório usando células modificadas com um repórter para miR‑146a, um microRNA ativado pelo regulador inflamatório mestre NF‑κB. Eles descobriram que, embora os perfis gerais de SASP fossem em grande parte ditados pelo tipo celular, apenas certos estados senescentes ativaram esse eixo NF‑κB/miR‑146a. Esses eram os mesmos estados que respondiam bem aos senolíticos dirigidos a BCL‑xL. Importante, essas células senescentes “positivas para SASP inflamatório” também mostraram maior uso de oxidação de ácidos graxos e um aumento transcricional em genes que transportam gorduras de cadeia longa para as mitocôndrias. Bloquear a entrada de ácidos graxos com o fármaco etomoxir reduziu a ativação do miR‑146a sem reverter totalmente a senescência, sugerindo que a escolha do combustível mitocondrial ajuda a autorizar um SASP inflamatório permissivo para senolíticos.
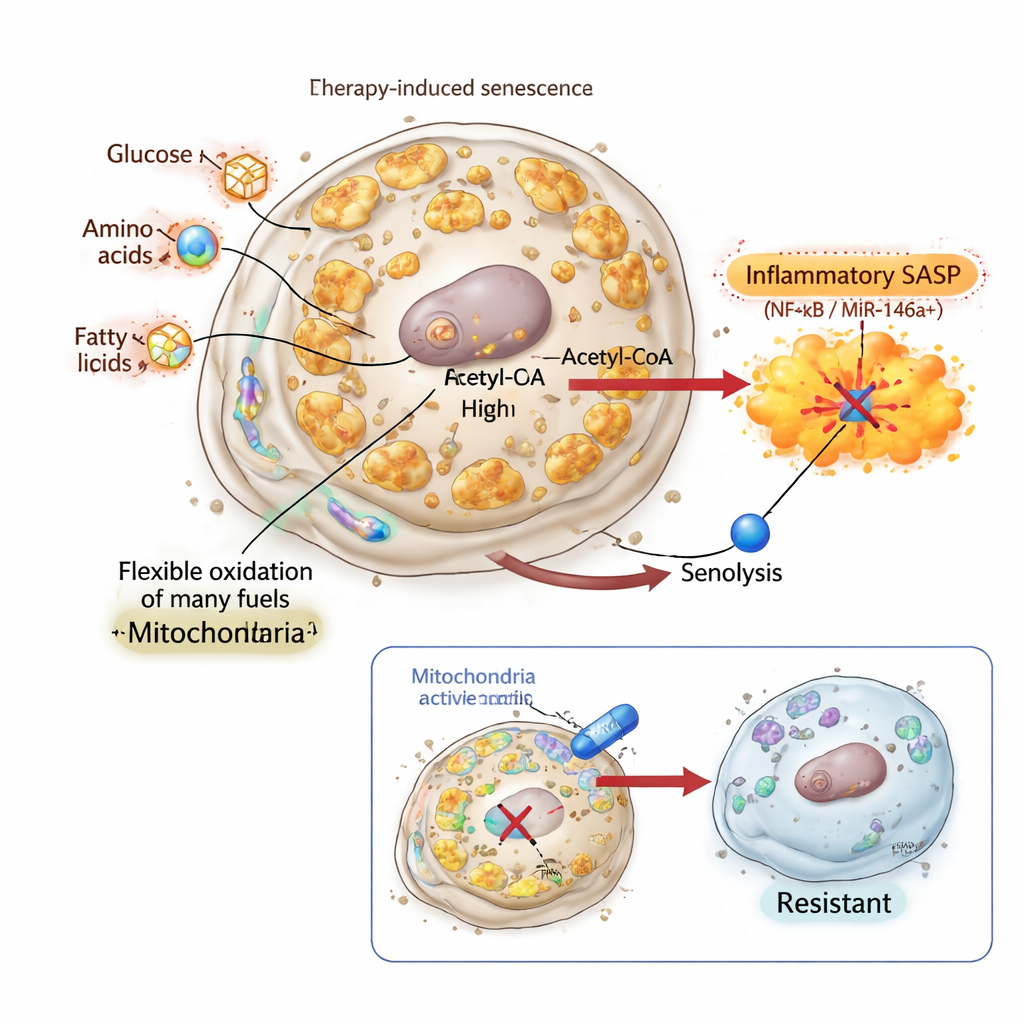
Silenciando o sinal e criando células senescentes inviáveis
Para testar se o SASP inflamatório é realmente necessário para a morte por senolíticos, os pesquisadores recorreram ao inflacromeno, um composto que se liga às proteínas de cromatina HMGB1 e HMGB2 e bloqueia seu papel na ativação de genes do SASP. Em células de câncer de pulmão e mama, o inflacromeno induziu um fenótipo senescente clássico: as células tornaram-se grandes, pararam de se dividir e acumularam marcadores de senescência. Sua massa mitocondrial e atividade bioenergética aumentaram substancialmente, e o uso de combustíveis foi claramente reprogramado. Ainda assim, seu SASP foi atenuado e o repórter miR‑146a permaneceu amplamente silencioso. Surpreendentemente, essas células senescentes sem SASP foram completamente resistentes aos senolíticos que miram BCL‑xL, apesar de terem mitocôndrias bioenergeticamente ativas e reprogramadas e expressão reduzida do gene antiapoptótico clássico BCL2. Isso mostrou que mudanças mitocondriais por si só não são suficientes; sem uma saída inflamatória conduzida pelas mitocôndrias, o “segundo golpe” senolítico falha.
O que isto significa para tratamentos futuros do câncer
Para o leitor leigo, a conclusão do estudo é que eliminar células cancerosas “zumbis” induzidas por terapia é regido por um circuito em camadas. Primeiro, a saúde e a arquitetura originais das mitocôndrias de uma célula tumoral determinam o quão longe os senolíticos podem chegar. Segundo, o tratamento específico que causa a senescência pode empurrar o metabolismo mitocondrial para uma maior ou menor flexibilidade, aproximando as células ou afastando-as do limiar da apoptose. Terceiro — e mais decisivo — os senolíticos só funcionam bem se a reprogramação metabólica conseguir engajar com sucesso um programa de SASP inflamatório que se comunique com o núcleo. Sem essa comunicação inflamatória, as células senescentes podem tornar‑se um estado final resistente a drogas. Na prática, isso sugere que terapias futuras podem ser otimizadas testando funcionalmente tanto a flexibilidade mitocondrial quanto a inflamação do SASP em tumores, e então escolhendo combinações de drogas que induzem senescência e senolíticos que garantam que as células “zumbis” não fiquem apenas congeladas no lugar, mas preparadas para remoção.
Citação: Llop-Hernández, À., Verdura, S., López, J. et al. Mitochondrial bioenergetics-SASP crosstalk determines senolytic efficacy in therapy-induced senescence. Cell Death Discov. 12, 103 (2026). https://doi.org/10.1038/s41420-026-02967-6
Palavras-chave: senescência celular, mitocôndrias, senolíticos, metabolismo do câncer, SASP inflamatório