Clear Sky Science · pt
A redução de SREBP1 desencadeia ferroptose ao suprimir o eixo Nrf2-XCT/GPX4 em câncer de ovário
Virando a fábrica de gordura do câncer contra si
O câncer de ovário costuma ser detectado tardiamente e pode ser muito difícil de tratar. Este estudo explora uma vulnerabilidade inesperada desses tumores: a dependência de produzir gorduras e óleos. Os pesquisadores mostram que desligar um interruptor chave da "fábrica de gordura" nas células cancerígenas pode tanto frear seu crescimento quanto ativar um tipo especial de morte celular, ao mesmo tempo em que facilita a ação do sistema imunológico contra o tumor.
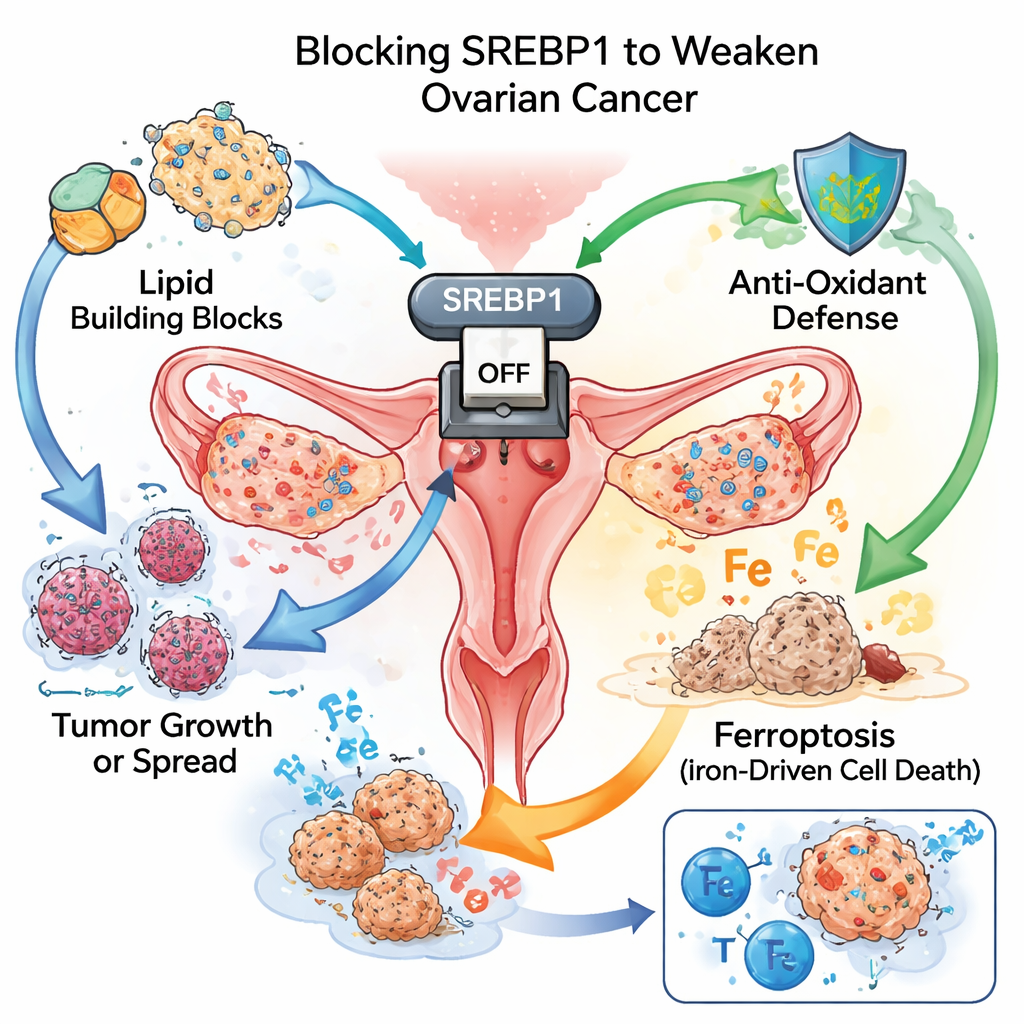
Um interruptor mestre para o combustível tumoral
Como ervas daninhas de crescimento rápido, células cancerígenas precisam de enormes quantidades de blocos de construção e energia. Uma maneira de suprir essa demanda é reprogramando como produzem e usam lipídios. A equipe concentrou-se na SREBP1, uma proteína que atua como um interruptor mestre da produção de gorduras. Em amostras de tecido de mais de cem pacientes, tumores ovarianos apresentaram níveis de SREBP1 bem mais altos do que o tecido normal adjacente. Mulheres cujos tumores mostraram coloração mais intensa para SREBP1 tenderam a ter doença mais agressiva e sobrevida mais curta, marcando essa proteína tanto como um impulsionador da progressão quanto como um sinal de pior prognóstico.
Reduzindo crescimento e disseminação ao cortar o suprimento de gordura
Em linhagens celulares de câncer de ovário cultivadas em laboratório, diminuir a SREBP1 reduziu fortemente a capacidade das células de se multiplicarem e formarem colônias. As células ficaram presas em fases específicas do ciclo celular, o que impediu sua divisão eficiente. Os pesquisadores também observaram menos sinais de migração e invasão: testes de “scratch” e Transwell mostraram que células com menos SREBP1 migravam menos, e marcadores-chave de um processo de mudança de forma chamado EMT regressaram a um estado mais “normal”. Ao mesmo tempo, medidas de triglicerídeos e colesterol caíram, e colorações revelaram menos gotículas lipídicas dentro das células, confirmando que sua maquinaria interna de produção de gordura havia sido reduzida.
Desencadeando uma morte celular alimentada por ferro
O efeito mais marcante do bloqueio de SREBP1 foi a ativação da ferroptose, uma forma de morte celular recentemente reconhecida, impulsionada por ferro e pela oxidação (peroxidação) das membranas celulares. Apenas um bloqueador de ferroptose, e não inibidores de outras vias de morte, conseguiu resgatar células com SREBP1 silenciado, apontando a ferroptose como a principal causa de seu declínio. Testes químicos mostraram mais produtos de dano provenientes de lipídios oxidativos, menos glutationa antioxidante e níveis mais altos de moléculas lipídicas reativas. Duas proteínas que normalmente protegem as células da ferroptose, chamadas xCT e GPX4, foram fortemente reduzidas quando SREBP1 foi suprimida, removendo um amortecedor protetor crucial contra esse processo destrutivo.
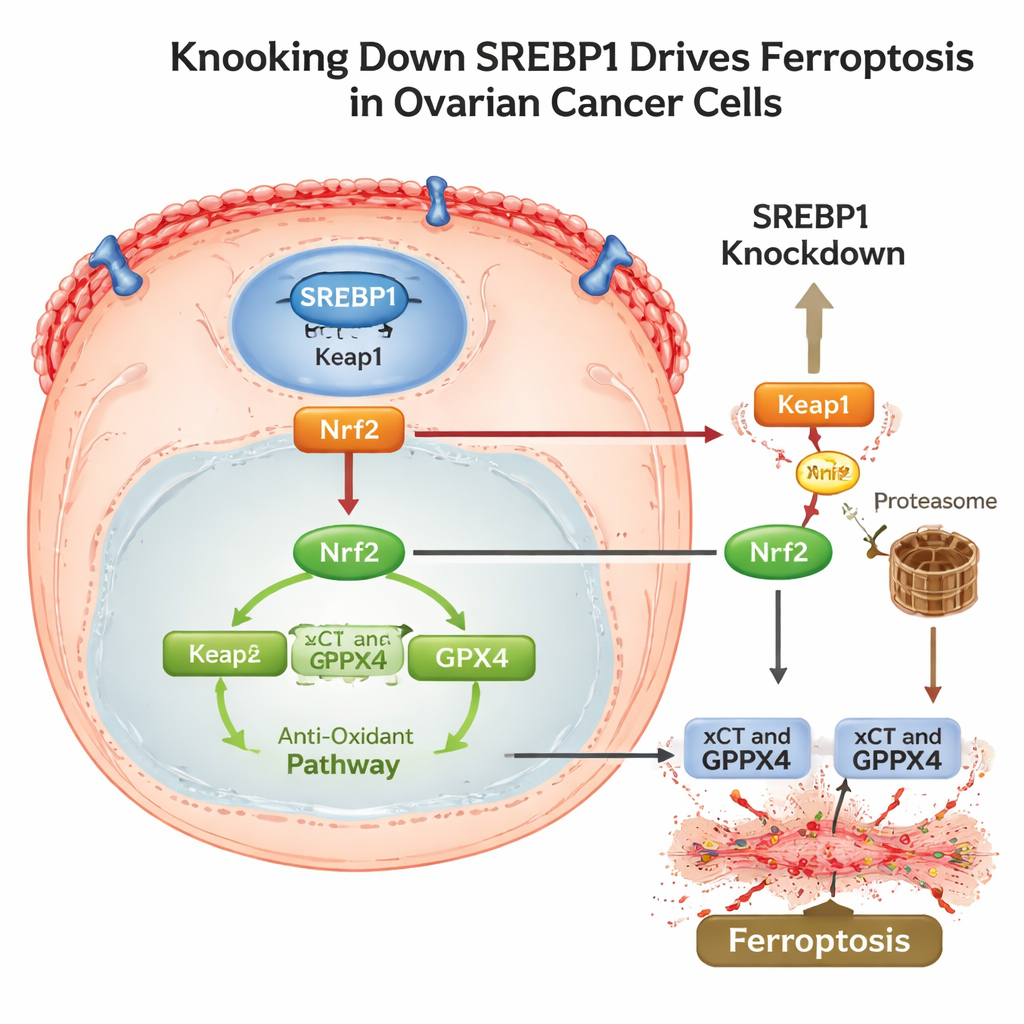
Desarmando o escudo antioxidante celular e artifícios de evasão
Para entender como SREBP1 se conecta a esse programa de morte, os cientistas traçaram uma via envolvendo outra importante proteína de resposta ao estresse, Nrf2. Em condições normais, Nrf2 ajuda as células a sobreviver ligando genes antioxidantes, incluindo xCT e GPX4. O estudo encontrou que reduzir SREBP1 aumentou os níveis de Keap1, uma proteína que marca Nrf2 para degradação, levando a mais quebra de Nrf2 e menos entrada deste no núcleo. À medida que o Nrf2 diminuía, suas defesas a jusante enfraqueciam e a ferroptose ocorria. Importante, tumores ricos em SREBP1 também mostraram níveis mais altos de PD-L1, uma proteína de superfície que ajuda as células cancerígenas a se esconderem de linfócitos T atacantes. Quando a SREBP1 foi silenciada em tumores de camundongos, os cânceres cresceram mais lentamente, exibiram mais sinais de dano lipídico, menos Nrf2 e GPX4, e menor PD-L1, junto com aumento da atividade imune.
Por que isso importa para tratamentos futuros
Em termos simples, tumores ovarianos parecem usar a SREBP1 como uma ferramenta de dupla lâmina para sobreviver: ela alimenta o crescimento ao impulsionar a produção de lipídios e, ao mesmo tempo, os equipa com um escudo antioxidante e uma camuflagem imune. Este trabalho mostra que desligar a SREBP1 pode privar o tumor de lipídios, retirar sua proteção contra danos induzidos por ferro e reduzir sua capacidade de escapar da resposta imune. Isso torna SREBP1 um alvo atraente para novos medicamentos e sugere que combinar bloqueadores de SREBP1 com tratamentos que induzem ferroptose ou liberam o sistema imune pode oferecer aos pacientes um controle mais eficaz e duradouro da doença.
Citação: Nie, R., Zhou, H., Chen, L. et al. SREBP1 knockdown triggers ferroptosis by suppressing the Nrf2-XCT/GPX4 axis in ovarian cancer. Cell Death Discov. 12, 101 (2026). https://doi.org/10.1038/s41420-026-02964-9
Palavras-chave: câncer de ovário, metabolismo lipídico, ferroptose, SREBP1, imunidade tumoral