Clear Sky Science · pt
PDHA1 aumenta a resistência ao ferroptose em câncer de próstata resistente à anóikis ao aumentar AIFM2
Por que algumas células de câncer de próstata se recusam a morrer
Quando células cancerígenas se desprendem de um tumor e entram na corrente sanguínea, a maioria deveria morrer antes de alcançar um novo órgão. Ainda assim, uma minoria perigosa sobrevive, viaja e origina metástases que frequentemente são letais. Este estudo faz uma pergunta central: o que permite que certas células de câncer de próstata resistam a uma forma de morte celular que normalmente ocorre quando perdem o contato com seu tecido de origem? Ao descobrir um circuito de sobrevivência oculto dentro dessas células, a pesquisa aponta para novas maneiras de bloquear a metástase em sua origem.
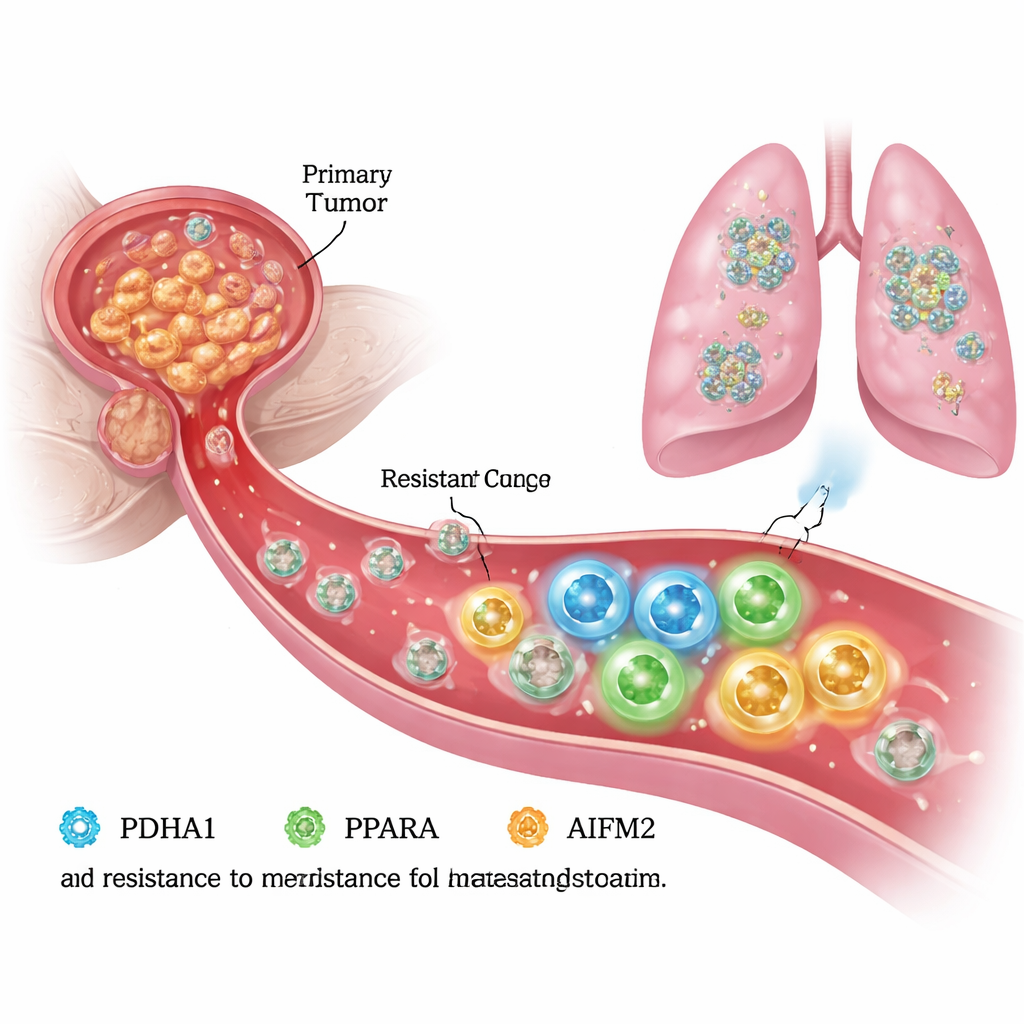
Escapando da morte na corrente sanguínea
Para se espalhar, as células do câncer de próstata devem suportar a vida sem o suporte do tecido circundante, conhecido como matriz extracelular. Nessas condições “desprendidas”, células saudáveis passam por uma morte programada chamada anóikis, e muitas células cancerígenas também são vulneráveis a um processo relacionado, dependente de ferro, chamado ferroptose. Os autores criaram em laboratório células de câncer de próstata resistentes à anóikis e as compararam com suas células “parentais” originais. Eles descobriram que as células resistentes não apenas migravam e invadiam com mais agressividade, mas também sobreviviam melhor em situação de desprendimento, sugerindo que haviam reconfigurado sua maquinaria interna para evitar a ferroptose e continuar crescendo.
Uma mudança metabólica com uma segunda função
Investigando mais a fundo, a equipe concentrou-se em uma enzima metabólica chamada PDHA1, mais conhecida por ajudar as células a transformar o piruvato derivado do açúcar em acetil-CoA nas mitocôndrias, alimentando a produção de energia. Nas células resistentes à anóikis, os níveis e a atividade de PDHA1 estavam marcadamente mais altos, e amostras de pacientes mostraram mais PDHA1 em tumores primários de homens cujo câncer de próstata havia se espalhado para linfonodos ou locais distantes. Quando os pesquisadores reduziram PDHA1, as células resistentes perderam grande parte de sua capacidade de se mover, invadir e sobreviver. Surpreendentemente, uma porção substancial de PDHA1 nessas células não estava mais confinada às mitocôndrias; ela havia se deslocado para o núcleo, onde o DNA é compactado com histonas que podem ser modificadas quimicamente para ligar ou desligar genes.
Reescrevendo a atividade gênica para bloquear a ferroptose
No interior do núcleo, PDHA1 pareceu alimentar a produção local de acetil-CoA, um elemento-chave para a acetilação de histonas. Os autores mostraram que o PDHA1 nuclear aumentava uma marca específica, a acetilação de H3K9, na região de controle de um gene chamado PPARA. Essa alteração atuou como um afrouxamento dos “carretéis” de cromatina, tornando mais fácil ativar o PPARA. O PPARA, por sua vez, funcionou como um interruptor mestre que aumentou a produção de outra proteína, AIFM2, ligando-se ao seu promotor e elevando sua transcrição. Em vez de ajustar diretamente o gene AIFM2, o PDHA1 trabalhou através do PPARA, estabelecendo uma via em vários passos desde o metabolismo alterado até a regulação gênica alterada.
Construindo um escudo contra danos mediados por ferro
AIFM2 é conhecida como um freio interno à ferroptose: ela ajuda a proteger os lipídios nas membranas celulares da oxidação destrutiva. Nas células de câncer de próstata resistentes, a regulação positiva de PDHA1 elevou os níveis de AIFM2, enquanto a diminuição de PDHA1 os reduziu. Testes funcionais mostraram que reduzir PDHA1 intensificou os sinais de ferroptose — mais espécies reativas de oxigênio, mais dano lipídico, menor potencial de membrana mitocondrial e encolhimento mitocondrial característico — especialmente quando as células foram expostas ao fármaco indutor de ferroptose erastina. A superexpressão de AIFM2 reverteu esses efeitos, resgatando a sobrevivência celular em culturas e restaurando a metástase pulmonar em camundongos, mesmo quando PDHA1 estava suprimido. Isso confirmou que AIFM2 é um efetor crítico a jusante da resistência à ferroptose promovida por PDHA1.
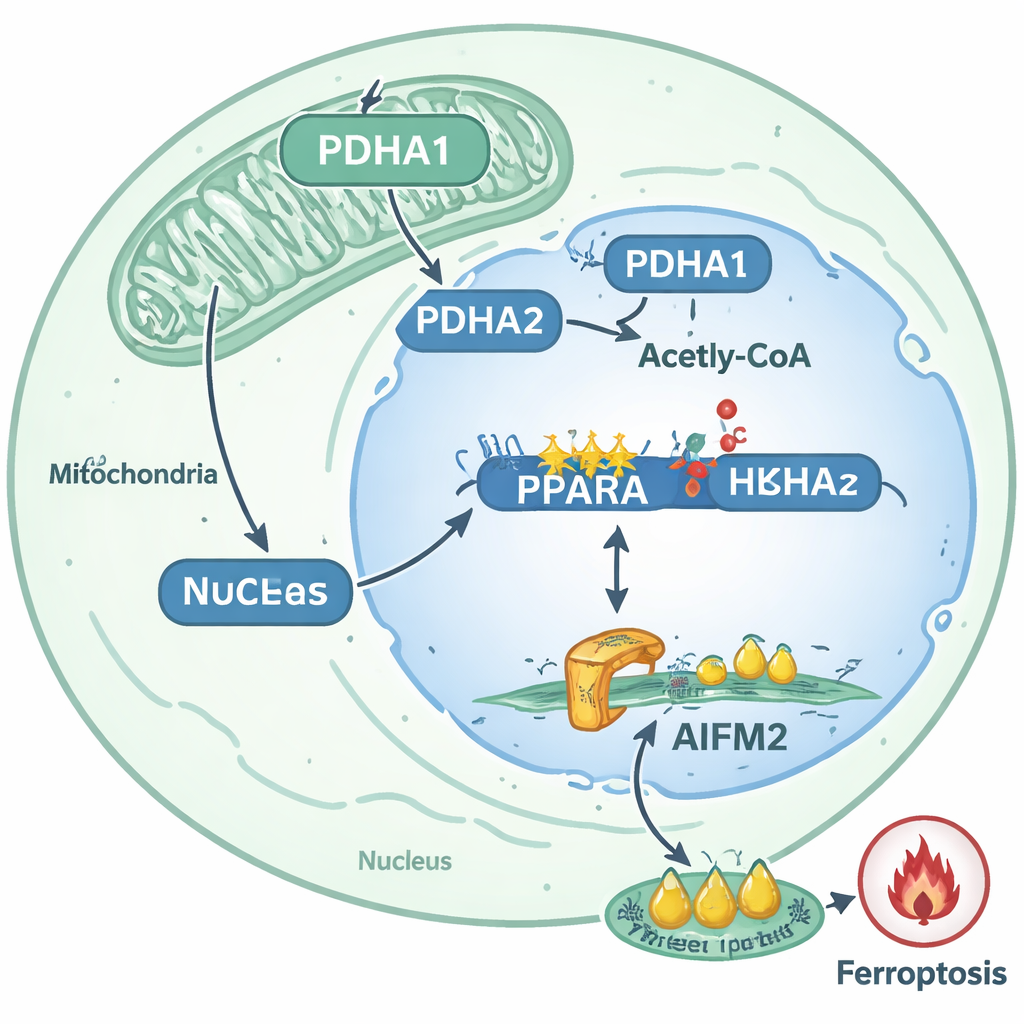
Do circuito molecular a ideias de tratamento
Ao mapear esses eventos, o estudo descreve uma rota clara pela qual células de câncer de próstata desprendidas se tornam mais difíceis de matar: PDHA1 migra para o núcleo, aumenta a acetilação de histonas no gene PPARA, eleva a atividade de PPARA e, assim, aumenta os níveis de AIFM2 para bloquear a ferroptose. Essa via está fortemente associada ao comportamento metastático em tumores de pacientes e em modelos animais. Para leigos, a conclusão é que certas células cancerígenas reaproveitam uma enzima metabólica comum como uma ferramenta epigenética que reconfigura a atividade gênica e constrói um escudo bioquímico contra uma forma potente de morte celular. Os autores sugerem que drogas direcionadas a PDHA1, PPARA ou AIFM2 — ou terapias que desencadeiem deliberadamente a ferroptose — poderiam um dia ser combinadas para despojar as células metastáticas de câncer de próstata dessa vantagem de sobrevivência e torná‑las muito mais vulneráveis durante sua jornada mais arriscada: o salto de um órgão para outro.
Citação: Cong, Y., Chen, K., Ju, Y. et al. PDHA1 enhances resistance to ferroptosis in anoikis-resistant prostate cancer by upregulating AIFM2. Cell Death Discov. 12, 105 (2026). https://doi.org/10.1038/s41420-026-02958-7
Palavras-chave: metástase do câncer de próstata, ferroptose, resistência à anóikis, PDHA1, AIFM2