Clear Sky Science · pt
Modulando assinaturas metabólicas para mitigar resistência ao cabozantinibe em modelos celulares de leucemia mieloide aguda FLT3-ITD
Por que isso importa para o tratamento do câncer
Muitos medicamentos modernos contra o câncer são projetados para mirar uma única proteína defeituosa nas células tumorais. Esses medicamentos direcionados podem provocar remissões dramáticas, mas os cânceres frequentemente encontram formas de se adaptar e voltar a crescer. Este artigo investiga como um tipo de câncer no sangue, a leucemia mieloide aguda (LMA), desenvolve resistência a um desses medicamentos direcionados, o cabozantinibe, e como reprogramar o uso de energia pelas células cancerosas pode ajudar os médicos a contornar essa resistência.
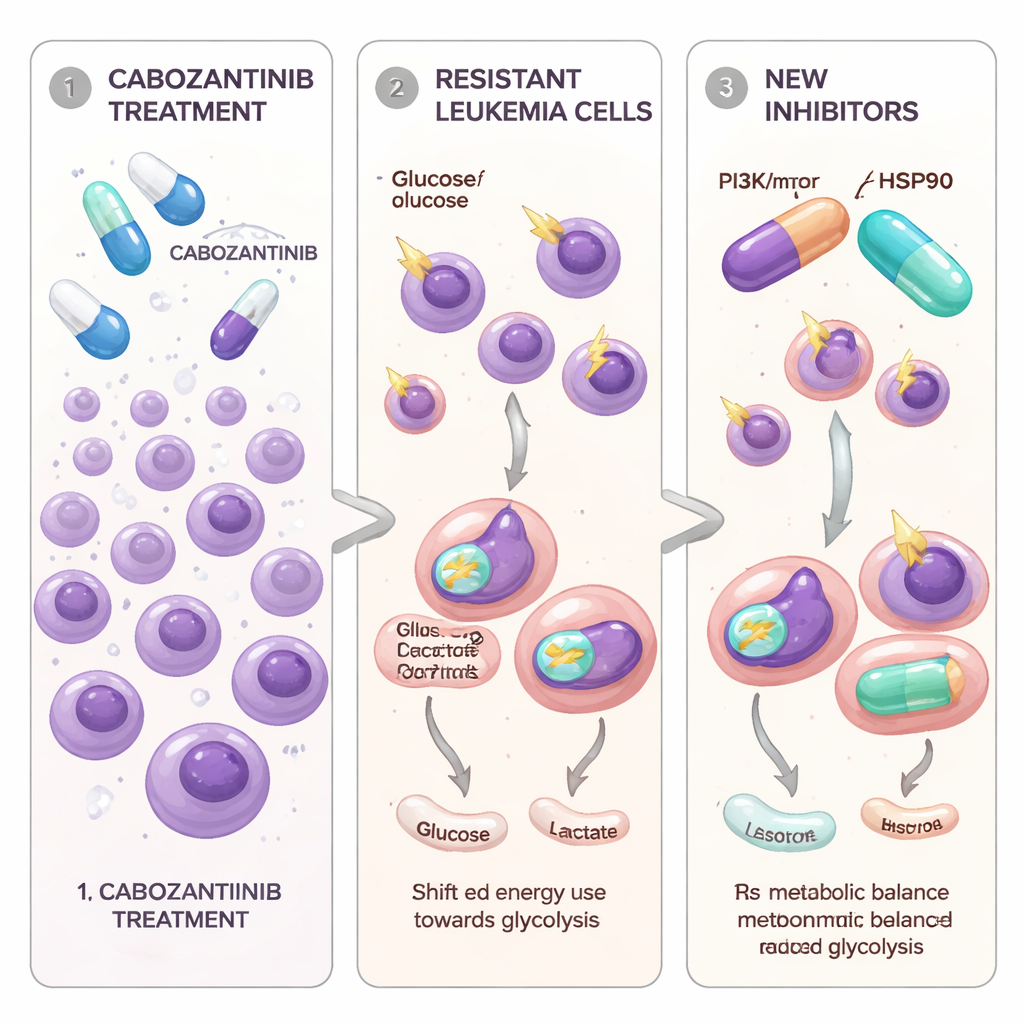
Células leucêmicas que aprendem a escapar de um medicamento direcionado
Os pesquisadores concentraram-se em células de LMA que carregam uma mutação no interruptor de sinal de crescimento chamado FLT3-ITD, conhecida por impulsionar uma doença especialmente agressiva. O cabozantinibe, um comprimido já usado em vários tumores sólidos, pode bloquear fortemente células leucêmicas dirigidas por FLT3 em laboratório. Para modelar o que acontece nos pacientes ao longo do tempo, a equipe expôs gradualmente duas linhagens celulares de LMA com mutação em FLT3 a doses crescentes de cabozantinibe até que algumas células sobreviveram e voltaram a crescer. Essas novas populações celulares, chamadas Molm13‑XR e MV4‑11‑XR, toleraram concentrações de cabozantinibe muitas vezes superiores às das células “parentais” originais. Elas também se tornaram menos sensíveis a dois outros medicamentos aprovados que miram FLT3, sorafenibe e quizartinibe, mantendo-se vulneráveis a um inibidor diferente, o gilteritinibe.
Ajustes genéticos que ajudam o câncer a sobreviver
Ao investigar mais a fundo, os cientistas descobriram que essas células leucêmicas resistentes carregavam novas alterações no gene FLT3. Ambas as linhagens resistentes adquiriram a mesma mutação pontual, chamada D835Y, em uma região crucial do domínio quinase de FLT3, um ponto quente conhecido para resistência a vários fármacos. Uma das linhagens, MV4‑11‑XR, também ganhou uma deleção incomum de 1,3 kilobase que removeu um éxon inteiro de FLT3, apagando parte do domínio importante para a ligação de medicamentos. Essas alterações pareceram ter sido selecionadas durante a exposição prolongada ao cabozantinibe: versões mutantes de FLT3 tornaram-se muito mais comuns nas células resistentes do que na população inicial. Ao mesmo tempo, vias de sinalização chave a montante e a jusante de FLT3 — como ERK, STAT5 e AKT — estavam mais fortemente ativadas, sustentando crescimento mais rápido e maior formação de colônias nas células resistentes.
Células cancerosas trocam o sistema de combustível
A equipe então perguntou se a resistência estava ligada não só à genética, mas também a como as células se abastecem energeticamente. Usando sequenciamento de RNA e testes metabólicos dedicados, eles encontraram um padrão consistente: as células resistentes ao cabozantinibe dependiam muito mais da glicólise — a rápida quebra da glicose no citosol — mesmo quando o oxigênio estava disponível. Essas células captaram mais glicose, produziram mais lactato, exibiram maior atividade de uma enzima chave chamada GAPDH e aumentaram a expressão de múltiplos genes relacionados à glicólise. Em contraste, as mitocôndrias das células, as estruturas que sustentam uma produção de energia mais eficiente, estavam menos ativas e menos abundantes. Medidas do uso de oxigênio revelaram que tanto a respiração mitocondrial basal quanto a máxima estavam reduzidas, e espécies reativas de oxigênio dentro das células estavam elevadas, apontando para mitocôndrias estressadas e com desempenho reduzido.
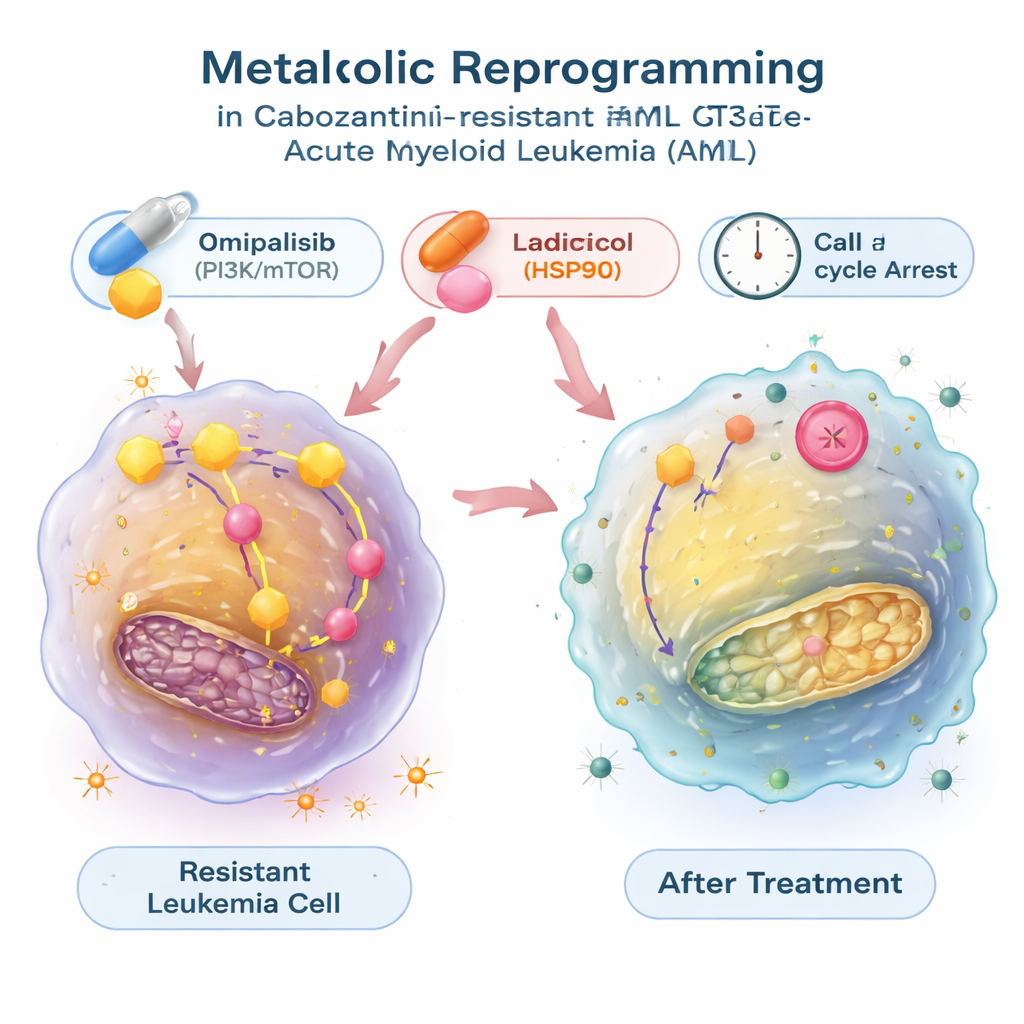
Encontrando fármacos que revertam a chave metabólica
Para ver se essa mudança energética podia ser revertida, os pesquisadores usaram um grande banco de dados público que conecta padrões de expressão gênica com os efeitos de milhares de compostos. Eles buscaram medicamentos previstos para contrariar a assinatura metabólica das células leucêmicas resistentes e focaram em dois: radicicol, que bloqueia uma chaperona proteica chamada HSP90, e omipalisibe, que inibe a via de sinalização PI3K/mTOR que controla crescimento e metabolismo. Em testes de laboratório, ambas as moléculas não apenas retardaram o crescimento das células resistentes, mas também reduziram sua glicólise hiperativa, normalizando a captação de glicose e a liberação de lactato e reduzindo a expressão de genes relacionados à glicólise. Esses compostos empurraram as células leucêmicas para uma fase de repouso do ciclo celular e, no caso do radicicol, também desencadearam morte celular programada substancial. Quando combinados com cabozantinibe, o omipalisibe — e, em um modelo, o radicicol — atuaram sinergicamente, facilitando a eliminação das células resistentes ao medicamento.
O que isso significa para terapias futuras da leucemia
Para não especialistas, a mensagem é que as células leucêmicas podem escapar de um medicamento direcionado não apenas mutando seu alvo direto, mas também mudando como produzem e usam energia. O estudo mostra que células de LMA resistentes ao cabozantinibe adotam uma estratégia de “queima de açúcar” enquanto deixam suas mitocôndrias definhar. Ao atingir as vias que sustentam esse metabolismo reprogramado — por meio de fármacos como omipalisibe ou inibidores de HSP90 — pode ser possível restaurar a sensibilidade ao cabozantinibe e tratamentos similares. Embora essas descobertas provenham de modelos celulares e não de pacientes, elas sugerem que combinar medicamentos direcionados com agentes moduladores do metabolismo pode ser uma abordagem promissora para atrasar ou superar a resistência em LMA com mutação FLT3.
Citação: Fu, YH., Ng, K.M., Tseng, CY. et al. Modulating metabolic signatures to mitigate cabozantinib resistance in FLT3-ITD acute myeloid leukemia cell models. Cell Death Discov. 12, 98 (2026). https://doi.org/10.1038/s41420-026-02957-8
Palavras-chave: leucemia mieloide aguda, resistência a medicamentos, mutação FLT3, metabolismo do câncer, cabozantinibe