Clear Sky Science · pt
Polimerase de DNA kappa estabilizada por Ptbp2 interage com MRE11 e promove instabilidade genômica na leucemia
Como células de leucemia mantêm DNA quebrado e ainda sobrevivem
Nosso DNA está constantemente sob ataque, mas células saudáveis normalmente são muito eficientes em identificar e reparar danos. Na leucemia, entretanto, algumas células aprendem a conviver com DNA quebrado e instável — e até transformam essa instabilidade em uma vantagem de sobrevivência. Este estudo revela uma “parceria” molecular entre uma proteína de splicing (Ptbp2), uma enzima especial de cópia do DNA (polimerase de DNA kappa, ou Polk) e um fator sensor de danos (MRE11) que ajuda células de leucemia a reparar o suficiente para permanecerem vivas, enquanto acumulam o caos genético que impulsiona a progressão do câncer.
Um ajudante oculto nas células de leucemia
Os pesquisadores focaram na leucemia mieloide crônica (LMC), um câncer do sangue geralmente impulsionado pelo gene de fusão BCR::ABL1. Embora medicamentos modernos que bloqueiam BCR::ABL1 funcionem bem em fases iniciais da doença, muitos pacientes que chegam à fase agressiva de “crise blástica” respondem mal. Trabalhos anteriores mostraram que Ptbp2, uma proteína que se liga ao RNA e influencia o processamento das mensagens, é aumentada por BCR::ABL1 e age como um oncogene na LMC. Aqui, a equipe descobriu que Ptbp2 se liga à extremidade final (3′ UTR) do RNA mensageiro de Polk e o protege da degradação. Como resultado, células leucêmicas produzem mais proteína Polk sempre que os níveis de Ptbp2 estão altos.
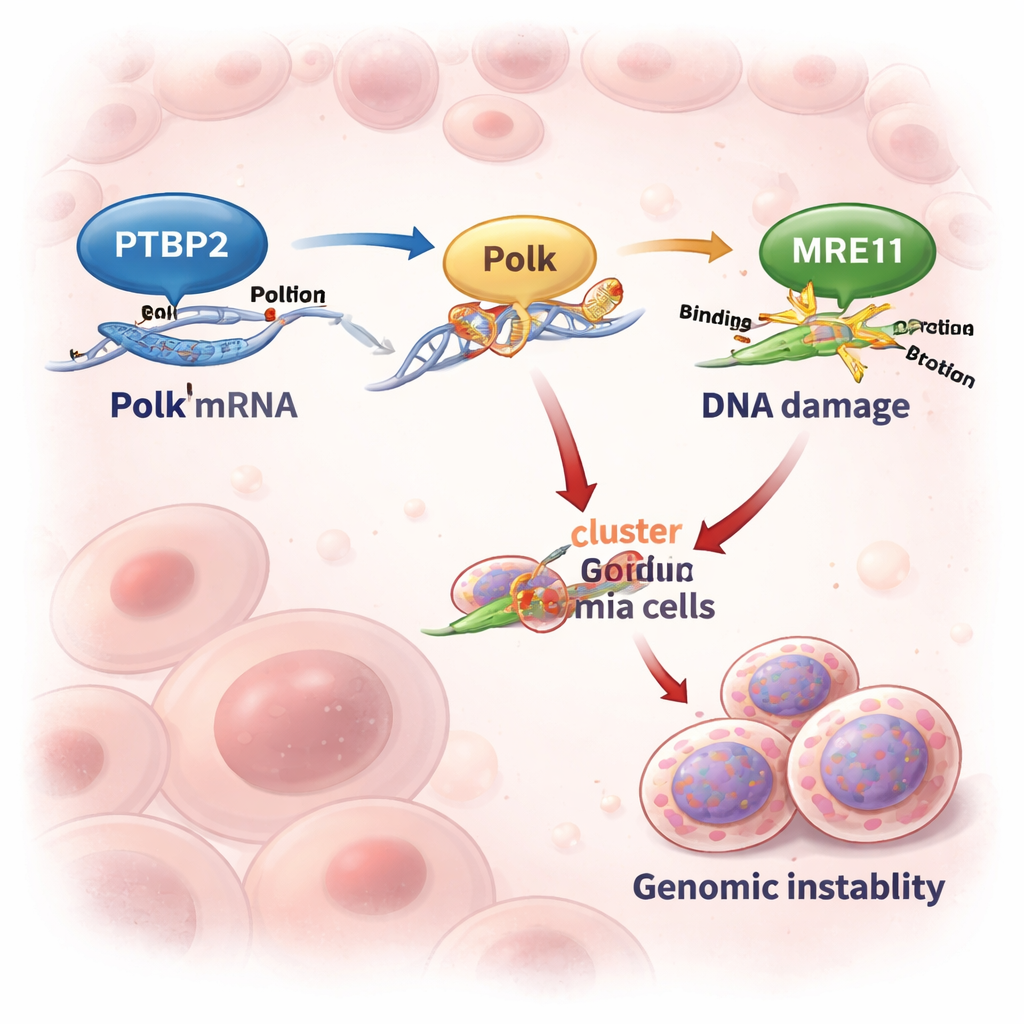
Ligando uma máquina de cópia do DNA propensa a erros
Polk é uma polimerase de DNA “de reserva” que pode copiar por cima de DNA danificado quando a maquinaria usual de replicação trava. Essa capacidade pode salvar células sob estresse — mas tem um custo, porque Polk é propensa a erros e pode introduzir mutações. Em linhagens celulares e amostras de pacientes com LMC avançada, os níveis de Ptbp2 e Polk aumentavam e diminuíam em conjunto. Quando os cientistas eliminaram Ptbp2 em células leucêmicas, os níveis de Polk caíram acentuadamente, e o RNA de Polk decaiu quase duas vezes mais rápido. Reintroduzir Polk em células deficientes em Ptbp2 restaurou seu comportamento, mostrando que o papel principal de Ptbp2 aqui é manter Polk abundante e ativo.
Reparando danos — mas não perfeitamente
Para entender como essa dupla afeta o reparo do DNA, os pesquisadores trataram células com hidroxiureia, um medicamento que atrasa a replicação do DNA e é frequentemente usado em pacientes com LMC. Células sem Ptbp2 sofreram muito mais danos ao DNA, visíveis como longas “caudas de cometa” e focos brilhantes de γH2AX — marcas de cromossomos quebrados. Essas células danificadas tinham maior probabilidade de morrer. Em contraste, células com altos níveis de Ptbp2 e Polk toleraram melhor a droga, repararam danos de forma mais eficiente e sobreviveram, apesar de seu reparo ser descuidado. A superexpressão de Polk em células com knockout de Ptbp2 reverteu essa sensibilidade, confirmando que a parceria Ptbp2–Polk ajuda células leucêmicas a superar estresse de replicação e evitar apoptose.
Uma rede de danos ao DNA que favorece a instabilidade
A história não termina com Polk. A equipe demonstrou que Polk interage fisicamente com MRE11, um membro-chave do complexo MRN que detecta quebras de DNA e ativa a via de resposta a danos ATM–CHK2. Quando Ptbp2 foi removido, Polk diminuiu, os níveis e a atividade de MRE11 declinaram, e a sinalização ATM–CHK2 enfraqueceu. Reintroduzir Polk restaurou MRE11 e sua ativação. Experimentos detalhados com fibras de DNA revelaram que Ptbp2 e Polk ajudam a proteger forquilhas de replicação travadas de serem degradadas, em grande parte por meio de MRE11. Bloquear MRE11 com um medicamento prejudicou essa proteção das forquilhas e aumentou os danos ao DNA. Paradoxalmente, células com sinalização ativa Ptbp2–Polk–MRE11 acumularam mais anomalias cromossômicas, como trocas de cromátides irmãs, quebras, lacunas, fusos multipolares e células gigantes multinucleadas — sinais clássicos de instabilidade genômica que podem nutrir um câncer mais agressivo.
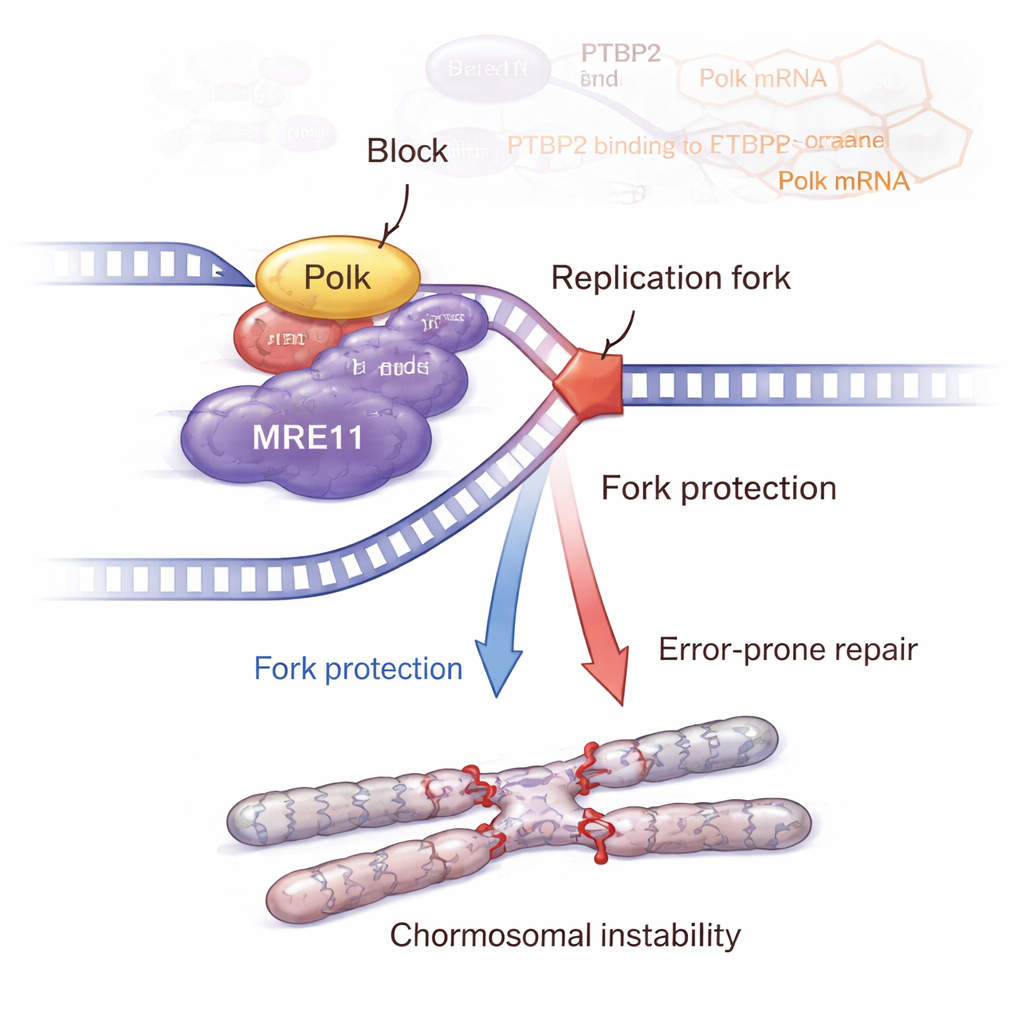
De camundongos a possíveis novos tratamentos
Em modelos de camundongo, células leucêmicas com Ptbp2 intacto produziram tumores maiores e mais anormais do que células sem Ptbp2. Tecidos desses camundongos mostraram níveis mais altos de Ptbp2, Polk, do marcador de proliferação Ki-67 e estruturas de divisão celular distorcidas. Em um modelo separado semelhante à LMC impulsionado por BCR::ABL1, adicionar Ptbp2 extra aumentou Polk e elevou o número de células em divisão atípicas e aglomerados invasivos de leucemia no baço e no fígado, apontando para uma progressão mais rápida da doença. Em conjunto, esses achados sugerem que o eixo Ptbp2–Polk–MRE11–ATM–CHK2 permite que células leucêmicas sobrevivam a intenso estresse no DNA enquanto acumulam continuamente mutações prejudiciais.
Por que isso importa para os pacientes
Para um leigo, a mensagem principal é que algumas células de leucemia escapam do controle ao andar numa corda bamba: elas consertam o DNA o suficiente para permanecerem vivas, mas não tão bem a ponto de evitar mutações. Ptbp2 estabiliza Polk, que então se junta a MRE11 para proteger DNA estressado e manter sinais de dano ativos — porém esse reparo é imperfeito e promove o caos genético. Como LMC avançada e outros cânceres parecem depender desse equilíbrio frágil, mirar Ptbp2 ou seu controle sobre Polk pode inclinar as células para longe da sobrevivência e em direção à autodestruição, oferecendo um novo e promissor caminho para terapias, especialmente no estágio de crise blástica de difícil tratamento.
Citação: Lama, S., Barik, B., IS, S. et al. DNA polymerase kappa stabilized by Ptbp2 interacts with MRE11 and promotes genomic instability in leukemia. Cell Death Discov. 12, 96 (2026). https://doi.org/10.1038/s41420-026-02951-0
Palavras-chave: leucemia mieloide crônica, instabilidade genômica, reparo de DNA, polimerase de DNA kappa, PTBP2