Clear Sky Science · pt
Desvendando vulnerabilidades do glioma: direcionando vias de morte celular regulada para terapias inovadoras
Por que a morte das células tumorais cerebrais importa
Os gliomas estão entre os tumores cerebrais mais comuns e letais em adultos. Mesmo com cirurgia, radioterapia e quimioterapia, eles frequentemente retornam e são difíceis de controlar. Este artigo de revisão explora um novo ângulo de ataque: explorar as diferentes maneiras pelas quais as células podem ser programadas para morrer. Ao entender e direcionar essas rotas de “autodestruição”, os pesquisadores esperam expor fragilidades nas células de glioma e tornar tratamentos futuros mais eficazes e mais personalizados.
Como os gliomas driblam os tratamentos padrão
Os gliomas surgem das células de suporte do cérebro e variam de formas de crescimento lento a formas altamente agressivas, como o glioblastoma. Seus desfechos ruins decorrem de vários problemas interligados: mutações genéticas, alterações epigenéticas, células com características de células-tronco difíceis de eliminar, suprimento sanguíneo anormal e um ambiente imune fortemente supressor. Além disso, a barreira hematoencefálica limita a eficácia com que os fármacos alcançam o tumor. Em conjunto, esses fatores permitem que as células tumorais sobrevivam à cirurgia e aos fármacos padrão, se adaptem ao estresse e, eventualmente, reapareçam. 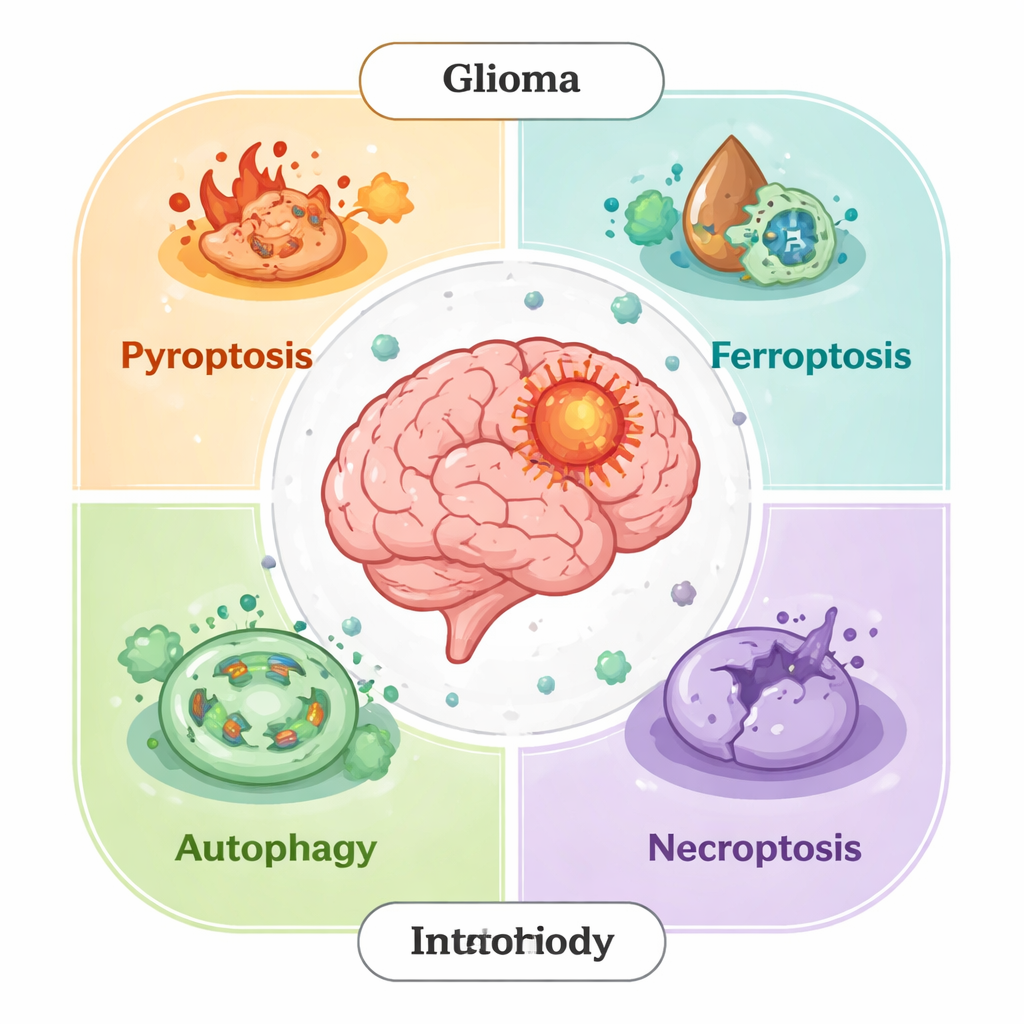
As muitas faces da autodestruição celular
Durante décadas, os cientistas concentraram-se em uma forma principal de morte celular programada, chamada apoptose. Hoje sabemos que isso é apenas parte da história. Células de glioma também podem morrer por outras vias reguladas: piroptose (uma explosão inflamatória e “ardente”), ferroptose (dano de membrana impulsionado por ferro), necroptose (uma versão controlada da ruptura celular) e morte dependente de autofagia (autodigestão que pode ir longe demais). Em tecidos saudáveis, esses processos removem células danificadas e previnem o câncer. Nos tumores, entretanto, as células de glioma frequentemente reprogramam essas vias — bloqueando sinais de morte, aumentando defesas antioxidantes ou convertendo a autofagia em uma ferramenta de sobrevivência — para resistir ao tratamento e moldar um microambiente que favoreça seu crescimento.
Convertendo vias de morte em terapia
Em vez de ver essas rotas de morte como um problema, os pesquisadores aprendem a transformá-las em armas. Estratégias que induzem piroptose usam nanopartículas inteligentes, aquecimento por luz, vírus modificados ou hidrogeis carregados com fármacos para fazer as células de glioma incharem, rompam e liberem sinais de perigo que alertam o sistema imune. Abordagens baseadas em ferroptose forçam as células tumorais a um colapso alimentado por ferro, bloqueando enzimas protetoras chave como GPX4, interrompendo a produção de glutationa ou alterando como as células tratam os lipídios. Muitas dessas táticas são entregues com veículos avançados, incluindo graphdiyne e outras nanopartículas, para ajudar os fármacos a atravessar a barreira hematoencefálica e se concentrar no interior do tumor, poupando o tecido cerebral saudável. 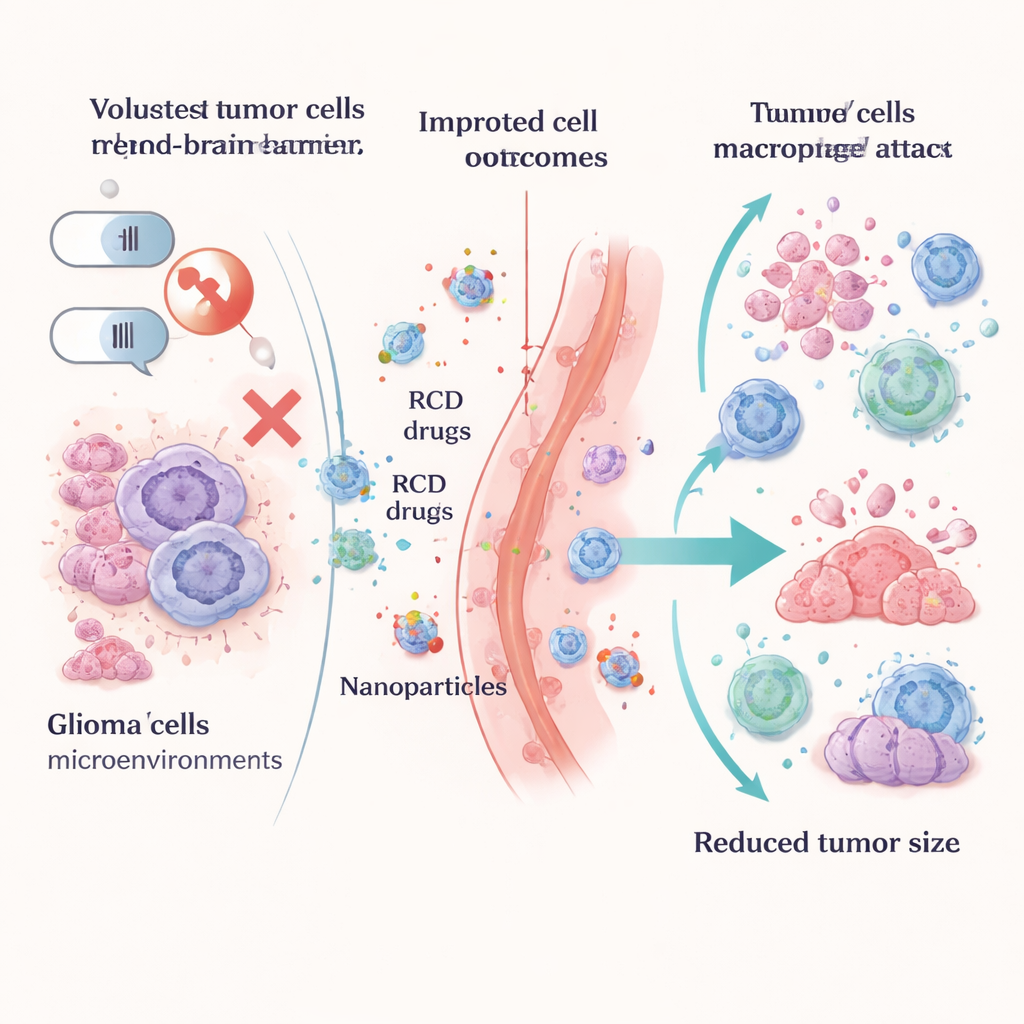
Reiniciando a paisagem imune do tumor
Terapias focadas em necroptose buscam superar a resistência em células que não respondem mais aos sinais de morte padrão. Produtos naturais como shikonina, emodina e derivados de celastrol podem empurrar as células de glioma para a necroptose, que não apenas as mata, mas também libera moléculas que atraem células imunes para o tumor. Ao mesmo tempo, os cientistas investigam a autofagia, às vezes bloqueando-a para impedir que as células tumorais usem a “auto-limpeza” para resistir à radiação e à quimioterapia, e às vezes estimulando-a além do limite para desencadear a morte celular. Ensaios clínicos iniciais com fármacos como cloroquina e hidroxicloroquina mostram que a autofagia pode ser modulada com segurança em pacientes, embora benefícios claros de sobrevida ainda não tenham sido comprovados.
Das descobertas de laboratório ao cuidado personalizado
Traduzir esses conceitos em tratamentos do mundo real continua desafiador. Os gliomas são altamente variados entre pacientes e mesmo dentro de um único tumor, portanto nenhuma estratégia de via de morte servirá para todos. A barreira hematoencefálica ainda dificulta a entrega de fármacos, e o microambiente imune pode neutralizar até combinações engenhosas de terapias. Os autores destacam direções promissoras: combinar indutores de ferroptose com inibidores de checkpoint imunológico, juntar vírus oncolíticos com fármacos que aumentam sinais de “me coma” nas células cancerosas, ou adicionar moduladores de autofagia a regimes selecionados de quimiorradiação. Perfis multi-ômicos e melhores biomarcadores devem ajudar a identificar quais pacientes têm maior probabilidade de se beneficiar de uma dada combinação de estratégias.
Olhando adiante: fazer o tumor optar pela autodestruição
Em termos simples, este artigo conclui que o futuro do tratamento do glioma pode residir em forçar as células tumorais a apertarem seus próprios botões de autodestruição de forma cuidadosamente controlada. Ao aprender a desencadear e coordenar piroptose, ferroptose, necroptose e morte dependente de autofagia — e ao acoplar essas vias com imunoterapias modernas e entrega precisa de fármacos — os pesquisadores esperam transformar um diagnóstico hoje sombrio em algo mais manejável e, em última análise, mais curável.
Citação: Guo, J., Zong, L., Huang, Y. et al. Unlocking glioma vulnerabilities: targeting regulated cell death pathways for innovative therapies. Cell Death Discov. 12, 95 (2026). https://doi.org/10.1038/s41420-026-02949-8
Palavras-chave: glioma, morte celular regulada, piropOptose, ferroptose, terapia do glioblastoma