Clear Sky Science · pt
Mitofagia no câncer de pâncreas: percepções mecanísticas e implicações para novas estratégias terapêuticas
Por que as usinas de energia das nossas células importam no câncer de pâncreas
O adenocarcinoma ductal pancreático é um dos cânceres mais letais, em parte porque os tumores aprendem rapidamente a resistir a quase todo tratamento que os médicos aplicam. Este artigo de revisão explora um protagonista surpreendente nessa história de resistência: a mitofagia, o sistema intrínseco da célula para identificar e reciclar mitocôndrias desgastadas, as pequenas “usinas de energia” que geram energia. Entender como o câncer de pâncreas sequestra esse processo de limpeza pode abrir novos caminhos para terapias mais eficazes e duradouras.
Equipes de limpeza celulares e os truques de sobrevivência do câncer
As mitocôndrias fazem muito mais do que gerar energia; elas ajudam a controlar o metabolismo, a morte celular e o manejo de moléculas nocivas chamadas espécies reativas de oxigênio. Quando mitocôndrias são danificadas ou excessivas, as células usam a mitofagia para marcá‑las e removê‑las. Isso pode ocorrer por duas rotas principais. Uma, conhecida como via PINK1/Parkin, depende de um sensor de dano (PINK1) e de uma enzima de marcação (Parkin) para sinalizar mitocôndrias defeituosas para destruição. A outra usa proteínas receptoras como BNIP3, NIX e FUNDC1 presentes na superfície mitocondrial para conectá‑las diretamente às bolsas de descarte celular, chamadas autofagossomos, sem o mesmo passo de marcação. Essas vias frequentemente atuam em conjunto, oferecendo às células maneiras flexíveis de ajustar seu estoque mitocondrial a estresses como baixa oxigenação ou exposição a fármacos. 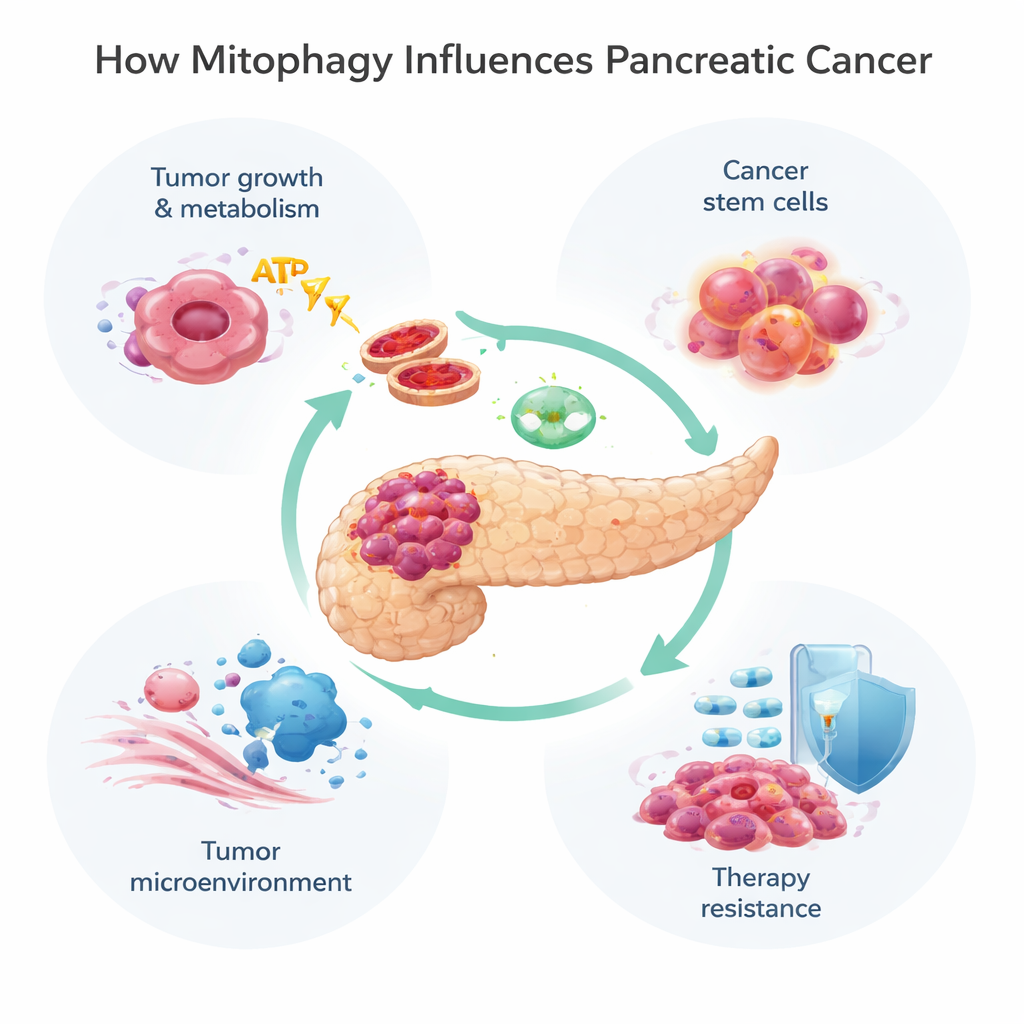
Como os tumores pancreáticos remodelam seu uso de energia
Os tumores pancreáticos vivem em um ambiente hostil: são mal supridos de sangue e oxigênio e circundados por um tecido denso semelhante a cicatriz. Para sobreviver, as células cancerosas reprogramam seus sistemas energéticos, muitas vezes mudando da respiração mitocondrial dependente de oxigênio para um processo mais primitivo de queima de açúcar conhecido como glicólise. A mitofagia ajuda a ajustar essa mudança. No estágio inicial do desenvolvimento tumoral, a perda de PINK1 ou Parkin acelera a formação do câncer ao permitir acúmulo de ferro, excesso de espécies reativas de oxigênio e um deslocamento para a glicólise. Ao mesmo tempo, outra proteína de mitofagia, NIX, pode ajudar a remover mitocôndrias ainda funcionais, empurrando as células ainda mais para o metabolismo glicolítico e crescimento mais rápido. Em contraste, BNIP3 mostra um padrão mais complexo: parece presente precocemente, é mais tarde silenciada em muitos tumores avançados e, quando restaurada, pode desacelerar o crescimento das células cancerosas, sugerindo que algumas vias de mitofagia restringem o câncer enquanto outras o alimentam.
Células‑tronco cancerosas e o microambiente tumoral
Nem todas as células cancerosas são iguais. Um subconjunto pequeno, frequentemente chamado de células‑tronco cancerosas, pode autorrenovar‑se, gerar novos tumores e resistir particularmente bem à quimioterapia. No câncer de pâncreas, essas células dependem da mitofagia para manter flexibilidade metabólica. Uma proteína modificadora chamada ISG15 sustenta esse processo e ajuda a preservar traços de tipo‑tronco, ligando a mitofagia diretamente à recidiva e ao insucesso do tratamento. Além das próprias células cancerosas, a mitofagia também molda o microambiente tumoral — a mistura de células de suporte, células imunes e tecido conjuntivo ao redor do tumor. Fibroblastos associados ao câncer, por exemplo, podem ser levados a um “efeito Warburg reverso”, no qual aumentam sua própria mitofagia e glicólise e então alimentam o tumor com subprodutos ricos em energia. A mitofagia também influencia como células imunes reconhecem e atacam o câncer, ao alterar a exibição de sinais imunes como MHC‑I e de freios como PD‑L1 que os tumores usam para se esconder.
Por que bloquear ou impulsionar a limpeza pode alterar a resposta a medicamentos
Muitos tratamentos padrão e experimentais para o câncer de pâncreas, incluindo a quimioterapia com gemcitabina e um novo fármaco direcionado contra a mutação comum KRAS‑G12D, lesionam mitocôndrias. As células tumorais frequentemente respondem ativando a mitofagia, eliminando o dano e escapando da morte. Estudos mostram que a mitofagia conduzida por PINK1 pode atenuar os efeitos letais da quimioterapia e de alguns compostos naturais, ajudando as células tumorais a sobreviver. Por outro lado, sob certas condições, forçar demais a mitofagia — especialmente via BNIP3 e NIX — pode privar as células de mitocôndrias funcionais em excesso, empurrando‑as para uma crise energética e promovendo a morte celular. Essa natureza dual significa que a mitofagia pode tanto proteger tumores do tratamento quanto, se direcionada corretamente, torná‑los mais vulneráveis. 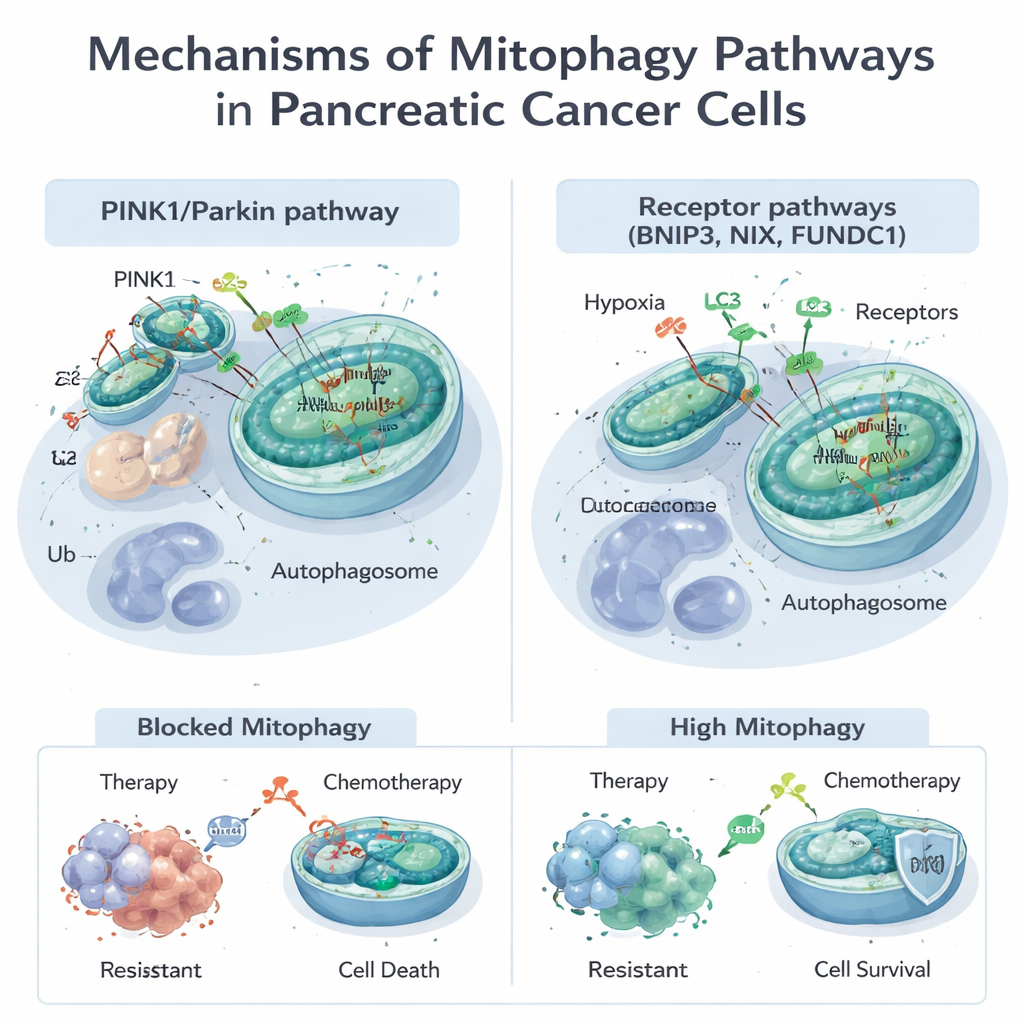
Novas ideias de tratamento e a necessidade de pareamento inteligente dos pacientes
Como a mitofagia está no cruzamento entre metabolismo, respostas ao estresse e morte celular, ela é um alvo atraente para terapias combinadas. As estratégias farmacológicas atuais atuam principalmente de forma indireta: alguns compostos interferem com a fissão e fusão mitocondrial; outros, como a cloroquina e a hidroxicloroquina, bloqueiam as etapas finais do processo de reciclagem ao impedir a fusão dos sacos de descarte com compartimentos ácidos de degradação. Vários ensaios clínicos testam esses fármacos em combinação com quimioterapia padrão no câncer de pâncreas. Ainda assim, os resultados até agora são mistos — alguns pacientes se beneficiam, outros não. Parte do problema é que os tumores diferem amplamente em seus níveis basais de mitofagia e perfis metabólicos: alguns dependem fortemente da respiração mitocondrial, outros da glicólise. Os autores sustentam que o sucesso futuro dependerá de melhores biomarcadores e assinaturas genéticas para agrupar pacientes pela atividade da mitofagia e pelo uso de energia, e do desenvolvimento de fármacos mais precisos que ajustem seletivamente vias específicas de mitofagia em vez de simplesmente ligar ou desligar a autofagia. Para leitores leigos, a conclusão principal é que aprender a ler e a ajustar cuidadosamente esse sistema de limpeza mitocondrial pode ajudar a transformar o câncer de pâncreas de um adversário resistente em uma doença mais manejável.
Citação: Wang, Z., Lyu, Z., Palmen, R. et al. Mitophagy in pancreatic cancer: mechanistic insights and implications for novel therapeutic strategies. Cell Death Discov. 12, 93 (2026). https://doi.org/10.1038/s41420-026-02948-9
Palavras-chave: câncer de pâncreas, mitofagia, mitocôndrias, resistência à quimioterapia, metabolismo tumoral