Clear Sky Science · pt
Células-tronco mesenquimais primadas atenuam a fibrose por esquistossomose ao promover mudança de subtipos de macrófagos e efarocitose via eixo Itgb2-Rac1
Reduzindo Cicatrizes no Fígado Causadas por um Parasita Comum
A esquistossomose, uma doença parasitária que afeta mais de 200 milhões de pessoas no mundo, frequentemente deixa cicatrizes persistentes no fígado mesmo após a eliminação dos vermes. Essas cicatrizes, conhecidas como fibrose, podem evoluir para cirrose e insuficiência hepática potencialmente fatal. Este estudo investiga um novo tratamento celular que ensina as próprias células imunes do organismo a limpar os danos com maior eficiência, oferecendo uma nova abordagem para reverter a fibrose hepática induzida por parasitas.
Por que as Cicatrizes no Fígado Custam a Cicatrizar
Quando os vermes Schistosoma depositam ovos no fígado, o sistema imunológico forma aglomerados densos de células — granulomas — ao redor deles. Com o tempo, essa resposta protetora deposita tecido cicatricial em excesso, gradualmente tornando o fígado mais rígido. Um papel central nesse processo é desempenhado pelos macrófagos, a equipe de limpeza do organismo. Um subtipo, chamado macrófagos “inflamatórios”, alimenta o dano ao liberar sinais químicos agressivos; outro subtipo, mais “resolutivo”, ajuda a degradar o tecido cicatricial e a acalmar a inflamação. A questão central deste trabalho é se podemos, com segurança, direcionar os macrófagos do estado danoso para o estado reparador.
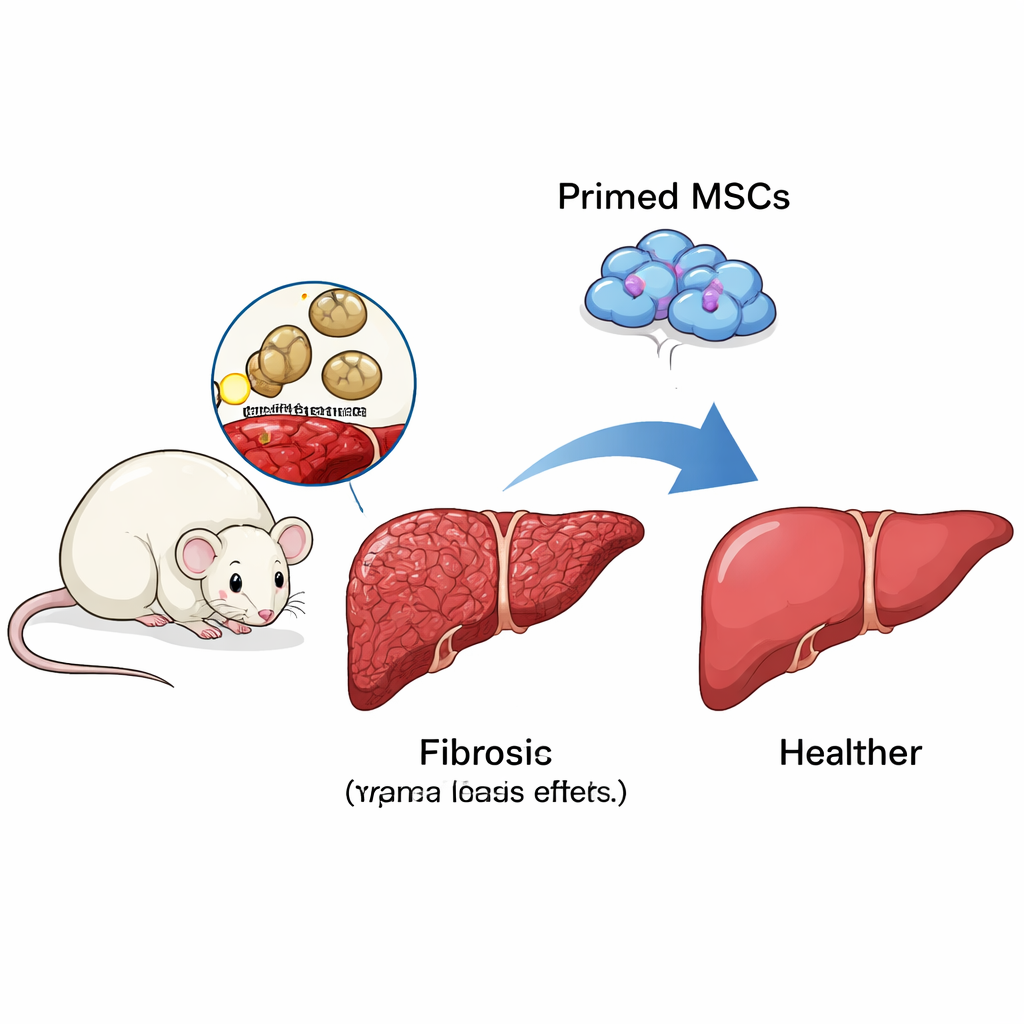
Treinando Células-tronco para Guiar o Sistema Imune
As células-tronco mesenquimais (CTMs) — células versáteis encontradas na medula óssea e em outros tecidos — atraíram atenção como um possível tratamento para a fibrose hepática. Sozinhas, porém, nem sempre funcionam bem. Os pesquisadores descobriram que “primar” as CTMs em laboratório com dois sinais imunes, IFN‑γ e LPS, melhorou dramaticamente seu desempenho em camundongos infectados por Schistosoma japonicum. Em comparação com animais não tratados ou com CTMs não primadas, os camundongos que receberam CTMs primadas tinham fígados com aspecto mais saudável a olho nu, ganharam mais peso e mostraram granulomas muito menores e menor acúmulo de colágeno ao microscópio. Marcadores de células ativadas formadoras de cicatriz também diminuíram, indicando uma redução real da fibrose, não apenas mudanças cosméticas.
Reprogramando a Equipe de Limpeza do Corpo
Indo mais a fundo, a equipe mediu como as CTMs primadas afetavam o comportamento dos macrófagos. Nos fígados tratados, havia menos macrófagos inflamatórios e mais do subtipo pró-resolutivo, que é melhor em desmontar o tecido cicatricial. Ao mesmo tempo, os níveis de moléculas inflamatórias clássicas caíram, enquanto fatores úteis à cicatrização foram mantidos numa faixa equilibrada em vez de serem levados a extremos. Quando os pesquisadores bloquearam a chegada de novos macrófagos inflamatórios ao fígado, tanto o número de células resolutivas quanto os benefícios sobre a fibrose diminuíram. Isso sugere que as CTMs primadas não apenas acrescentam novas células, mas convertem macrófagos inflamatórios em trânsito para uma forma mais pacífica e orientada à reparação.
Ajudando os Macrófagos a Comerem até a Cura
O estudo então abordou um processo chamado efarocitose — a “comida” ordenada de células moribundas, em especial neutrófilos gastos, outro tipo de célula imune. Em camundongos infectados tratados com CTMs primadas, os macrófagos hepáticos apresentaram muito mais probabilidade de conter neutrófilos ingeridos, sinal de uma limpeza ativa. Em pratos de cultura, macrófagos expostos a CTMs primadas tornaram-se melhores em engolir neutrófilos apoptóticos marcados e, paralelamente, alteraram sua atividade gênica para um perfil pró-resolutivo. Os pesquisadores identificaram um ponto molecular chave para essa mudança: um receptor chamado Itgb2 nos macrófagos, que se comunica com um interruptor interno, Rac1, que controla o citoesqueleto e o movimento de englobamento da célula. As CTMs primadas aumentaram tanto a atividade de Itgb2 quanto de Rac1; bloquear qualquer um deles reduziu fortemente a efarocitose e reverteu a mudança para macrófagos do tipo reparador.
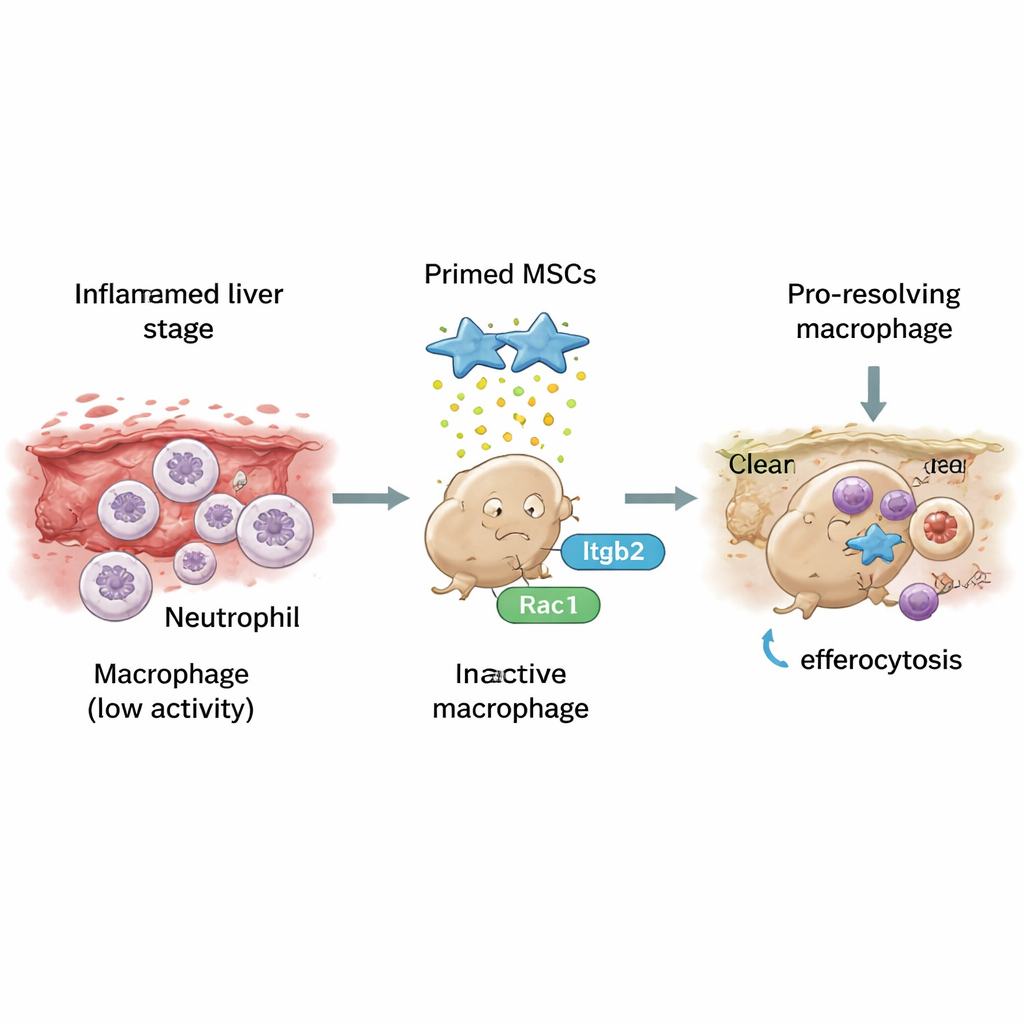
O Que Isso Pode Significar para Tratamentos Futuros
Em termos simples, o trabalho mostra que células-tronco especialmente primadas podem atuar como “treinadoras” para células imunes após a esquistossomose, encorajando-as a parar de alimentar a inflamação e, em vez disso, limpar detritos e tecido cicatricial com maior eficiência. Ao ativar a via Itgb2–Rac1, essas CTMs primadas ajudam os macrófagos a eliminar suavemente células moribundas e, em seguida, a adotar uma personalidade que resolve cicatrizes. Embora ainda falte muito para que essa abordagem possa ser testada em humanos, o estudo fornece um roteiro mecanístico claro para projetar terapias baseadas em CTMs que não apenas suprimam o dano, mas ajudem ativamente o fígado a reconstruir-se após a infecção parasitária.
Citação: Lei, J., Ren, Y., Chen, Z. et al. Primed mesenchymal stem cells attenuate schistosomiasis fibrosis by enhancing macrophage subset switching and efferocytosis via Itgb2-Rac1 axis. Cell Death Discov. 12, 97 (2026). https://doi.org/10.1038/s41420-026-02947-w
Palavras-chave: esquistossomose, fibrose hepática, células-tronco mesenquimais, macrófagos, efarocitose