Clear Sky Science · pt
Câncer colorretal derivado de osteopontina reprograma macrófagos para um estado M2 promotor de metástase via o eixo PI3K/AKT/CSF1-CSF1R
Por que isto importa para pessoas com câncer de cólon
A maioria das mortes por câncer colorretal (do cólon e do reto) não é causada pelo tumor original, mas pela sua disseminação para outros órgãos. Este estudo investiga como as células tumorais "conversam" com células imunes próximas para facilitar a propagação do tumor. Ao descobrir uma mensagem-chave que as células cancerígenas enviam para reprogramar células imunes em auxiliares em vez de combatentes, o trabalho aponta para novas estratégias terapêuticas que podem retardar ou impedir a metástase em casos avançados de câncer colorretal.
Uma proteína pegajosa com um lado sombrio
Os pesquisadores focaram em uma proteína chamada osteopontina, ou OPN, produzida tanto por células tumorais quanto por certos tipos de células imunes dentro dos tumores. A OPN há muito está associada a piores desfechos em vários cânceres, mas o modo exato como ela promove a disseminação no câncer colorretal era incerto. Ao analisar grandes bases de dados de pacientes e amostras tumorais, a equipe constatou que os níveis de OPN eram muito mais altos em tecido de câncer colorretal do que em tecido de cólon normal, especialmente em pacientes com doença avançada e metástases distantes. Pacientes cujos tumores apresentavam mais OPN geralmente tinham sobrevida pior, sugerindo que a OPN está fortemente ligada a tumores agressivos e de difícil tratamento.
Não são só as próprias células cancerosas
Surpreendentemente, quando os cientistas forçaram células de câncer colorretal em laboratório a produzir mais ou menos OPN, as células não se tornaram mais invasivas ou móveis por si mesmas. Seu crescimento, migração e capacidade de invadir através de membranas artificiais mudaram muito pouco. Isso contestou a ideia comum de que a OPN atua principalmente fortalecendo diretamente as próprias células cancerosas. Em vez disso, a equipe examinou a vizinhança do tumor — o chamado microambiente tumoral — especialmente um grupo de células imunes chamadas macrófagos, que podem tanto atacar tumores (estado “M1”) quanto apoiá-los (estado “M2”).
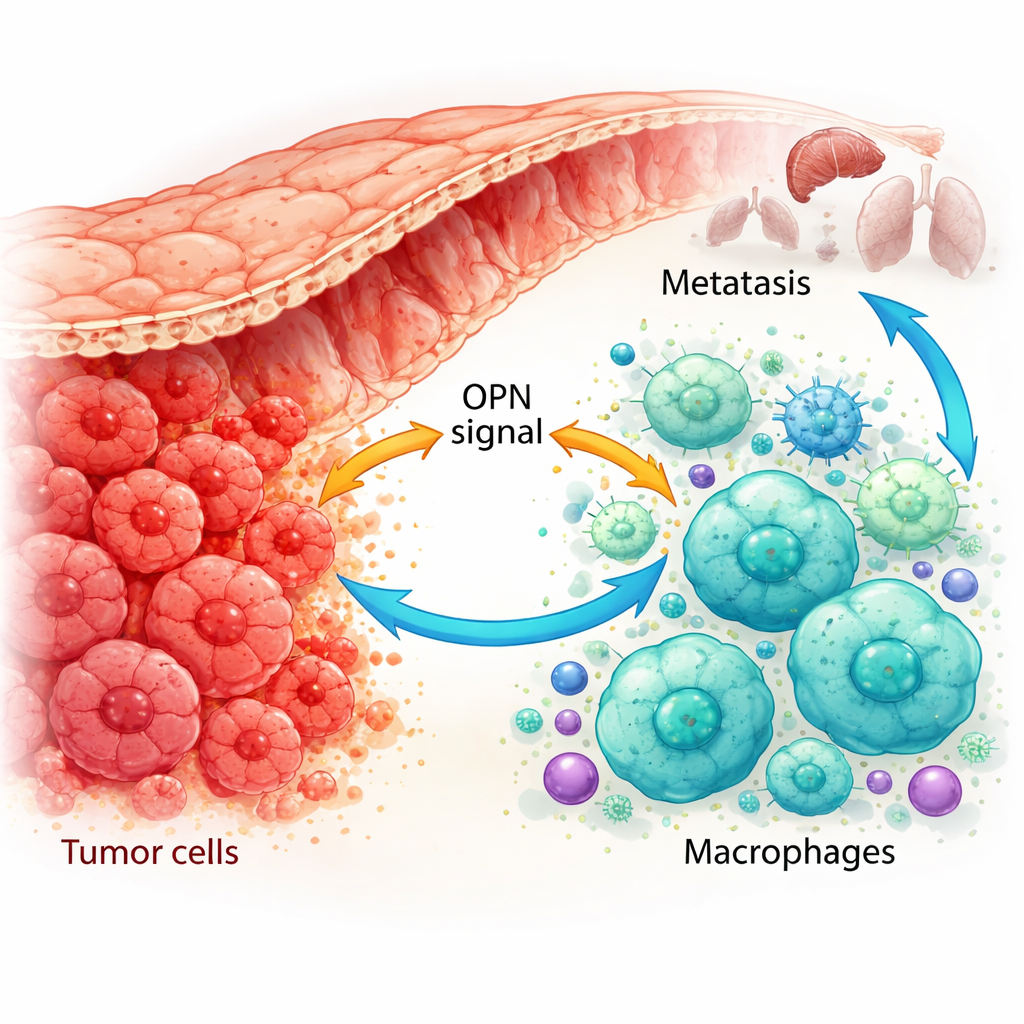
Como as células imunes são reprogramadas em cúmplices do tumor
Usando mapas genéticos de célula única e colorações avançadas de tecidos de pacientes, os pesquisadores demonstraram que a OPN é produzida não apenas por células tumorais, mas também por macrófagos associados ao tumor. Em tumores que já haviam se espalhado, tanto as células cancerosas quanto um subtipo específico de macrófagos eram ricos em OPN. Esses macrófagos tendiam a apresentar um estado semelhante a M2, de suporte ao tumor, e eram mais abundantes quando os níveis de OPN no tumor eram altos. Em modelos murinos, tumores engenheirados para produzir mais OPN atraíam mais desses macrófagos tipo M2 e cresciam mais rapidamente, enquanto tumores com OPN reduzida tinham menos macrófagos M2 e cresciam mais lentamente. Isso sugere que a OPN é um poderoso recrutador e reprogramador de macrófagos no ambiente tumoral.
A cadeia de sinalização oculta: da OPN à metástase
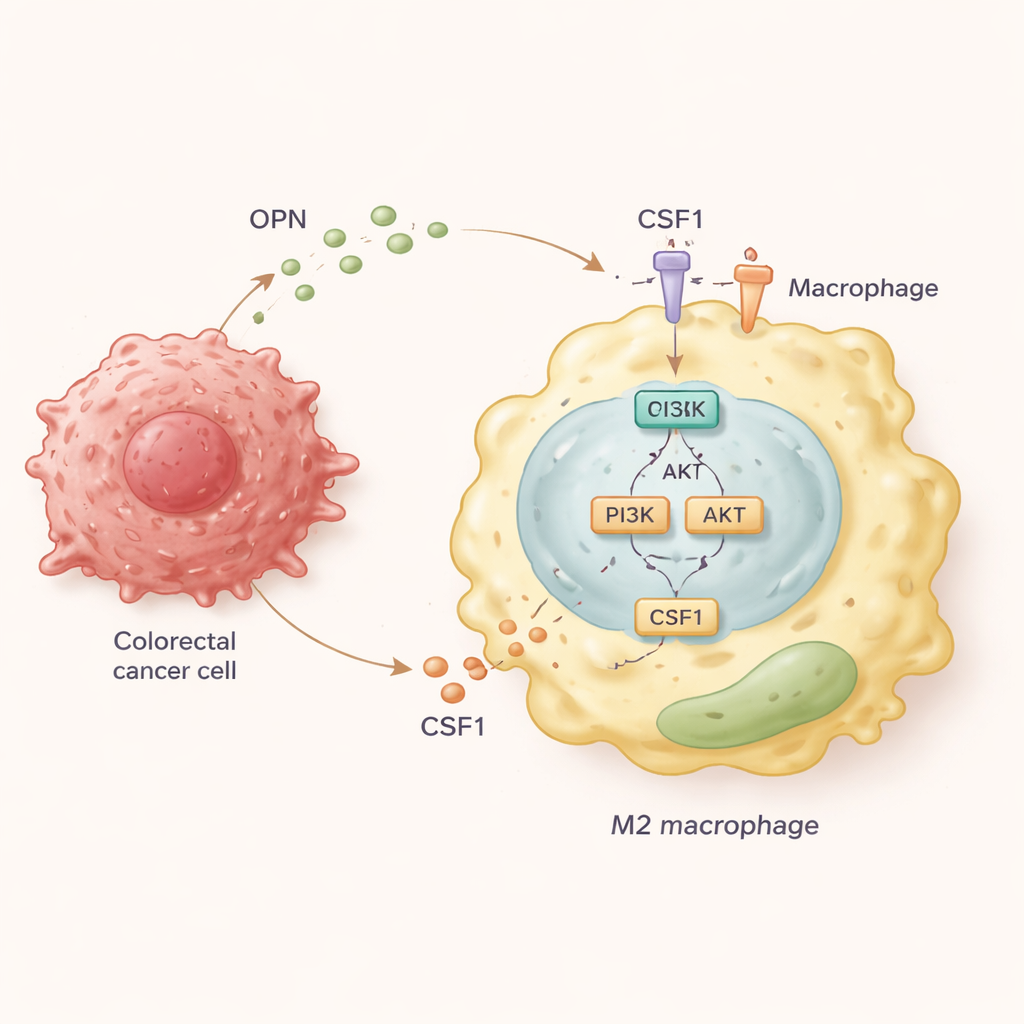
Para elucidar a sequência molecular de eventos, a equipe cultivou macrófagos humanos junto com células de câncer colorretal produzindo quantidades diferentes de OPN. Eles descobriram que células tumorais com alta OPN empurravam macrófagos em direção ao estado M2 e estimulavam um movimento bidirecional: macrófagos migravam em direção ao tumor, e as células tumorais tornavam-se mais invasivas em resposta a sinais desses macrófagos. Investigando mais a fundo, os cientistas descobriram que a OPN ativa uma via de sinalização dentro dos macrófagos chamada PI3K/AKT. Essa ativação, por sua vez, faz com que os macrófagos liberem grandes quantidades de outra molécula, CSF1, e aumentem o receptor dessa molécula, CSF1R, em sua superfície. O CSF1 então atua em um circuito que reforça o estado M2 pró-metastático e continua atraindo macrófagos para o tumor.
Bloquear o circuito para frear a disseminação
Em modelos murinos de câncer colorretal que haviam se espalhado dentro do abdome, os pesquisadores testaram um medicamento bloqueador de CSF1R chamado PLX3397. Camundongos com tumores ricos em OPN desenvolveram muitos nódulos metastáticos, mas o tratamento com o inibidor de CSF1R reduziu significativamente tanto o número de metástases quanto a presença de macrófagos do tipo M2 nos tumores. As células tumorais exibiram menor crescimento e mais sinais de morte celular programada. Importante, a droga reduziu sobretudo os macrófagos que promovem o tumor sem afetar de forma marcante o tipo mais inflamatório, sugerindo uma maneira relativamente direcionada de enfraquecer o sistema de suporte do tumor.
O que isso significa para tratamentos futuros
Para o público leigo, a principal mensagem é que alguns cânceres colorretais conseguem se espalhar não apenas porque as células cancerosas são agressivas, mas porque sequestram células imunes próximas e as transformam em cúmplices. Neste estudo, a OPN derivada das células tumorais atua como um interruptor mestre que reprograma macrófagos através da via de sinalização PI3K/AKT e do circuito CSF1/CSF1R, criando um terreno fértil para a metástase. Ao quebrar essa cadeia — particularmente no passo do CSF1R — os pesquisadores conseguiram reduzir a disseminação tumoral em camundongos. Isso sugere que medir os níveis de OPN pode ajudar a identificar pacientes que poderiam se beneficiar de drogas que miram macrófagos, e que combinar tais drogas com tratamentos existentes ou imunoterapias pode oferecer novas esperanças para pessoas com câncer colorretal avançado.
Citação: Liang, X., Qin, F., Yuan, Z. et al. Colorectal cancer-derived osteopontin rewires macrophages into a pro-metastatic M2 state via the PI3K/AKT/CSF1-CSF1R axis. Cell Death Discov. 12, 92 (2026). https://doi.org/10.1038/s41420-026-02945-y
Palavras-chave: câncer colorretal, osteopontina, macrófagos associados a tumor, metástase, inibição de CSF1R