Clear Sky Science · pt
Trim15 estabiliza VDAC3 via ubiquitinação para suprimir a autofagia e aumentar a quimiossensibilidade no carcinoma espinocelular de hipofaríngeo
Por que este estudo sobre câncer é importante
O carcinoma espinocelular de hipofaríngeo é um câncer de garganta de difícil tratamento, com baixas taxas de sobrevida e poucas opções eficazes quando se dissemina ou deixa de responder aos medicamentos. Este estudo revela uma via celular oculta que ajuda a determinar se essas células cancerosas morrem durante o tratamento ou silenciosamente se adaptam e sobrevivem. Ao explicar como duas proteínas, Trim15 e VDAC3, controlam a autolimpeza celular e as respostas ao estresse, o trabalho aponta caminhos potenciais para tornar os quimioterápicos existentes mais eficazes.
Um câncer de garganta letal que se esconde à vista
A hipofaringe fica profunda na garganta, de modo que os tumores ali frequentemente crescem sem ser notados até atingirem um estágio avançado. Nesse ponto, os médicos precisam escolher entre cirurgia agressiva — que pode afetar severamente fala e deglutição — ou abordagens de preservação do órgão, como quimioterapia e radioterapia, que nem sempre curam a doença. Como a sobrevida não melhorou muito nas últimas décadas, os pesquisadores procuram além dos tratamentos tradicionais, investigando a biologia subjacente que permite a esses tumores crescer, se espalhar e resistir aos medicamentos. O estudo atual foca em como as células cancerosas lidam com mitocôndrias danificadas — suas usinas de energia — e como isso molda sua resposta ao estresse e à terapia.
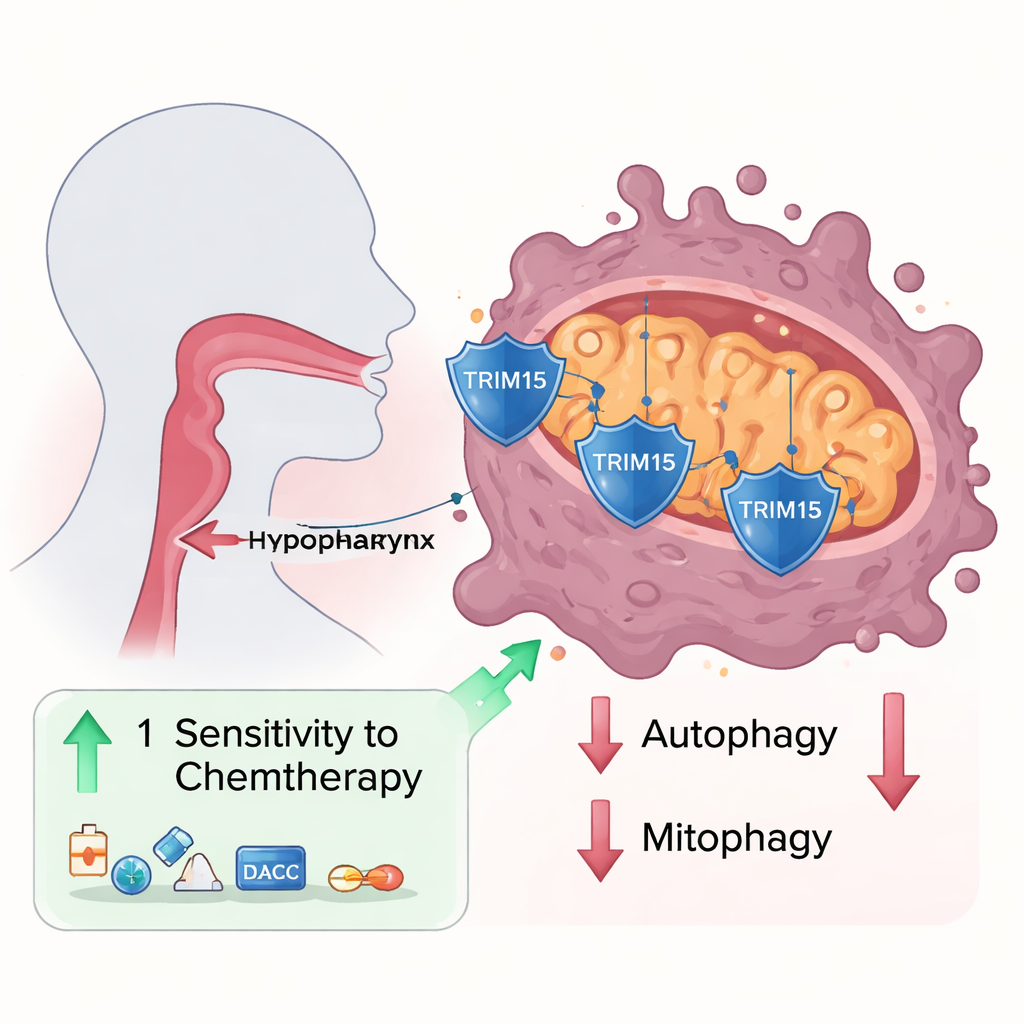
Uma proteína guardiã desaparece
Os pesquisadores examinaram amostras de tumor e linhagens celulares de câncer de hipofaringe e descobriram que uma proteína chamada Trim15 estava consistentemente reduzida em comparação com o tecido normal adjacente. Quando forçaram as células cancerosas a produzir mais Trim15, as células cresceram e migraram mais lentamente; quando a removeram, as células se tornaram mais agressivas. Usando experimentos bioquímicos de pull‑down, descobriram que Trim15 interage fisicamente com outra proteína, VDAC3, que se localiza na membrana externa das mitocôndrias e atua como uma porta para moléculas que entram e saem. Em vez de marcar VDAC3 para destruição, Trim15 adiciona um tipo específico de etiqueta molecular que, na verdade, estabiliza VDAC3, mantendo seus níveis elevados.
Como as células cancerosas reciclam suas usinas de energia
As mitocôndrias são continuamente monitoradas e, quando danificadas, podem ser removidas por um processo especializado de reciclagem chamado mitofagia. A equipe mostrou que VDAC3 normalmente atua como um freio nesse mecanismo de reciclagem. Quando VDAC3 estava abundante, marcadores de autodigestão geral (autofagia) e de mitofagia diminuíam; quando VDAC3 era reduzido, esses processos aceleravam e mais mitocôndrias eram engolfadas e degradadas. Essa mudança também afetou o equilíbrio de espécies reativas de oxigênio (ROS) — moléculas quimicamente reativas frequentemente descritas como o exaustor celular. VDAC3 em altos níveis elevou os níveis de ROS, aumentando o estresse das células, enquanto baixos níveis de VDAC3 permitiram que as células removessem mitocôndrias danificadas, reduzissem ROS e sobrevivessem melhor em condições adversas.
Álcool, estresse oxidativo e resistência a medicamentos
A exposição crônica ao álcool é um grande fator de risco para o câncer de hipofaringe, em parte porque o etanol concentrado banha repetidamente o revestimento da garganta. Quando os pesquisadores expuseram células cancerosas ao álcool em laboratório, tanto Trim15 quanto VDAC3 diminuíram. Essa queda pareceu ser uma manobra adaptativa das células tumorais: ao enfraquecer o eixo Trim15–VDAC3, elas aumentaram a mitofagia, mantiveram os níveis de ROS em patamares mais seguros e toleraram o dano induzido pelo álcool. Uma resposta semelhante ocorreu com o quimioterápico padrão 5‑fluorouracil (5‑FU): o tratamento reduziu Trim15 e VDAC3, o que provavelmente ajuda as células tumorais a evitar estresse oxidativo letal e contribui para a quimiorresistência.
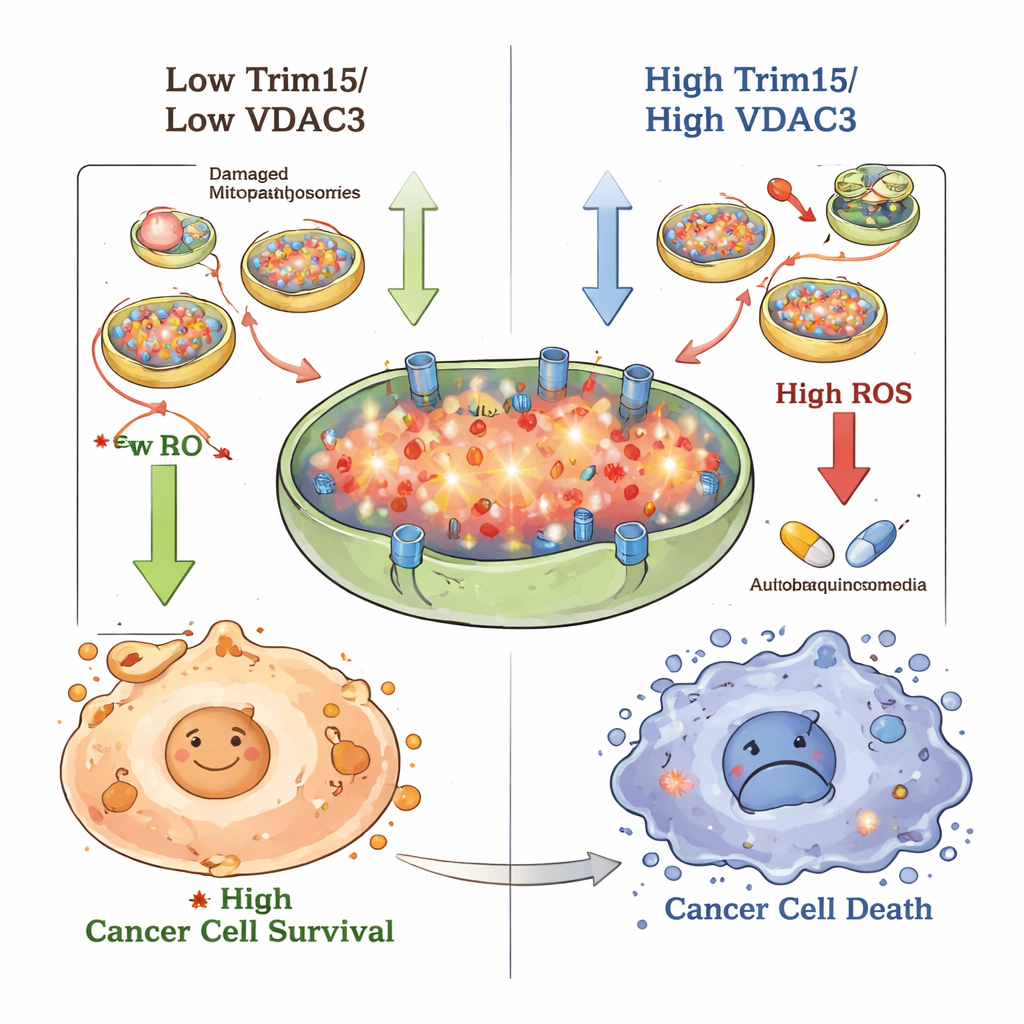
Desligar a autoproteção para potencializar a quimioterapia
A equipe então perguntou se bloquear a autofagia poderia tirar essa proteção. Eles usaram cloroquina, um medicamento antimalárico conhecido que interfere nas etapas finais da autodigestão celular. Em cultura celular, a cloroquina sozinha retardou o crescimento e o movimento das células de câncer de hipofaringe e eliminou a vantagem de crescimento produzida pela perda de VDAC3. Em camundongos portadores de enxertos tumorais humanos, cloroquina e 5‑FU reduziram os tumores individualmente, mas a combinação funcionou melhor, diminuindo o volume e o peso tumoral mais do que cada fármaco isoladamente, sem toxicidade adicional óbvia. Importante, forçar as células a superproduzirem Trim15 ou VDAC3 as tornou mais sensíveis ao 5‑FU, em parte elevando os níveis de ROS a patamares que as células não conseguiam mais controlar.
O que isso significa para tratamentos futuros
Para um público leigo, o estudo mostra que algumas células de câncer de hipofaringe sobrevivem à quimioterapia tornando‑se recicladoras mais eficientes: elas removem rapidamente mitocôndrias danificadas e mantêm o estresse oxidativo justo abaixo do limiar letal. Trim15 e VDAC3 atuam juntos como um contrapeso a esse comportamento — quando presentes, limitam a reciclagem e aumentam o estresse, tornando as células cancerosas mais fáceis de eliminar. Ao direcionar esse eixo Trim15–VDAC3–mitofagia, por exemplo com drogas como a cloroquina adicionadas à quimioterapia padrão, os médicos podem eventualmente tornar tumores de garganta resistentes mais responsivos ao tratamento e melhorar os resultados para os pacientes.
Citação: Wang, G., Shen, Y., Wang, L. et al. Trim15 stabilizes VDAC3 via ubiquitination to suppress autophagy and enhance chemosensitivity in hypopharyngeal squamous cell carcinoma. Cell Death Discov. 12, 88 (2026). https://doi.org/10.1038/s41420-026-02943-0
Palavras-chave: câncer de hipofaringe, autofagia, mitocôndrias, resistência à quimioterapia, cloroquina