Clear Sky Science · pt
Rottlerin desencadeia degradação dupla de SLC7A11 e GPX4 para induzir ferroptose e quimiossensibilização no carcinoma hepatocelular
Por que este composto natural importa para o câncer de fígado
O carcinoma hepatocelular, a forma mais comum de câncer primário de fígado, frequentemente é diagnosticado tardiamente e continua difícil de tratar. Este estudo investiga se uma molécula de origem vegetal chamada rottlerin, conhecida há muito tempo por seus amplos efeitos anticâncer, pode ser usada para desencadear uma forma mais recente de morte celular chamada ferroptose em células de câncer de fígado. Ao entender como a rottlerin age no nível molecular, os pesquisadores esperam abrir novas vias para tratamentos mais eficazes e menos sujeitos a resistência.
Uma nova maneira de matar células tumorais
Fármacos anticâncer tradicionais normalmente empurram as células tumorais para programas de morte bem conhecidos, como a apoptose. A ferroptose é diferente: é um processo dependente de ferro conduzido pelo acúmulo de lipídios tóxicos nas membranas celulares. Células de câncer de fígado são especialmente vulneráveis a esse tipo de dano porque dependem fortemente de sistemas antioxidantes para controlar esses tóxicos lipídicos. A equipe investigou se a rottlerin poderia sabotar essas defesas e, assim, forçar as células tumorais hepáticas a entrar em ferroptose.
Como a rottlerin desacelera o crescimento tumoral
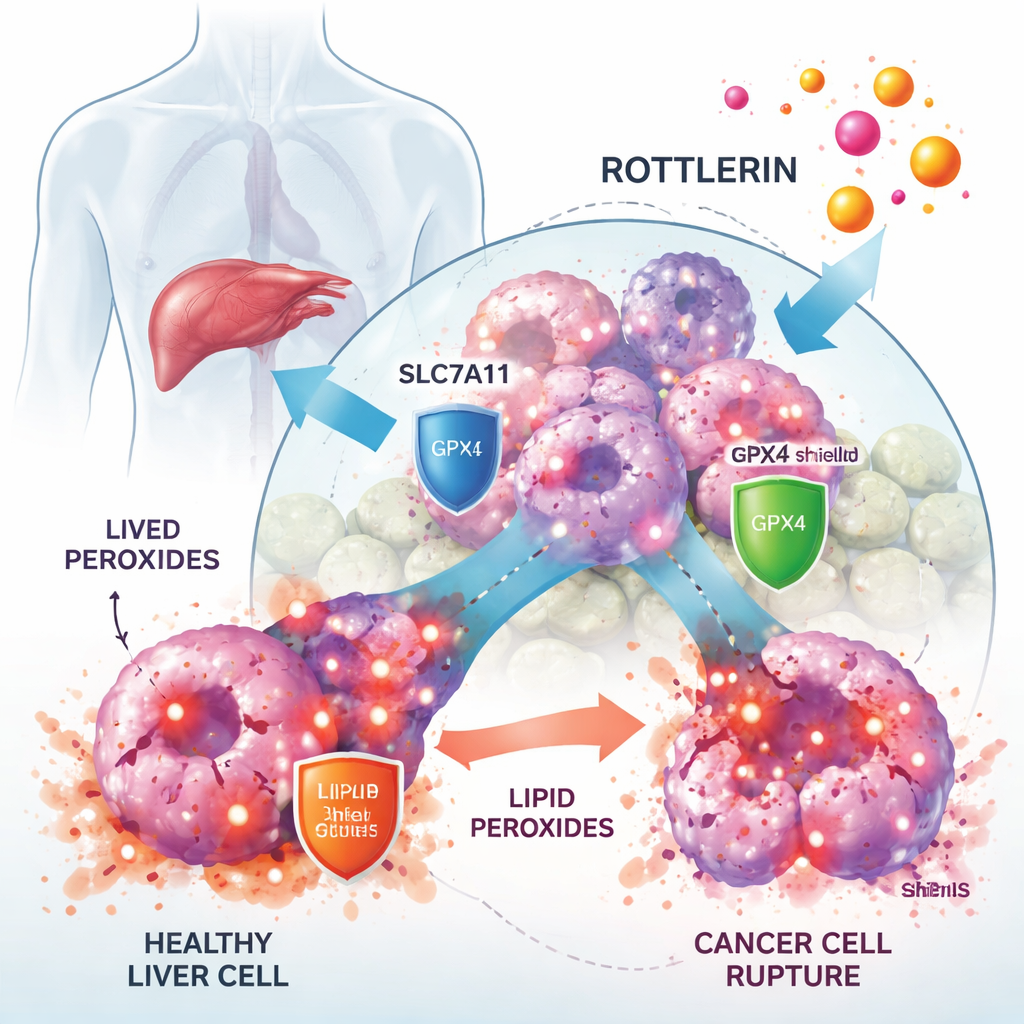
Trabalhando com linhagens celulares humanas de câncer de fígado, os pesquisadores mostraram que a rottlerin reduziu fortemente o crescimento das células tumorais em doses micromolares baixas, enquanto células relacionadas ao fígado normais foram menos afetadas. Quando adicionaram um bloqueador específico de ferroptose chamado Ferrostatin‑1, grande parte da morte celular induzida pela rottlerin foi revertida, sugerindo fortemente que a ferroptose era o principal modo de morte. Microscopia e testes bioquímicos corroboraram isso: células tratadas com rottlerin acumularam altos níveis de peróxidos lipídicos, exibiram mitocôndrias alteradas e mostraram quantidades reduzidas do antioxidante glutationa, todas características da ferroptose.
Desarmando os escudos antioxidantes das células
As células de câncer de fígado sobrevivem apoiando‑se em um eixo defensivo crítico formado pelo transportador SLC7A11 e pela enzima GPX4. SLC7A11 importa cistina, um bloco de construção para a glutationa, enquanto GPX4 usa glutationa para neutralizar peróxidos lipídicos antes que danifiquem as membranas. O estudo descobriu que a rottlerin causou a queda dos níveis de proteína de SLC7A11 e GPX4 ao longo do tempo. Isso não ocorreu porque as células deixaram de sintetizá‑las, mas porque as proteínas foram marcadas com pequenas etiquetas de “destrua‑me” (ubiquitina) e encaminhadas para a maquinaria de degradação proteica da célula, o proteassoma. Bloquear o proteassoma reverteu essa perda, e aumentar artificialmente SLC7A11 ou GPX4 nas células as protegeu parcialmente da rottlerin. Em conjunto, esses achados mostram que a rottlerin atua como um degradador duplo de duas defesas centrais contra a ferroptose.
Potencializando fármacos já usados contra câncer de fígado
Muitos pacientes com câncer de fígado avançado recebem sorafenibe, um fármaco padrão de primeira linha que pode por si só induzir ferroptose, mas a resistência frequentemente limita seu benefício. Os autores testaram se doses baixas, por si só fracas, de rottlerin poderiam tornar as células tumorais mais sensíveis a fármacos indutores de ferroptose, como sorafenibe e RSL3. Em culturas celulares, a combinação de rottlerin em baixa dose com qualquer um desses fármacos aumentou marcadamente a morte das células tumorais e deslocou curvas dose‑resposta, indicando potência maior. Importante, esse efeito sensibilizante persistiu mesmo quando a proteína alvo clássica da rottlerin, PKCδ, foi reduzida geneticamente, mostrando que a ação chave não se dava por essa quinase, mas sim pela degradação de SLC7A11 e GPX4. Em modelos de camundongos com tumores hepáticos humanos, o tratamento combinado com rottlerin e sorafenibe desacelerou o crescimento tumoral mais do que o sorafenibe sozinho e reduziu ainda mais os níveis de SLC7A11 e GPX4 nos tumores.
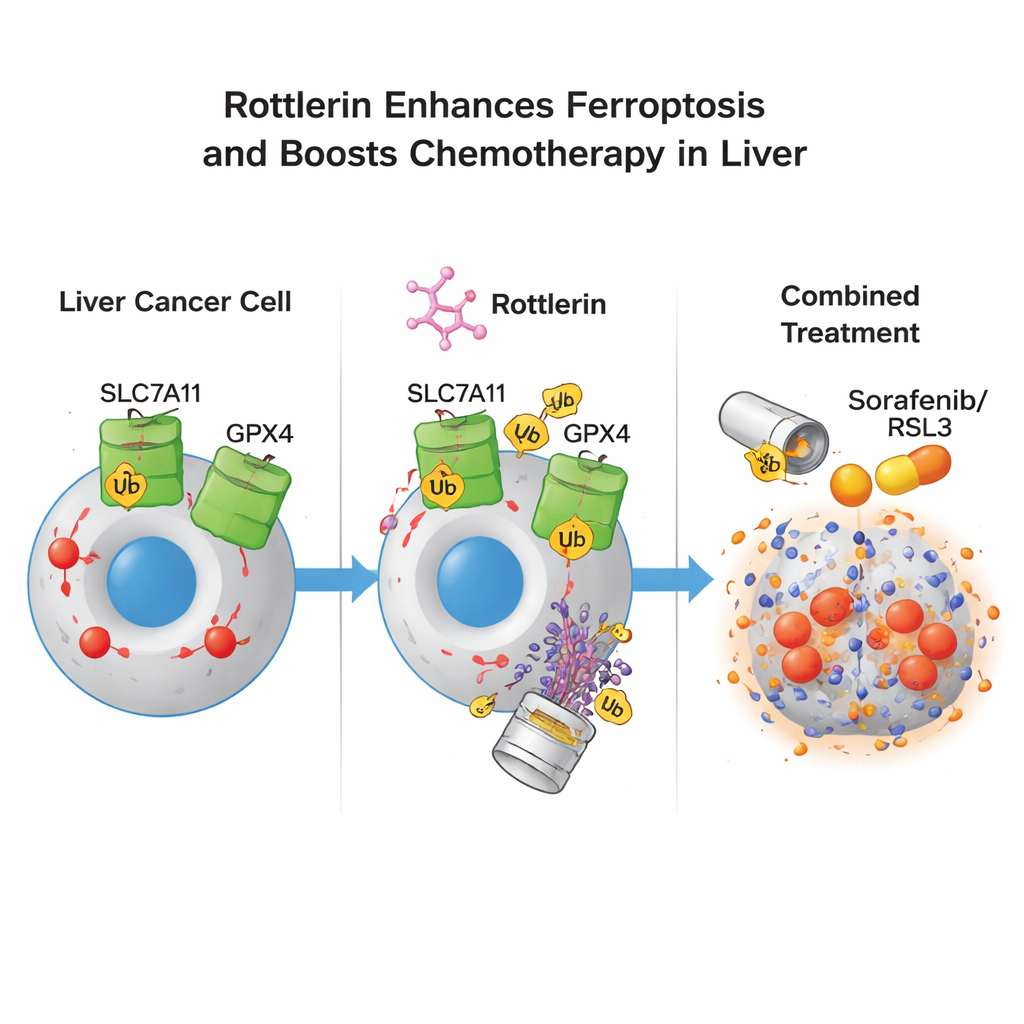
O que isso pode significar para tratamentos futuros
Para não especialistas, a mensagem é que a rottlerin age como uma “chave mestra dupla” nas células de câncer de fígado: ela remove simultaneamente dois fechos cruciais — SLC7A11 e GPX4 — que normalmente protegem as células de uma onda letal de oxidação lipídica. Uma vez que esses fechos se foram, as células tumorais tornam‑se muito mais propensas a sofrer ferroptose, especialmente quando combinadas com fármacos existentes que as empurram nessa direção. Embora sejam necessários mais estudos antes que a rottlerin ou compostos relacionados possam ser usados em pacientes, essa estratégia de degradador duplo oferece uma maneira promissora de contornar as defesas adaptativas que frequentemente tornam os tumores hepáticos tão difíceis de tratar.
Citação: Luo, H., Jin, X., Gao, C. et al. Rottlerin triggers dual degradation of SLC7A11 and GPX4 to drive ferroptosis and chemosensitization in hepatocellular carcinoma. Cell Death Discov. 12, 89 (2026). https://doi.org/10.1038/s41420-026-02942-1
Palavras-chave: câncer de fígado, ferroptose, rottlerin, SLC7A11, GPX4